Содержание
- 2. СТРОЕНИЕ. Медь-элемент побочной подгруппы 1 группы. Строение атома: +12Сu 1s2|2s22p6|3s23p63d10|4s1|
- 3. Нахождение в природе. Медь встречается в природе в основном в связанном виде и входит в состав
- 4. Физические свойства. Медь – металл светло-розового цвета, тягучий, вязкий, легко прокатывается. Температура плавления 1083 градуса по
- 5. Химические свойства. В сухом воздухе и при обычной температуре медь почти не изменяется. А при повышенной
- 6. Взаимодействие с простыми веществами. С кислородом 2Cu+O2 2CuO оксид меди(2) С серой Cu+S CuS сульфид меди
- 7. Взаимодействие со сложными веществами. Находясь в ряду напряжений левее водорода медь не вытесняет водород из разбавленных
- 8. Получение. Процесс получения меди весьма сложный. Упрощенно процесс ее производства из медного блеска отразить можно так:
- 9. Применение. Чистая медь используется в электротехнической промышленности для изготовления электрических проводов, кабелей и в теплообменных аппаратах.
- 10. Соединения меди. CuSO4 –сульфат меди (белый порошок). CuSO4*5H2O –медный купорос (голубой порошок). CuCl2*2H2O –хлорид меди (темно-зеленый
- 12. Скачать презентацию









 Аміни
Аміни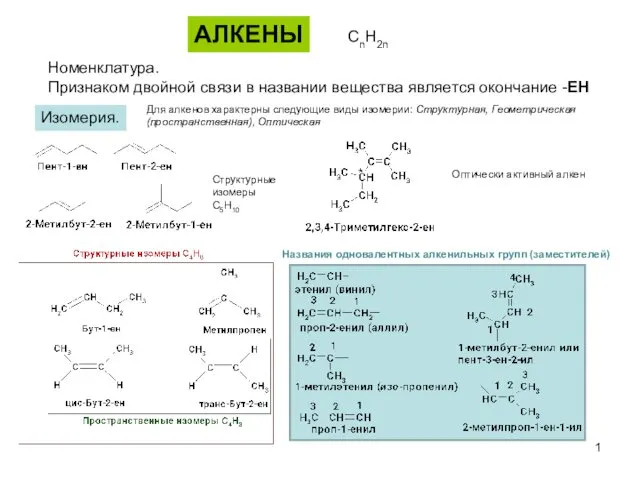 Алкены
Алкены Биохимия старения. (Лекция 24)
Биохимия старения. (Лекция 24) Альдегиды
Альдегиды Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Стекло, его происхождение и значение в жизни человека
Стекло, его происхождение и значение в жизни человека Количества вещества
Количества вещества Презентация по дисциплине «Химия» на тему: «Сложные эфиры» Автор: Садыгова Елена, студентка группы Т-1 Руководитель: Лебединск
Презентация по дисциплине «Химия» на тему: «Сложные эфиры» Автор: Садыгова Елена, студентка группы Т-1 Руководитель: Лебединск Цинк. Знаходження в періодичній системі і основні характеристики
Цинк. Знаходження в періодичній системі і основні характеристики Классификация химических элементов в географической оболочке
Классификация химических элементов в географической оболочке Растворы
Растворы Электролитическая диссоциация
Электролитическая диссоциация Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика
Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика Презентация Угольная кислота
Презентация Угольная кислота Технология получения сплавов с заданными свойствами
Технология получения сплавов с заданными свойствами Химия
Химия Кислоты
Кислоты Секвенирование Ion Chip. Технология CMOS и устройство чипа для секвенирования
Секвенирование Ion Chip. Технология CMOS и устройство чипа для секвенирования Көмірсулар. Моносахаридтер
Көмірсулар. Моносахаридтер Пластмаси. Види пластмас. (11 клас)
Пластмаси. Види пластмас. (11 клас) Вероятность протекания химических реакций. Скорость химических реакций
Вероятность протекания химических реакций. Скорость химических реакций Открытие водорода
Открытие водорода Коррозия металлов
Коррозия металлов Химические реакторы
Химические реакторы Неравновесные явления в растворах электролитов
Неравновесные явления в растворах электролитов Пищевая биотехнология
Пищевая биотехнология Аттестационная работа. Образовательная программа, элективный курс Химия в задачах и упражнениях
Аттестационная работа. Образовательная программа, элективный курс Химия в задачах и упражнениях Комплексные соединения
Комплексные соединения