Содержание
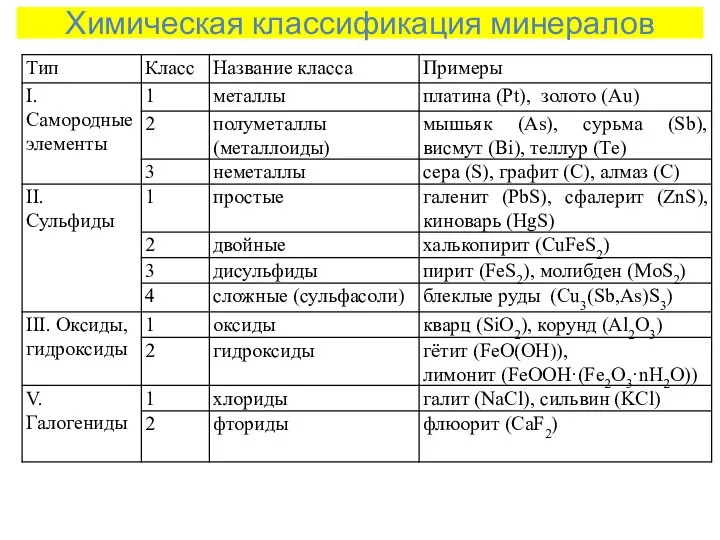
- 2. 1. Химическая классификация минералов Классификация основана на разделении минералов по: химическому составу; структурным (кристаллохимическим) связям
- 3. Химическая классификация минералов
- 5. Тип I. Самородные минералы Состоят из одного химического элемента и называемые по этому элементу (всего 30
- 6. серебро самородная сурьма графит Самородный мышьяк
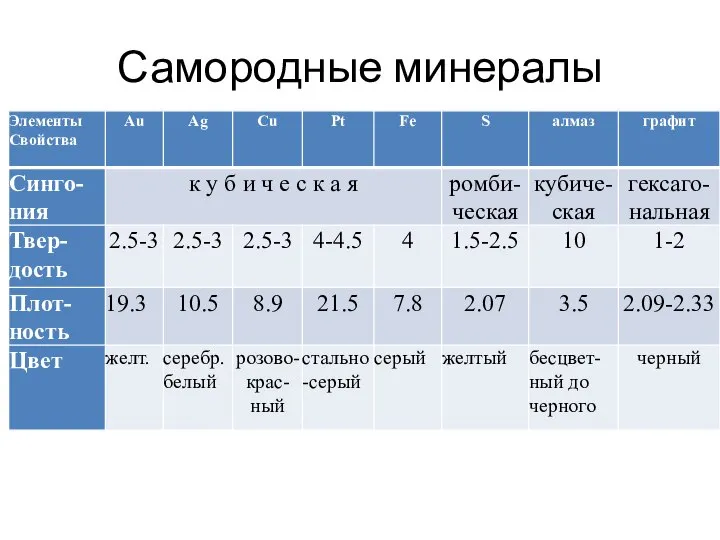
- 7. Самородные минералы
- 8. Происхождение самородных минералов В основном, образуются при эндогенных процессах в интрузивных породах и кварцевых жилах, сера
- 9. Применение ювелирное производство и валютные запасы ( Au , Pt , Ag , алмазы); культовые предметы
- 10. Тип II. Сульфиды и их аналоги Природные соединения металлов и полуметаллов с серой (производные сероводорода), с
- 11. В зависимости от особенностей физических свойств, все сульфиды имеют второе название, т.к. делятся на: блески -
- 12. Колчеданы (от др.-греч колония в Малой Азии) — устар. собирательное название, применявшееся в отношении минералов из
- 13. Происхождение сульфидов Преимущественно, гидротермальное, являются рудами металлов, сопутствуют нефти и природному газу, содержатся в вулканическом пепле
- 14. ОБЩИЕ ЧЕРТЫ: Яркая окраска, чёрная или тёмная черта, металлический блеск, высокая и средняя отражательная способность, низкая
- 15. Тип III. Оксиды и гидроксиды Соединения металлов и полуметаллов (металлоидов) с кислородом: Широко распространены в природе
- 16. Простые оксиды – соединения одного элемента с кислородом - кварц (диоксид кремния - SiO2) Сложные оксиды
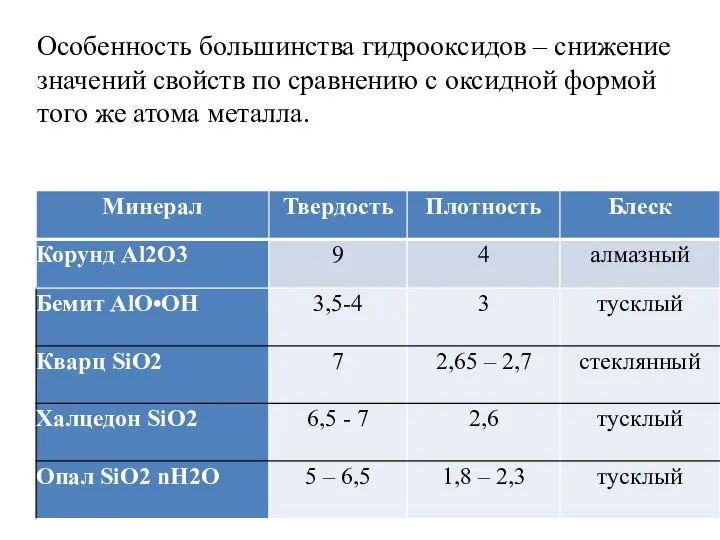
- 17. Особенность большинства гидрооксидов – снижение значений свойств по сравнению с оксидной формой того же атома металла.
- 18. Происхождение оксидов и гидроксидов Представляют собой продукты экзогенных процессов, протекающих в самых верхних частях земной коры
- 19. Использование оксидов и гидроксидов Для получения Fe , Mn , Al , Sn . Прозрачные, кристаллические
- 20. Тип IV. Соли кислородных кислот (кислородные соли, оксисоли) Кл. 1. Карбонаты — соли угольной кислоты (H2CO3)
- 21. Неорганические соединения углерода в природе, известно около 240 минералов, большая часть из которых относится к солям
- 22. Наиболее распространенными являются карбонаты: безводные - кальцит СаСО3; магнезит MgСО3; доломит СаМg (СО3)2; сидерит FeСО3 с
- 23. В большинстве случаев карбонаты образуются в гипергенных процессах (хотя известны и магматические карбонаты). Происхождение некоторых карбонатов,
- 24. Кристаллизуются в ромбической и тригональной сингониях (хорошие кристаллические формы и спайность по ромбу); Цвет: большинство белые
- 25. Большинство карбонатов относительно хорошо растворяются в воде богатой свободной углекислотой по схеме СаСО3 + СО2 +
- 26. являются породообразующими минералами осадочных пород (известняки, доломиты и др.) и метаморфических пород (мрамор, скарны); используются как
- 27. Класс 2. Сульфаты — соли серной кислоты (H2SO4) В природе известно около 300 минералов (155), относящихся
- 28. Наиболее распространены и известны сульфаты Ca, Ba, Sr, Pb: гипс (CaSO4.2H2O), ангидрит (CaSO4), барит или тяжёлый
- 29. Общие свойства сульфатов: кристаллизация в моноклинной и ромбической сингониях, небольшая твердость (меньше 3,5), светлая окраска, стеклянный
- 30. Класс 3. Фосфаты (165 минеральных видов) — соли ортофосфорной (H3PO4) кислоты В большинстве своем гипергенные минералы,
- 31. Класс 4. Вольфроматы – соли вольфрамовой (H2WO4) кислоты Вольфраматы в природе не многочислены. Однако в рассматриваемый
- 32. Класс 5. Молибдаты — соли молибденовой (H2MoO4) кислоты Большинство молибдатов являются гипергенными минералами, образующихся в зонах
- 33. Класс 6. Хроматы - представители солей ортохромовой кислоты (H2CrO4) - очень редки (около 10 минералов). Встречаются
- 34. Класс 7. Бораты - кальциевые и магниевые соли борных кислот H3BO3, HBO2, H2B4O7 Относятся более 100
- 35. Класс 8. Ванадаты — группа минералов, представляющих собой различные по составу и сложности соли ортованадиевой кислоты
- 36. Класс 9. Арсенаты — соли ортомышьяковой (H3AsO4) кислоты Включает около 120 минералов. В комплексном анионе AsO43-
- 37. Класс 10. Силикаты – соли кремниевых кислот Минералы сложного химического состава, самый многочисленный класс, насчитывающий до
- 38. А. Островные (сложены изолированными тетраэдрами) – группы оливина, гранатов, циркона, ставролита, дистена (кианита), топаз и кольцевые
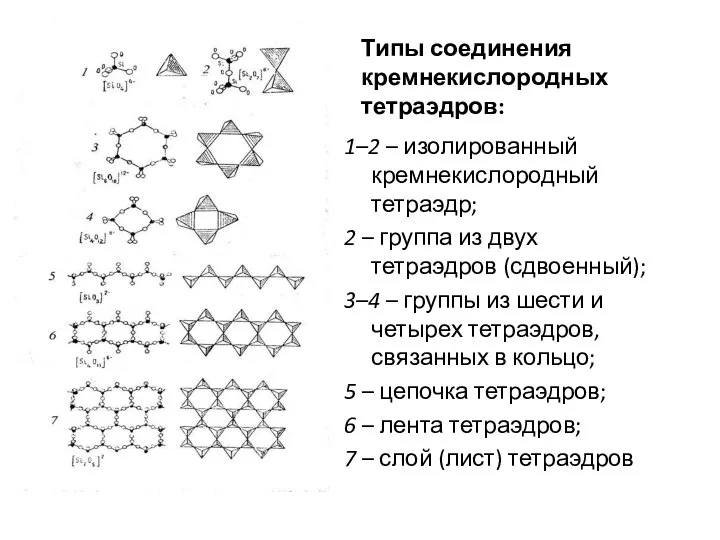
- 39. Типы соединения кремнекислородных тетраэдров: 1–2 – изолированный кремнекислородный тетраэдр; 2 – группа из двух тетраэдров (сдвоенный);
- 40. Островные силикаты Оливин Ставролит Дистен (кианит) Топаз Гранаты Циркон
- 41. Кольцевые силикаты – встречаются сравнительно редко, состоят из 3-х или 6-ти тетраэдров, замкнутых в кольца Берилл
- 42. ЦЕПОЧЕЧНЫЕ СИЛИКАТЫ Группа пироксенов Кристаллическая решетка построена из простых одинарных цепочек кремнекислородных тетраэдров, между которыми катионы
- 43. Ленточные силикаты Ленточные силикаты с радикалом [Si4O11]6-объединяют минералы группы амфиболов – минералов с непостоянным химическим составом,
- 44. Слоистые (слоевые, листовые) силикаты Представляют непрерывные слои, где тетраэдры связаны ионами кислорода, а между слоями связь
- 45. Слоистые (слоевые, листовые) силикаты Представляют непрерывные слои, где тетраэдры связаны ионами кислорода, а между слоями связь
- 46. Наиболее сложная структура – бесконечные трёхмерные решётки или каркасы, состоящие из связанных между собой тетраэдров, через
- 47. Сложный химический состав и разнообразие кристаллической структуры дают большой разброс показателей физических свойств: Твёрдость: от 1
- 48. Многие силикаты являются полезными ископаемыми и применяются в народном хозяйстве. Это строительные материалы, облицовочные, поделочные и
- 49. Тип V. Галогениды (рождающие соль) или галоиды, галогены – соединения галогенов (электроотрицательных) с другими химическими элементами
- 50. Взаимодействие с водой: большинство растворимы Вкус: горько-соленый Гигроскопичность: интенсивно поглощают влагу из воздуха и расплываются в
- 51. Наиболее распространены: Класс 1. Хлориды — соли соляной кислоты (HСl), насчитывается до 25 минералов: галит (NaCl),
- 52. ОБЩИЕ СВОЙСТВА ДЛЯ ГАЛОГЕНИДОВ низкая твердость, кристаллизация в кубической сингонии, совершенная спайность, широкая цветовая гамма, прозрачность,
- 54. Скачать презентацию





































![Ленточные силикаты Ленточные силикаты с радикалом [Si4O11]6-объединяют минералы группы амфиболов –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1386671/slide-42.jpg)









 Транскрипция. Биосинтез РНК. (Лекция 7)
Транскрипция. Биосинтез РНК. (Лекция 7) Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Кислоты. Определение кислот
Кислоты. Определение кислот Текстиль материалдарың колорлауда нанотехнологияның жетісіктері
Текстиль материалдарың колорлауда нанотехнологияның жетісіктері Организация дипептида
Организация дипептида Көмірсулар
Көмірсулар Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Вода, ее физические и химические свойства, гигиеническое и экологическое значение (лекция №3)
Вода, ее физические и химические свойства, гигиеническое и экологическое значение (лекция №3) Конструкционные и функциональные волокнистые композиты. Органические волокна
Конструкционные и функциональные волокнистые композиты. Органические волокна Физическая и коллоидная химия
Физическая и коллоидная химия Белоктар. Биохимиясы
Белоктар. Биохимиясы Мы́ло — жидкий или твёрдый продукт, содержащий поверхностноактивные вещества
Мы́ло — жидкий или твёрдый продукт, содержащий поверхностноактивные вещества Гидролиз солей
Гидролиз солей Периодический закон и периодическая система химических элементов д.и.менделеева в свете учения о строении атома
Периодический закон и периодическая система химических элементов д.и.менделеева в свете учения о строении атома Единый государственный экзамен Химия 2021
Единый государственный экзамен Химия 2021 Презентация по Химии "Свойства растворов электролитов" - скачать смотреть
Презентация по Химии "Свойства растворов электролитов" - скачать смотреть  Презентация по Химии "Периодический закон и периодическая система элементов" - скачать смотреть бесплатно
Презентация по Химии "Периодический закон и периодическая система элементов" - скачать смотреть бесплатно Фолиевая кислота
Фолиевая кислота  Химия и проблемы экологии. Кислотные дожди
Химия и проблемы экологии. Кислотные дожди Коррозия металлов
Коррозия металлов Органическая химия. (Урок 1-2)
Органическая химия. (Урок 1-2) Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №1 с.Успенского Успенского района Краснодарско
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №1 с.Успенского Успенского района Краснодарско Презентация по Химии "Железо: ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА" - скачать смотреть
Презентация по Химии "Железо: ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА" - скачать смотреть  МЕТАЛЛЫ Химические и физические свойства металлов
МЕТАЛЛЫ Химические и физические свойства металлов Презентация по Химии "Физические и химические свойства кислот. 8-й класс" - скачать смотреть
Презентация по Химии "Физические и химические свойства кислот. 8-й класс" - скачать смотреть  Модифицированные природные полимеры
Модифицированные природные полимеры Самородные элементы
Самородные элементы Мембранное материаловедение. Топливные элементы
Мембранное материаловедение. Топливные элементы