Содержание
- 2. Коррозия металлов и защита от нее. План 1. Введение. Виды коррозионных разрушений. 2. Типы коррозионных процессов:
- 3. Коррозия – самопроизвольно протекающий процесс разрушения металлов в результате взаимодействия с окружающей средой. Me0 – nē
- 4. ВИДЫ КОРРОЗИОННЫХ РАЗРУШЕНИЙ Особенно опасна, т.к. металл рассыпается наиме-нее опасна, теряет-ся 5% механ. свойств
- 5. Например, питтинг образуется при литье по выплавляемым моделям отливок из легированных сталей за счет взаимодействия материалов
- 6. ТИПЫ КОРРОЗИОННЫХ ПРОЦЕССОВ: Химическая коррозия: обмен электронами непосредственно между металлом и окислителем m Me + n
- 7. Газовая коррозия: в среде агрессивных газов (О2, F2, Cl2, SO2, NO2 и т.д.) Высокотемпературная Коррозия в
- 8. Все металлы окисляются кислородом воздуха: 2Ме (к) + О2 (г) ↔→ 2МеО (к); МеО (к) →
- 9. Газовая коррозия углеродистой стали, чугуна: Fe + O2 → FeO + Fe3O4 + Fe2O3 окалина Одновременно
- 10. Электрохимическая коррозия может возникать: - при контакте с электролитом двух металлов различной активности или сплава двух
- 11. По степени термодинамической неустойчивости к электрохимической коррозии: 1. Металлы повышенной термодинамической нестабильности: щелочные и щелочно-земельные, Al,
- 12. 3. Металлы промежуточной термодинамической стабильности: Bi, Sb, Re, Tc, Cu, Ag, Rh 0В 4. Металлы высокой
- 13. Коррозия железа с примесями меди: В кислой среде: К: 2Н+ + 2ē = Н2 Fe2+ +
- 14. коррозия углеродистой стали в различных средах: в этой паре катодными (пассивными) участками являются зерна карбида железа
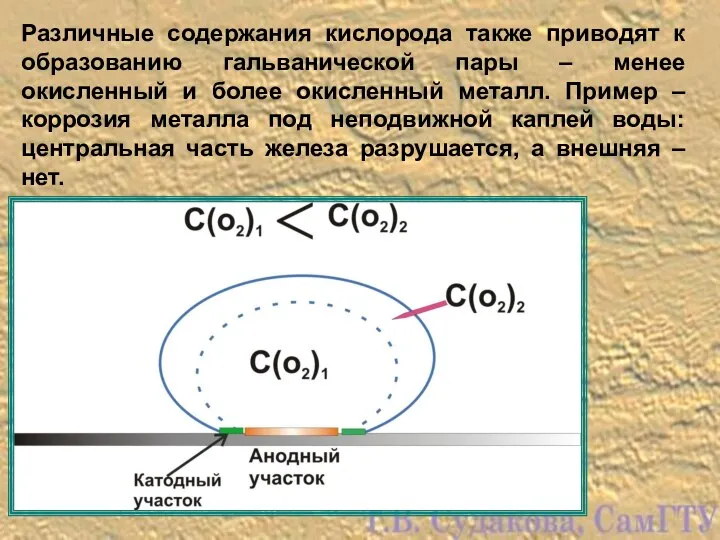
- 15. Различные содержания кислорода также приводят к образованию гальванической пары – менее окисленный и более окисленный металл.
- 16. Во всех вариантах для появления катодно-анодных участков необходимо условие неравномерности запаса энергии на каком-то участке поверхности
- 17. Нержавеющая сталь – сплав, содержащий как минимум 12% Cr, который создает на поверхности очень тонкий слой
- 18. ЗАЩИТА ОТ КОРРОЗИИ Изоляция металлов от агрессивной среды: Металлические покрытия (от высокотемпературной коррозии) 2) Покрытия от
- 19. Защитные слои от высокотемпературной коррозии могут быть созданы из тугоплавких соединений, обладающих низкой диффузионной проницаемостью для
- 20. 1200С Процесс металлизации распылением заключается в непрерывном плавлении металла, распылении его на мельчайшие частицы и нанесении
- 21. При металлизации сцепление частиц с основанием происходит вследствие шероховатости поверхности и под действием молекулярных сил и
- 22. Протекторные свойства металлизационных покрытий из Al, Zn и их сплавов. Поврежденное место на покрытии за счет
- 23. Сплавы Zn и Al (Zn/Al15, Zn/Al5) создают покрытия, стойкие к любым атмосферам, что объясняется быстрым заполнением
- 24. Zn и Al образуют плотный слой продуктов коррозии, по объему значительно больший, чем металл, из которого
- 25. металлические неметаллические Zn, Al, Sn, Cd, Ni, Cr, Ag, Cu, Au Лак, краска, эмаль Кислотоупорные материалы
- 26. Ингибирование коррозионно-активной среды. Ингибиторы – вещества, которые будучи введены в коррозионную среду в небольших количествах (от
- 27. Пример: для защиты стальных трубопроводов используют Са(НСО3)2. На катодных участках происходит восстановление растворенного в воде кислорода
- 28. Катодная защита: потенциал металла специально сдвигают из области активного растворения в более отрицательную область относительно потенциала
- 29. Основные протекторы для стали: Mg, Al, Zn и их сплавы. Протекторные сплавы: основа – магний, Al
- 30. Схема расположения анодов на автомобилях ГАЗель (рекомендуемое кол-во анодов – 13 шт) В местах, наиболее подверженных
- 31. Метод внешнего потенциала – защищаемое изделие или конструкция подключаются к отрицательному полюсу динамомашины или выпрямителя и
- 32. Коррозия трубопроводов в грунте за счет неодно-родности металла трубы и гетероген-ности грунта возникают участки с различным
- 33. Цветная нержавеющая сталь Под воздействием различных электрохимических воздействий на поверхности нержавеющей стали может образовываться защитная пленка
- 35. Скачать презентацию































 Ионная химическая связь
Ионная химическая связь Нефть и продукты ее переработки
Нефть и продукты ее переработки Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна
Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна  Структурні дослідження електрохімічних інтерфейсів методами малокутового розсіяння нейтронів та нейтронної рефлектометрії
Структурні дослідження електрохімічних інтерфейсів методами малокутового розсіяння нейтронів та нейтронної рефлектометрії Графические таблицы текущего цемента с 2 ПЛ
Графические таблицы текущего цемента с 2 ПЛ Введение. Биохимия
Введение. Биохимия Презентация Фосфор 9 класс
Презентация Фосфор 9 класс Химические вещества парабены
Химические вещества парабены Несовместимые сочетания лекарственных веществ. Способы преодоления несовместимости
Несовместимые сочетания лекарственных веществ. Способы преодоления несовместимости Каталітичні процеси нафтопереробки
Каталітичні процеси нафтопереробки Основные понятия и законы химии
Основные понятия и законы химии Силикатная промышленность
Силикатная промышленность Полимеры, пластмассы и волокна
Полимеры, пластмассы и волокна Алкины. Номенклатура и изомерия
Алкины. Номенклатура и изомерия Полимеры. Пластмассы
Полимеры. Пластмассы Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Углерод и кремний
Углерод и кремний Растворы. Основные понятия. Концентрация. Законы Рауля
Растворы. Основные понятия. Концентрация. Законы Рауля Способы получения оксидов, оснований, кислот и солей. Урок №2
Способы получения оксидов, оснований, кислот и солей. Урок №2 Строение и свойства металлов. Аллотропия. Анизотропия. Кристаллизация. Дендрит. Строение стального слитка. Ликвация. (Лекция 1)
Строение и свойства металлов. Аллотропия. Анизотропия. Кристаллизация. Дендрит. Строение стального слитка. Ликвация. (Лекция 1) Свойства атомов
Свойства атомов Гігієна води. Лекція 6
Гігієна води. Лекція 6 Неметаллы: общая характеристика
Неметаллы: общая характеристика Їх згубна дія на організм людини СПИРТИ
Їх згубна дія на організм людини СПИРТИ  Базальты. Классификация основных пород
Базальты. Классификация основных пород Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства
Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства Прикладная химия. Теплоперенос в химических реакторах и теплообменники
Прикладная химия. Теплоперенос в химических реакторах и теплообменники Этот многоликий цинк
Этот многоликий цинк