Содержание
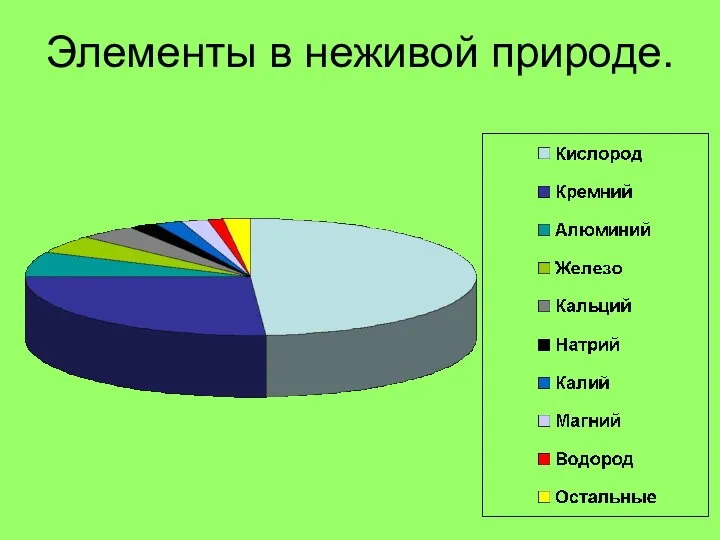
- 2. Элементы в неживой природе.
- 3. Нахождение в природе. Самородные элементы Сера Графит С Алмаз С Азот и кислород, инертные газы в
- 4. Нахождение в природе ← Апатиты Р Галит NaCl → ← FeS2 пирит Кварц SiO2 →
- 5. Неметаллы - это химические элементы, которые могут проявлять свойства как окислителя ( принимают электроны), так и
- 6. Соединения неметаллов. Оксиды – только кислотные SO3, SO2, CO2 и другие. (кроме NO и CO –безразличные)
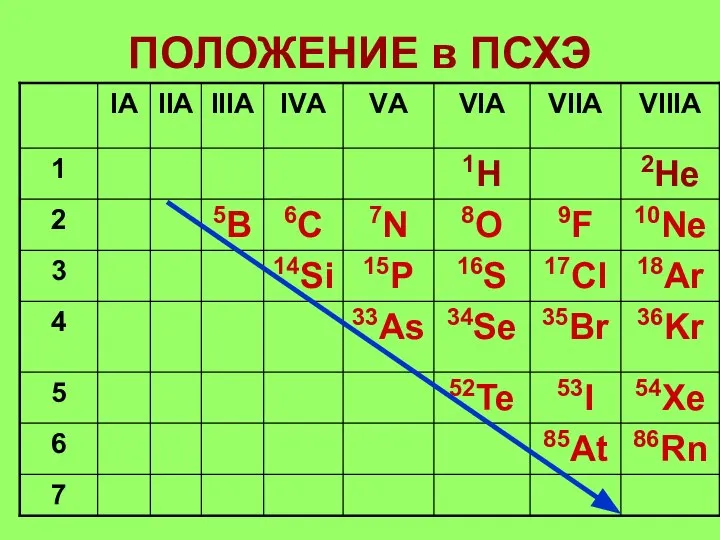
- 7. ПОЛОЖЕНИЕ в ПСХЭ
- 8. ЭЛЕМЕНТЫ - IA,IIIA,IVA Н
- 9. ПНИКТОГЕНЫ -VA Р
- 10. ХАЛЬКОГЕНЫ -VIA
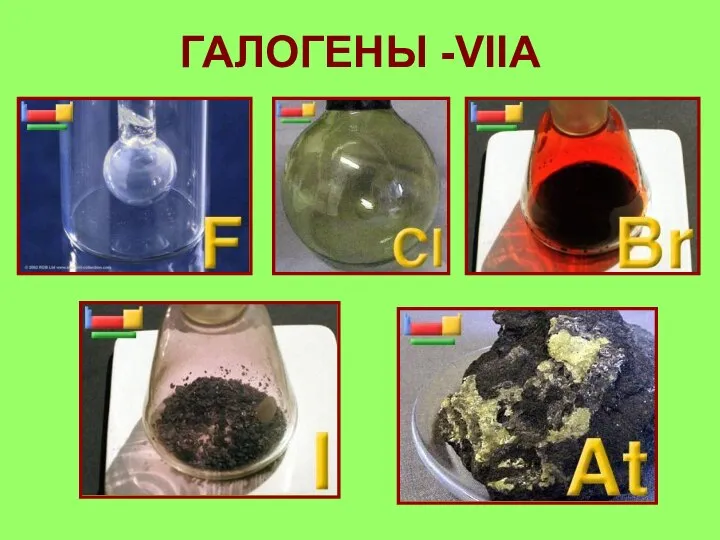
- 11. ГАЛОГЕНЫ -VIIA
- 12. ИНЕРТНЫЕ ГАЗЫ-VIIIA
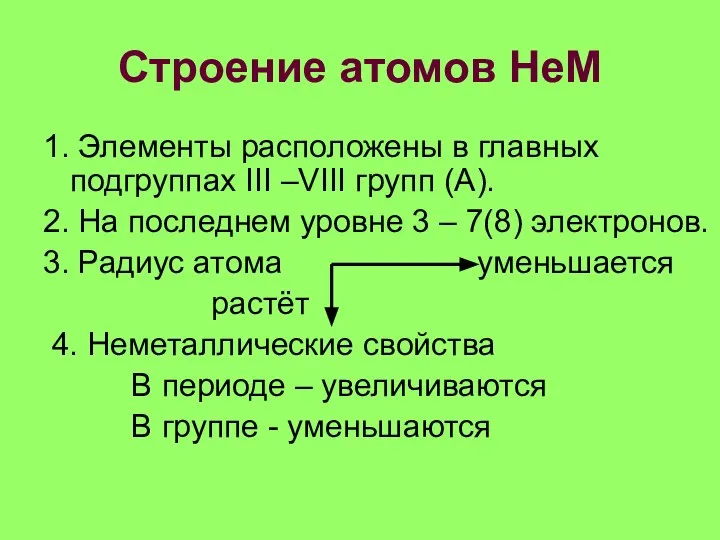
- 13. Строение атомов НеМ 1. Элементы расположены в главных подгруппах III –VIII групп (А). 2. На последнем
- 14. Строение атомов НеМ 5. Высокая электроотрицательность. 6. Принимают электроны и отдают. 7. НеМ → кислотный оксид→кислота
- 15. Физические свойства Агрегатное состояние. Газообразные – азот, кислород, хлор, инертные газы, водород. Жидкий – бром, Твёрдые
- 16. Строение неметаллов. Молекулярное (НеМ)х, где Х = 1 Инертные газы He, Ar, Ne… X=2 H2, Cl2,
- 17. Кислород, водород – пример газообразных бесцветных неметаллов
- 18. Хлор (как и фтор) – окрашенные газообразные неметаллы. При растворении хлора в воде получается хлорная вода
- 19. Бром – жидкость красно-бурого цвета При растворении брома в воде получается бромная вода
- 20. При растворении брома в воде получается бромная вода
- 21. Большинство неметаллов имеют твёрдое агрегатное состояние Сера – кристаллическое вещество жёлтого цвета Красный фосфор Углерод (уголь)
- 22. Неметаллы малорастворимы в воде Уголь Фосфор Сера не смачивается водой
- 23. Химические свойства. 1. Реагируют с металлами. 2. С кислородом. 3. С водородом. 4. С кислотами. 5.
- 25. Скачать презентацию


















 Комплексные соединения. Природа химической связи: метод молекулярных орбиталей
Комплексные соединения. Природа химической связи: метод молекулярных орбиталей Реакции ионного обмена
Реакции ионного обмена Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.
Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.  Лекция 3. Протолитические равновесия и процессы
Лекция 3. Протолитические равновесия и процессы Химия. Введение
Химия. Введение Железо Fe. Строение атома
Железо Fe. Строение атома Халькогены. Кислород в природе
Халькогены. Кислород в природе Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б
Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б Презентация по Химии "Биогенные элементы" - скачать смотреть бесплатно
Презентация по Химии "Биогенные элементы" - скачать смотреть бесплатно Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Э.М. Спиридонов. Эволюция минералов олова в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов олова в зоне гипергенеза Углерод и 4 группа
Углерод и 4 группа Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Регуляция и интеграция обмена веществ
Регуляция и интеграция обмена веществ Урок у 8 класі на тему: «Класифікація неорганічних сполук» Учитель хімії Верхівцевського НВК Кукса Наталія Миколаї
Урок у 8 класі на тему: «Класифікація неорганічних сполук» Учитель хімії Верхівцевського НВК Кукса Наталія Миколаї Воздух. Состав воздуха. Реакция горения
Воздух. Состав воздуха. Реакция горения Взаимосвязь неорганических веществ
Взаимосвязь неорганических веществ Волокна підготував учень 11 класу :
Волокна підготував учень 11 класу :  Железо и его соединения
Железо и его соединения Коэффициент концентрации меди
Коэффициент концентрации меди Карбонат натрия
Карбонат натрия Гетерофункционалды органикалық қосылыстар
Гетерофункционалды органикалық қосылыстар Структура и текстура магматических пород
Структура и текстура магматических пород Electron Structure
Electron Structure Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би
Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би Альдегиды. Кетоны
Альдегиды. Кетоны Свойство воды, устранение жесткости воды и очистка воды
Свойство воды, устранение жесткости воды и очистка воды Сурьма, Sb
Сурьма, Sb