Содержание
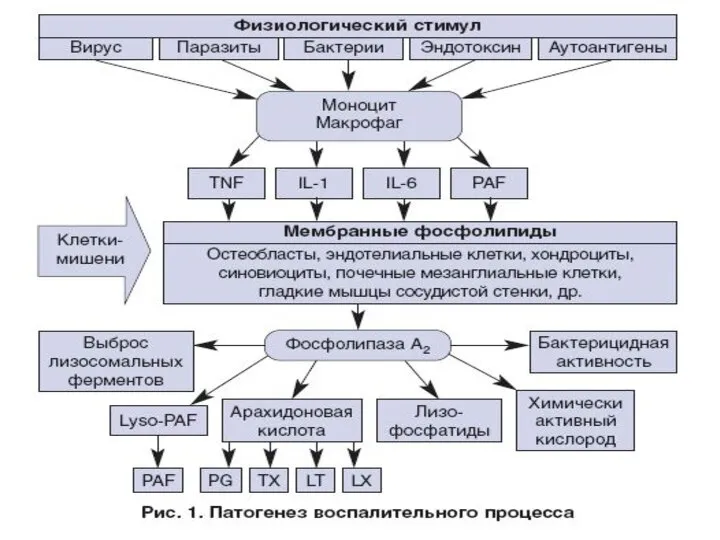
- 2. ФАЗЫ ВОСПАЛЕНИЯ 1. Острое воспаление – первоначальный ответ на поврежд. тканей (опосредован выделением гистамина, серотонина, брадикинина,
- 3. Эффекты медиаторов острого воспаления 1. Гистамин – вазодилат, сосуд. проницаемость 2. Серотонин – сосуд. проницаемость 3.
- 4. Эффекы медиаторов хронического воспаления ИЛ-1,2,3 (макрофаги Т-лимфоциты) – активация лимфоцитов, продукция ПГ; TNF (макрофаги) – продукция
- 6. Классификация НПВС С преимущественным действием на острую фазу воспаления (эксудативн., альтеративная) 1. Пр-ные салициловой кислоты -
- 7. Классификация НПВС 4. Пр-ные фенилалкановых кислот- ацеклофенак, диклофенак натрия, ибупрофен, кетопрофен 5. Оксикамы – пироксикам, мелоксикам,
- 8. Базисные противовоспалительные ср-ва, включены в стандарт медицинской помощи больным ревматическими заболеваниями 1. Иммунодепрессанты + цитостатические ср-ва:
- 9. Базисные ПВС, для лечения ревматических заболеваний (продолжение) б. Блокатор рецепторов ИЛ-6: - тоцилизумаб (актемира) Блокатор рецепторов
- 11. Базисные противовоспалительные ср-ва (вспомогательные) Производные 4-аминохинолина (хлорохин, гидроксихлорохин) Препараты золота (кризанол, ауранофин) Производные D-пеницилл- амина (пеницилламин,
- 12. Торможение молекул клеточной адгезии подавляют экспрессию молекул адгезии-1, селектинов в эндотелии сосудов Подавляют экспрессию молекул адгезии
- 13. Антагонизм НПВС с медиаторами воспаления Ингибируют ферменты участвующие в синтезе гистамина, серотонина, брадикинина, простагландинов. Повышают содержание
- 14. Антагонизм НПВС с медиаторами воспаления Подавляют дегрануляцию тучных клеток и выход из них БАВ (салицилаты, бутадион,
- 16. Индексы ингибирования ЦОГ-1/ЦОГ-2 Индометацин - 30 Диклофенак Na - 2,2 Мелоксикам - 0,33 Нимесулид - 0,2
- 17. Стабилизация лизосом. мембран и антиоксидантный (АО) эффект НПВС Тормозят выход лизосом. гидролаз (протеаз, липаз, фосфатаз), вызывающ.
- 18. Торможение энергопродукции в очаге воспаления Биохимические реакции, лежащие в основе воспаления – высоко энергозатратны: синтез медиаторов
- 19. Влияние НПВС на процессы пролиферации НПВС тормозят формирование соединительной ткани (синтез коллагена): Снижают активность фибробластов Нарушают
- 20. Иммунотропное действие НПВС Подавляют активацию фактора транскрипции (NF-kB) в Т-лимфоцитах Ингибируют синтез цитокинов (ИЛ-1,6,8, интерферон-β, ФНО-α),
- 21. Механизм обезболивающего действия Снижают гипералгезию в результате: блокады синтеза ПГ и простациклина, которые потенцируют раздражающ. дей-е
- 22. Механизм обезболивающего действия (продолжение) Уменьшают поток болевых импульсов из зоны воспаления в ЦНС Ингибируют ЦОГ-2 и
- 23. По мере убывания обезболивающего эффекта препараты располагаются: Кетопрофен, лорноксикам, мелоксикам, пироксикам, нимесулид ацеклофенак→напроксен, целекоксиб→индо- метацин →бутадион→анальгин→ибупрофен
- 24. Механизм формирования лихорадки В очаге воспаления в избытке образуются индукторы ЦОГ-2 (ИЛ-1,6, ФНО-α, интерфероны α и
- 25. Жаропонижающее действие НПВС В очаге воспаления блокируют ЦОГ-2 Угнетают синтез ПГЕ2 - его содержание в тепловом
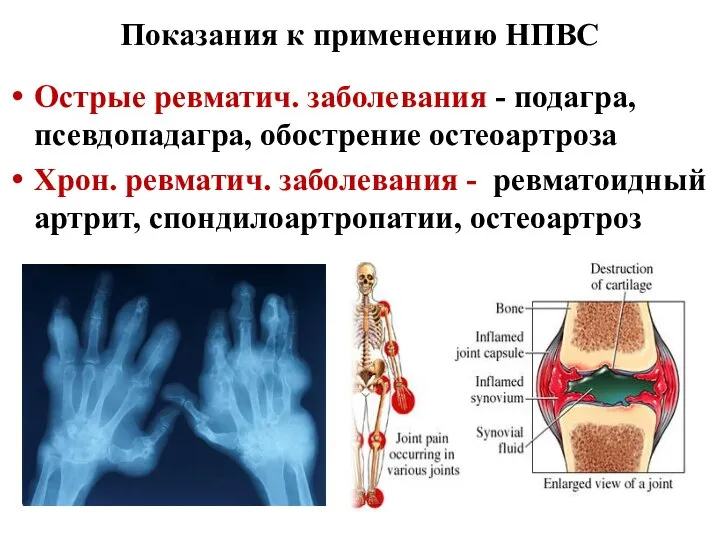
- 26. Показания к применению НПВС Острые ревматич. заболевания - подагра, псевдопадагра, обострение остеоартроза Хрон. ревматич. заболевания -
- 27. Показания к применению НПВС (продолжение) Острые неревматич. заболевания - травмы, боли в спине, послеоперационная боль, почечная
- 28. Побочное действие НПВС Ульцерогенное действие обусловлено 2-мя механизмами 1. Местным повреждением клеток слизистой желудка в результате
- 29. Местное повреждение клеток слизистой желудка в результате накопления в цитоплазме НПВС Нарушают состав фосфолипидов, гликопро-теинов, гликолипидов
- 30. Системное истощение цитопротекторных ПГ Ингибирование ЦОГ-1 с последующим снижением синтеза ПГ и простациклина Снижение содержания ПГ
- 31. Системное истощение цитопротекторных ПГ (продолжение) снижение кровотока и регенераторного потенциала тканей снижение секреции бикарбонатов и гликозаминогликанов
- 32. Ульцерогенное действие Сильное ульцерогенное д-е Кеторолак, пирокси- кам, лорноксикам, индометацин, бутади- он, к-та ацетилсали- циловая (аспириновая
- 33. Рекомендации по ведению больных с поражением ЖКТ НПВС Симптоматические побочные эфекты →антагонисты Н2 рецепторов (ранитидин); или
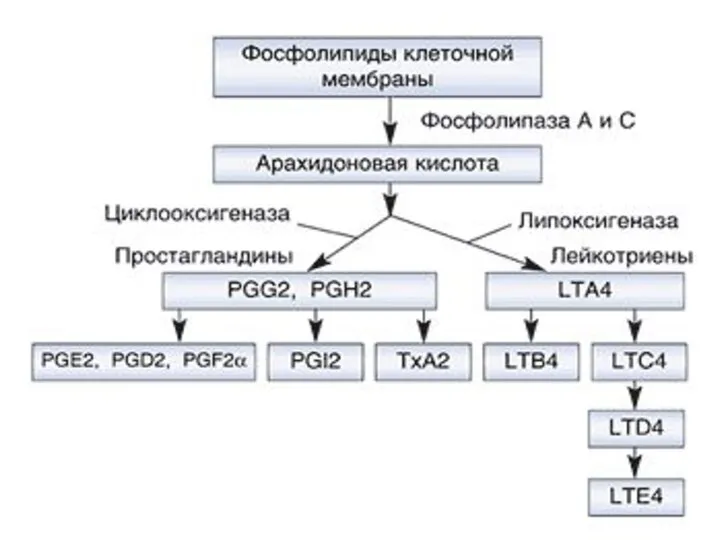
- 34. Аспирин-индуцированное респираторное заболевание (аспириновая астма) Патогенез аспириновой астмы связан с переключением метаболизма арахидоновой кислоты с ЦОГ-
- 35. Энцефалопатия + жировая дистрофия печени (синдром Рейе) На фоне вирусных инфекций прием АСК может вызвать синдром
- 36. Медленно действующие БПВ средства Производные 4-аминохинолина (хлорохин, гидроксихлорохин) Фармакодинамика – 1. блокируют синтез ДНК и РНК
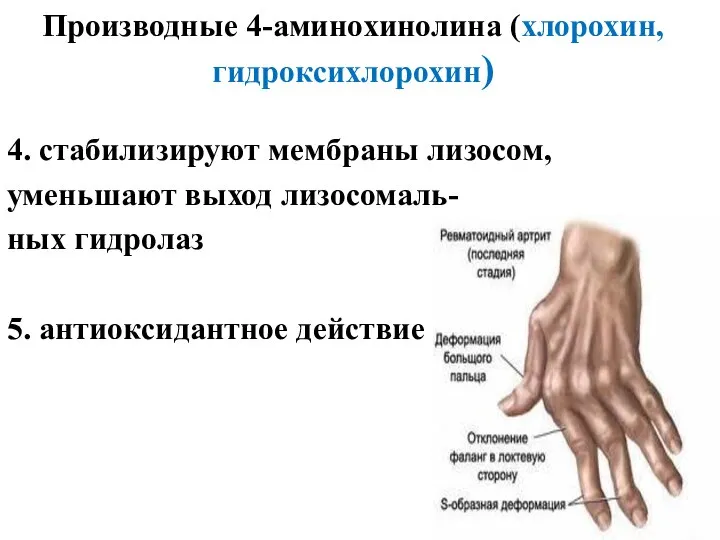
- 37. Производные 4-аминохинолина (хлорохин, гидроксихлорохин) 4. стабилизируют мембраны лизосом, уменьшают выход лизосомаль- ных гидролаз 5. антиоксидантное действие
- 38. Пенициламин (купренил) Фармакодинамика – 1. ингибирует активность металоферментов (супероксиддисмутазы, снижает содержание в тканях АФК); 2. Хелатирует
- 39. Пенициламин (купренил) продолжение 3. Угнетает Т- хелперную активность лимфоцитов, снижает хемотаксис нейтрофилов 4. Угнетает синтез коллагена
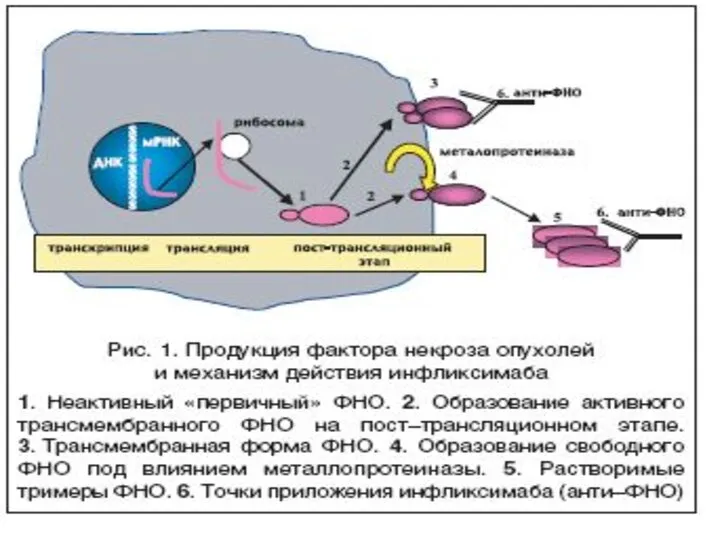
- 40. Базисные противовоспалительные ср-ва (Генно-инженерно-биологические препараты) Химерные моноклональные антитела – блокаторы ФНО - альфа - инфликсимаб (ремикейд)
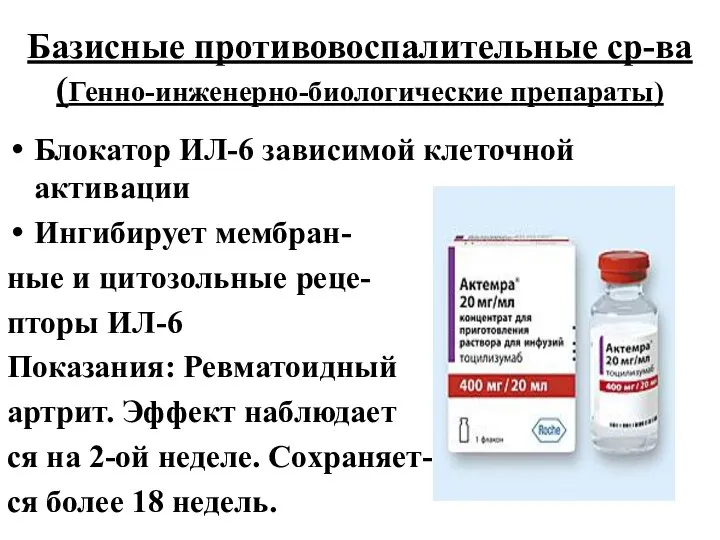
- 44. Базисные противовоспалительные ср-ва (Генно-инженерно-биологические препараты) Блокатор ИЛ-6 зависимой клеточной активации Ингибирует мембран- ные и цитозольные реце-
- 45. Базисные противовоспалительные ср-ва (Генно-инженерно-биологические препараты) Ингибитор В-клеточного звена иммунитета - Ритуксимаб (мабтера) Химерные моноклональные антитела к
- 47. Медленно действующие противовоспалительные ср-ва ЛЕФЛУНОМИД (АРАВА) – оказывает выраженное антипролиферативное, иммуно- супрессивное, противовоспа- лительное действие. Механизм
- 48. Механизм антипролиферативного действия: ЛЕФЛУНОМИДА (продолжение) 2. Ограничивает пролиферацию Т-лимфоцитов на стадии G1 клеточного цикла в результате
- 49. Механизм антипролиферативного действия: ЛЕФЛУНОМИДА (продолжение) 4. Тормозит экспрессию рецепторов к ИЛ-2 и ядерных антигенов ( маркеров
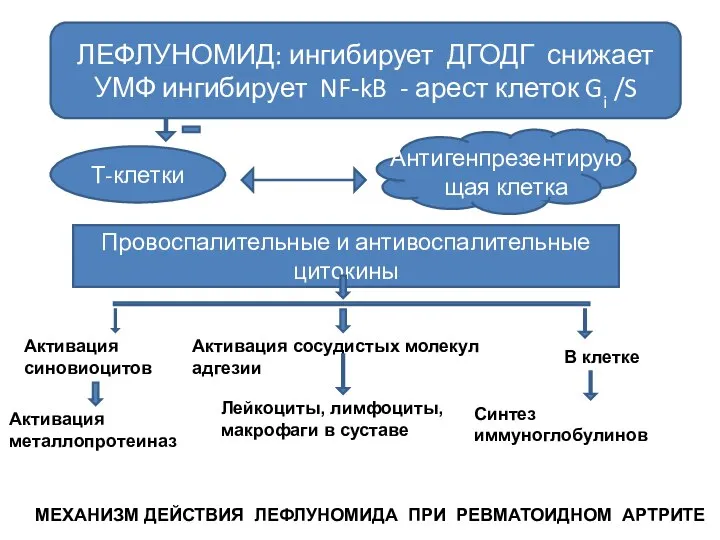
- 50. ЛЕФЛУНОМИД: ингибирует ДГОДГ снижает УМФ ингибирует NF-kB - арест клеток Gi /S Т-клетки Антигенпрезентирующая клетка Провоспалительные
- 51. Фармакокинетика Лефлуномида Лефлуномид (арава) пролекарство – в результате метаболизма в печени и стенке кишечника образуется активный
- 52. Базисный противоревматический препарат Лефлуномид (арава) Показания к применению: лечение активной фор- мы ревматоидного артрита, для уменьшения
- 54. Скачать презентацию










































 Друзья и соратники Д.И.Менделеева в сфере науки и культуры.
Друзья и соратники Д.И.Менделеева в сфере науки и культуры. Непредельные углеводороды алкены
Непредельные углеводороды алкены Презентация ОБЩАЯ ЖЕСТКОСТЬ ВОДЫ
Презентация ОБЩАЯ ЖЕСТКОСТЬ ВОДЫ  Зарождение научной химии в России в XVI XVIII веках. История и методология химии. Лекция 9
Зарождение научной химии в России в XVI XVIII веках. История и методология химии. Лекция 9 Влияние оксида азота на структуру и функцию собственной пластинки десны при экспериментальном гастродуодените
Влияние оксида азота на структуру и функцию собственной пластинки десны при экспериментальном гастродуодените Полиуретаны. Структура и строение
Полиуретаны. Структура и строение Общая характеристика элементов VIA-группы (халькогены). Сера. Кислород
Общая характеристика элементов VIA-группы (халькогены). Сера. Кислород Методы исследования и характеризации поверхностей. Поверхностное и межфазное натяжение. Тензиометрия и эллипсометрия
Методы исследования и характеризации поверхностей. Поверхностное и межфазное натяжение. Тензиометрия и эллипсометрия Підготував: учень 10-Б Резніков Дмитрій
Підготував: учень 10-Б Резніков Дмитрій  Урок по химии в 10 классе: «Углерод и кремний – р-элементы IVA-группы» подготовил учитель химии и биологии ГУО СШ №163 г.Минска Ко
Урок по химии в 10 классе: «Углерод и кремний – р-элементы IVA-группы» подготовил учитель химии и биологии ГУО СШ №163 г.Минска Ко Качественный химический анализ воды на определение металлов
Качественный химический анализ воды на определение металлов Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Основные классы неорганических соединений
Основные классы неорганических соединений АБС-пластик. Свойства
АБС-пластик. Свойства Природный газ
Природный газ Ферменты строение и свойства. Регуляция активности ферментов. (Лекция 1.3)
Ферменты строение и свойства. Регуляция активности ферментов. (Лекция 1.3) Презентация по Химии "ХІМІЯ ТАЇЖА" - скачать смотреть бесплатно
Презентация по Химии "ХІМІЯ ТАЇЖА" - скачать смотреть бесплатно Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Средства бытовой химиии
Средства бытовой химиии Растворы. рН среды. Вспомогательные вещества. Химические вещества и материалы в индустрии красоты. Лекция 7
Растворы. рН среды. Вспомогательные вещества. Химические вещества и материалы в индустрии красоты. Лекция 7 Хлор
Хлор Аминдердің химиялық қасиеттері
Аминдердің химиялық қасиеттері Диаграмма состояния Fe - FeC. Лекция 5 - 6
Диаграмма состояния Fe - FeC. Лекция 5 - 6 23 и 24 задание (ОГЭ-химия)
23 и 24 задание (ОГЭ-химия) Срез знаний по химии
Срез знаний по химии Термодинамика химических процессов
Термодинамика химических процессов Твердые тела и их свойства
Твердые тела и их свойства  Алюміній
Алюміній