Содержание
- 2. Основные классы неорганических соединений ОКСИДЫ ОСНОВАНИЯ КИСЛОТЫ СОЛИ
- 5. Классификация оснований ОСНОВАНИЯ Одноосновные NaОН, LiОН, NН4ОН Двухосновные Са(ОН)2 Трехосновные Fe(ОН)3 Растворимые, или щелочи LiОН, NаОН,
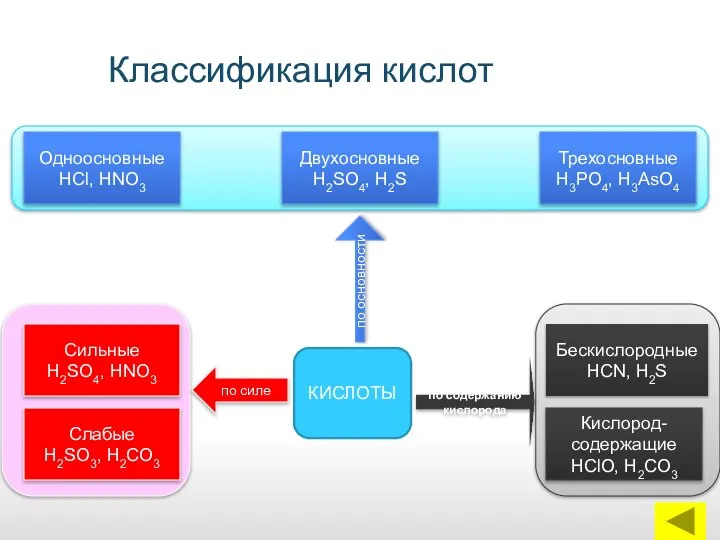
- 6. Классификация кислот КИСЛОТЫ Одноосновные НСl, НNО3 Сильные Н2SO4, НNО3 Слабые Н2SО3, Н2СО3 Кислород-содержащие НСlО, Н2СО3 Бескислородные
- 7. Классификация солей по составу СОЛИ Кислые NaHCO3 Смешанные CaClBr Двойные KNaSO4 Средние BaSO4 Основные Al(OH)2Cl Комплексные
- 9. ПОЛУЧЕНИЕ ОСНОВАНИЙ Взаимодействие активных металлов с водой Me + Н2O = МеОН + Н2 Взаимодействие оксидов
- 10. ПОЛУЧЕНИЕ КИСЛОТ Взаимодействие кислотных оксидов с водой неMeО + Н2O = P2O5 + H2O = H3PO4
- 11. ПОЛУЧЕНИЕ СОЛЕЙ Взаимодействием: Металла с неметаллом Са + Сl2 = СаСl Основного оксида с кислотным оксидом
- 12. Химические свойства основных оксидов 1.Основный оксид + кислота соль + вода 2.Основный оксид + кислотный оксид
- 13. Химические свойства кислотных оксидов 1.Кислотный оксид + основание соль + вода 2.Кислотный оксид+ основный оксид соль
- 14. Химические свойства амфотерных оксидов 1.Взаимодействуют с сильными кислотами ZnO + 2HCl ZnCl2 + H2O Основный оксид
- 15. Кислота Основания Растворимая соль Кислотный оксид Соль + Вода Соль + Нерастворимое основание Соль + Вода
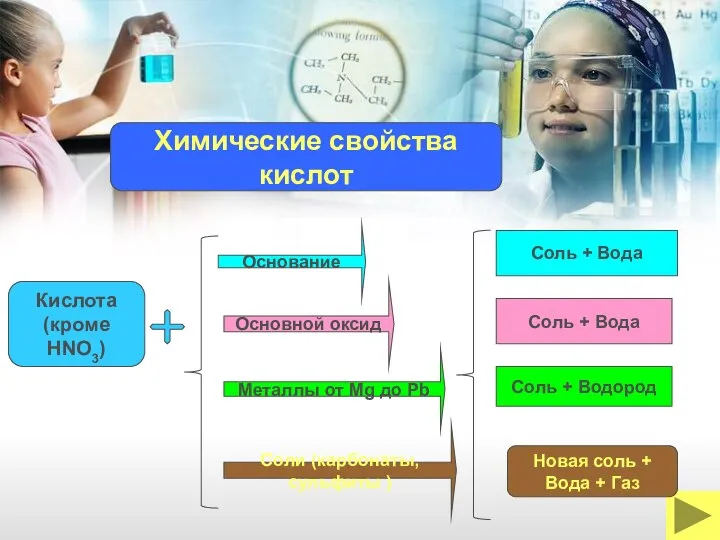
- 16. Основание Кислота (кроме HNO3) Металлы от Mg до Pb Основной оксид Соль + Вода Соль +
- 17. ТБ при работе с кислотами Запомни правило: «Сначала вода, потом кислота, иначе произойдет ужасное». Если же
- 19. Щелочь Соль Кислота Металл Новая соль + Нерастворимое основание Новая соль + Вода + Газ Новая
- 20. Применение оксидов Известно около 300 оксидов. Из железных руд, содержащих оксиды железа, получают железо. Песок, состоящий
- 25. Скачать презентацию



















 Гидрокрекинг нефтяного сырья
Гидрокрекинг нефтяного сырья Презентация Алкины Ацетилен
Презентация Алкины Ацетилен Застосування вуглеводів. Їх біологічна роль
Застосування вуглеводів. Їх біологічна роль Аммиак NH3
Аммиак NH3 Лаборатория мирового уровня в области термического анализа и физико-химии процессов тепловых методов добычи
Лаборатория мирового уровня в области термического анализа и физико-химии процессов тепловых методов добычи Классическая теория гармонического кристалла. Гармоническое приближение. Адиабатическое приближение
Классическая теория гармонического кристалла. Гармоническое приближение. Адиабатическое приближение Великий Ломоносов Работу выполнила учитель химии МБОУ «СОШ №27 с углубленным изучением отдельных предметов» Карташова Л.А.
Великий Ломоносов Работу выполнила учитель химии МБОУ «СОШ №27 с углубленным изучением отдельных предметов» Карташова Л.А. Вакуумная перегонка мазута
Вакуумная перегонка мазута Подгруппа селена
Подгруппа селена Электрические свойства дисперсных систем. (Лекция 5)
Электрические свойства дисперсных систем. (Лекция 5) Автомобильные бензины и дизельное топливо
Автомобильные бензины и дизельное топливо Обобщающее повторение по теме Неметаллы. Урок №7
Обобщающее повторение по теме Неметаллы. Урок №7 Полярография және оның фармацияда қолданылуы
Полярография және оның фармацияда қолданылуы Эмульсиялардың тұрақтылығына полиэтиленгликоль-баз композицияларының әсері
Эмульсиялардың тұрақтылығына полиэтиленгликоль-баз композицияларының әсері Полімери
Полімери  Тест- тренажер по теме: Основные классы неорганических веществ «Оксиды»
Тест- тренажер по теме: Основные классы неорганических веществ «Оксиды» Периодическая Система Д. И. Менделеева в свете учения о строении атома
Периодическая Система Д. И. Менделеева в свете учения о строении атома Счастливы вместе с химией
Счастливы вместе с химией Тема урока: Сложные эфиры.
Тема урока: Сложные эфиры. Применение s-, p-, d- элементов в медицине
Применение s-, p-, d- элементов в медицине Валентність
Валентність  Реологические свойства полимерных материалов
Реологические свойства полимерных материалов Кислородосодержащие органические соединения (2 часть) Муравьева Н.А. – учитель химии МОУ «Арбузовская сош»
Кислородосодержащие органические соединения (2 часть) Муравьева Н.А. – учитель химии МОУ «Арбузовская сош»  «Химия и цвет» Интегрированный урок по изобразительному искусству и химии Запольская О.А. Учитель МКОУ СОШ №1 п.Сосьва
«Химия и цвет» Интегрированный урок по изобразительному искусству и химии Запольская О.А. Учитель МКОУ СОШ №1 п.Сосьва Микрофлора и биохимические реакции подземных вод
Микрофлора и биохимические реакции подземных вод Номенклатура органических соединений
Номенклатура органических соединений Силікон Корєшкова А. В. 11-М
Силікон Корєшкова А. В. 11-М  Становление органической химии как отдельной науки. (Модуль 1)
Становление органической химии как отдельной науки. (Модуль 1)