Содержание
- 2. +6С )2)4 +14Si )2)8)4 +32Ge )2)8)18)4 +50Sn )2)8)18)18)4 +82Pb )2)8)18)32)18)4 S2 P2 Р - элементы Общая
- 3. Изменение свойств в группе С Si Ge Sn Pb Металлические свойства увеличиваются
- 4. Элементы IVА-группы Неметаллы Амфотерные элементы
- 5. Общая электронная формула: […] ns 2 (n–1)d 10np2 Валентные возможности: С: 2, 4; Si, Ge, Sn,
- 6. Оксиды элементов IVА-группы +IV CO2(г) уст. SiO2(т) уст. GeO2(т) уст. SnO2(т) уст. PbO2(т) с.окисл. +II CO
- 7. Водородные соединения элементов IVА-группы СH4 SiH4 GeH4 SnH4 PbH4 неуст. Склонность к катенации (образование цепей состава
- 8. Простые вещества Аллотропия Углерод: алмаз (sp3), графит (sp2), карбин (sp), фуллерен. Олово «белое» и «серое». Структура
- 9. Химические свойства При комн. темп. С, Si, Ge + H2O ≠ Sn, Pb + H2O ≠
- 10. Химические свойства С(т) + KOH ≠ Si + 4NaOH = Na4SiO4 + 2H2↑
- 11. Распространение в природе и важнейшие минералы 2. Si 25,80% (27,72% в литосфере) 13. C 0,087% (0,032%
- 12. Углерод: графит, алмаз, каменный уголь, нефть, природный газ, орг. в-ва, карбонаты
- 13. Германий, олово и свинец
- 14. Шкала степеней окисления углерода CO2, CO32−, H2CO3, Na2CO3, CS2, CF4, CCl2O, C(NH2)2O CO, HCN, C2F4 C
- 15. Графит Т. пл. 3800 °С, т. кип. 4000 °С, плотность 2,27 г/см3, электропроводен, устойчив. Типичный восст-ль
- 16. 0 Углерод
- 17. Аллотропные модификации углерода графит алмаз фуллерен
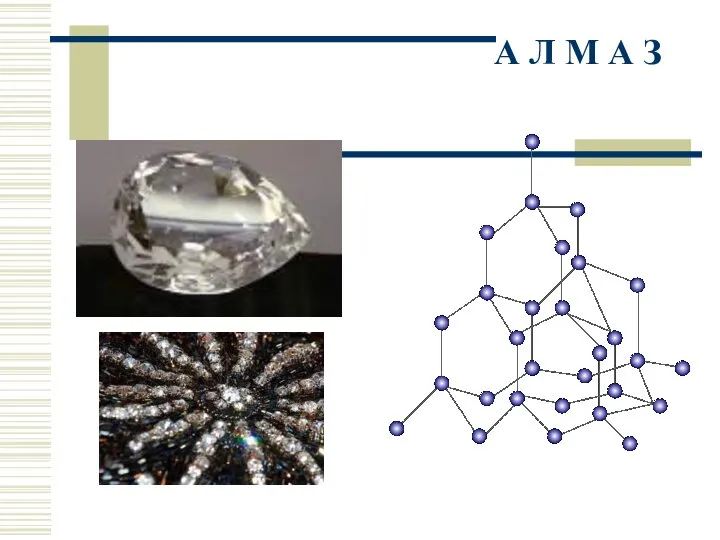
- 18. А Л М А З
- 19. Звезда ордена Св. Андрея Первозванного Алмаз «Шах» Скипетр императорский
- 20. Большая императорская корона Малая императорская корона
- 21. Г Р А Ф И Т Применение графита: Электроды для электролиза Облицовка сопел ракетных двигателей Смазка
- 22. П О Ч Е М У А Л М А З - очень твердый, Г Р
- 23. Угольные фильтры В бытовых фильтрах, в промышленном производстве, на очистных сооружениях – уголь поглощает вредные вещества
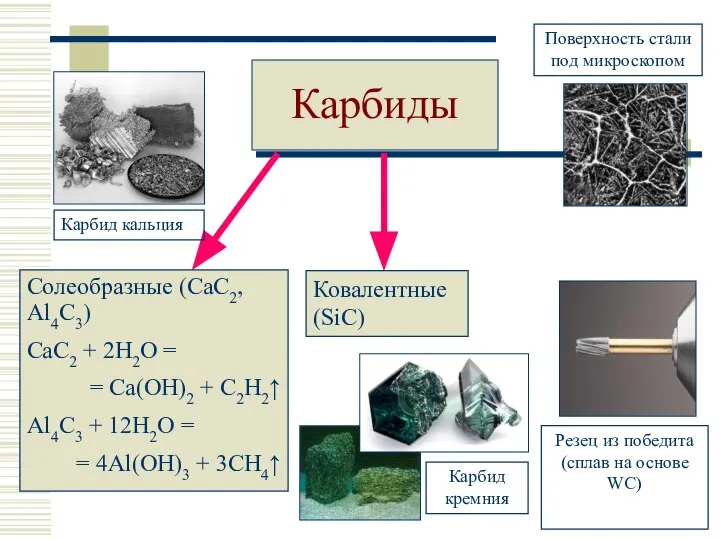
- 24. Карбиды
- 25. Водородные соединения. Метан CH4 СН4 – газ без цвета и запаха, горюч, главная сост. часть природного
- 26. Монооксид углерода CO – несолеобразующий оксид Бесцветный газ, без запаха, легче воздуха, малорастворим в воде, ядовит
- 27. Диоксид углерода CO2 (кислотный оксид) Бесцветный газ, без запаха, тяжелее воздуха, умеренно растворим в воде (при
- 28. Моногидрат CO2 . H2O и угольная кислота H2CO3 В водном растворе: CO2 (г) + H2O ⮀
- 29. Псевдогалогениды Циановодород HCN В водн. р-ре – слабая «синильная кислота»: HCN + H2O ⮀ CN– +
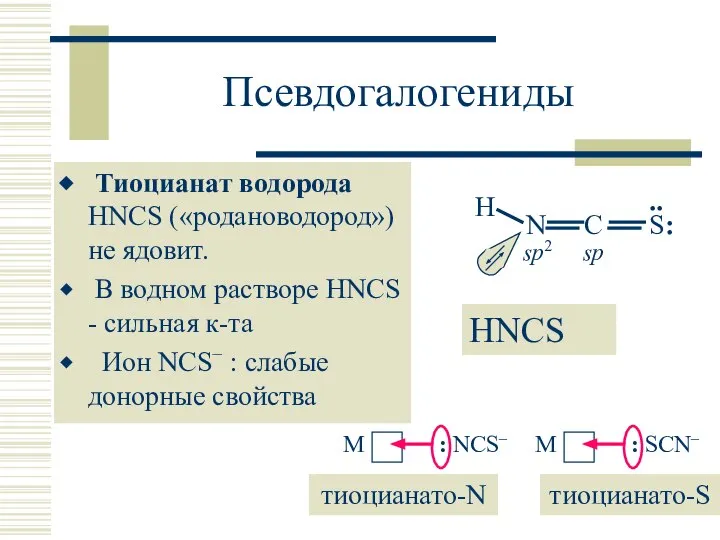
- 30. Псевдогалогениды Тиоцианат водорода HNCS («родановодород») не ядовит. В водном растворе HNCS - сильная к-та Ион NCS−
- 32. аллотропия КРЕМНИЯ Кристаллический кремний Аморфный кремний
- 33. Нахождение в природе SiO2 кремнезём (песок) Al2O3∙ 2SiO2∙2H2O каолинит (глина) По распространенности занимает второе место после
- 34. ПРИМЕНЕНИЕ КРЕМНИЯ Кремнистые стали Силиконовый каучук Фотоэлементы Силиконовый герметик
- 36. Получение кремния SiO2 + 2C = Si + 2CO SiO2 + 2Mg = 2MgO + Si
- 37. Водородные соединения SinH2n+2 (силаны) Моносилан SiH4: SiH4 + 2O2 = SiO2 + 2H2O Получение силанов: SiO2
- 38. СОЕДИНЕНИЯ КРЕМНИЯ ОКСИД КРЕМНИЯ SiO2 КРЕМНЕВАЯ КИСЛОТА H2SiO3 СОЛИ КРЕМНЕВОЙ КИСЛОТЫ СИЛИКАТЫ Si
- 39. ОКСИД КРЕМНИЯ - SiO2 песок горный хрусталь (кварц) аметист
- 40. Взаимодействие кремния с кислородом Si + O2 = SiO2
- 41. Кислородные соединения -SiO2 оксид кремния SiO2 + 2NaOH = Na2SiO3 + H2O (силикат натрия)
- 42. Травление стекла SiO2 + 6HF (изб.) = H2[SiF6] + 2H2O (гексафторосиликат водорода) Травление — в технике,
- 43. КРЕМНЕВАЯ КИСЛОТА H2SIO3 Na2SiO3 + 2HCl = 2NaCl + H2SiO3 ↓ кремневая кислота Получение: Кремниевая кислота
- 44. Получение кремниевой кислоты https://www.youtube.com/watch?v=hB6GOzNFEaA
- 46. Скачать презентацию



![Общая электронная формула: […] ns 2 (n–1)d 10np2 Валентные возможности: С:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396128/slide-4.jpg)

































![Травление стекла SiO2 + 6HF (изб.) = H2[SiF6] + 2H2O (гексафторосиликат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396128/slide-41.jpg)


 Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты
Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты Хром және оның қосылыстары
Хром және оның қосылыстары Металл и ржавчина: взаимодействие и способы защиты
Металл и ржавчина: взаимодействие и способы защиты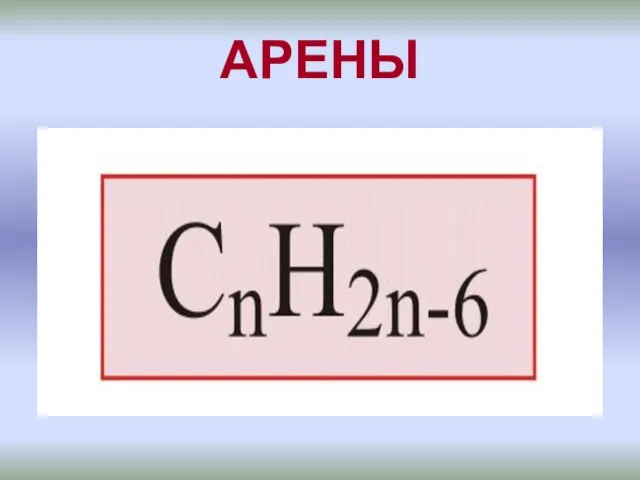 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Диссертация «Анализ и моделирование колебательно-вращательных спектров высокого разрешения молекулы двуокиси азота»
Диссертация «Анализ и моделирование колебательно-вращательных спектров высокого разрешения молекулы двуокиси азота» Отбор проб товаров для анализа. Химико-аналитический контроль
Отбор проб товаров для анализа. Химико-аналитический контроль Аттестационная работа. Задачи на смеси и сплавы
Аттестационная работа. Задачи на смеси и сплавы Способы получения полимеров (Лекция 3)
Способы получения полимеров (Лекция 3) Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений
Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений Сульфиды. Лекция 8
Сульфиды. Лекция 8 The alkali metals
The alkali metals Классификация химических реакций
Классификация химических реакций Оксиды углероды
Оксиды углероды Презентация по химии Применение кислорода
Презентация по химии Применение кислорода Дисперсные системы. Коллоидные растворы
Дисперсные системы. Коллоидные растворы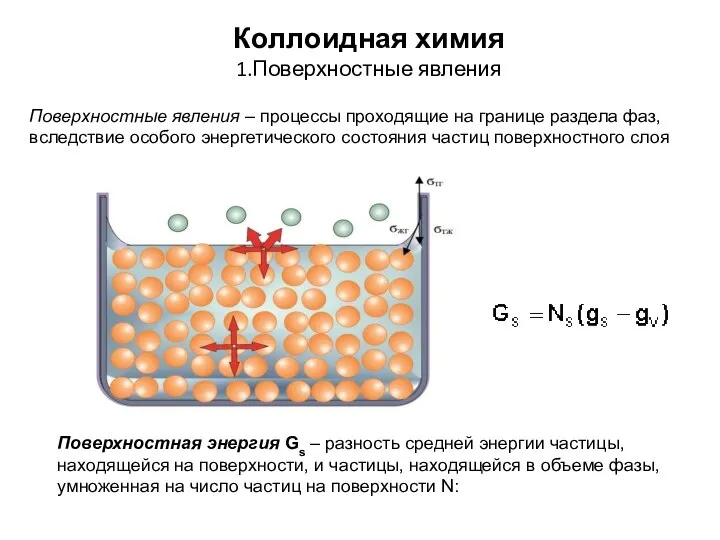 Коллоидная химия. Поверхностные явления
Коллоидная химия. Поверхностные явления Презентация по Химии "Степень окисления" - скачать смотреть
Презентация по Химии "Степень окисления" - скачать смотреть  Состав, строение, классификация кислот
Состав, строение, классификация кислот Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу
Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу Пральні порошки. Мила
Пральні порошки. Мила  Особенности строения, реакционной способности и методы синтеза галогенпроизводных углеводородов
Особенности строения, реакционной способности и методы синтеза галогенпроизводных углеводородов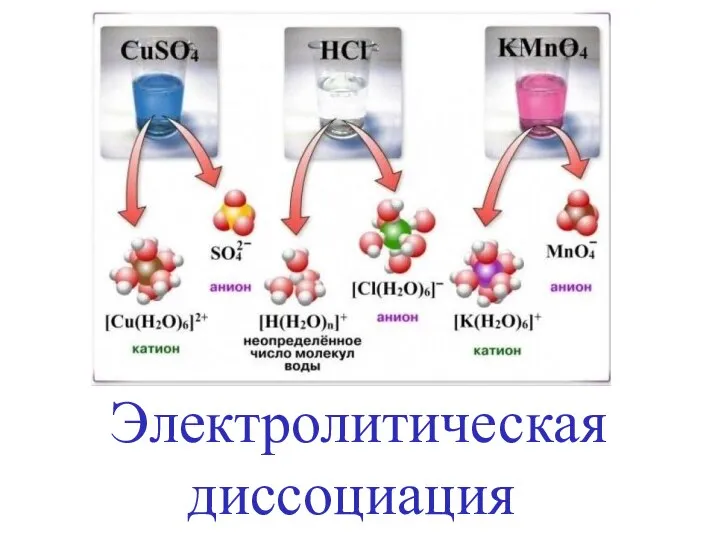 Электролитическая диссоциация
Электролитическая диссоциация Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Окислительно-восстановительные реакции с участием органических веществ
Окислительно-восстановительные реакции с участием органических веществ Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Елементи VІ групи головної підгрупи
Елементи VІ групи головної підгрупи Підготувала учениця 11-А класу Білецька Олеся
Підготувала учениця 11-А класу Білецька Олеся