Содержание
- 2. План лекции: 1. Общие вопросы аналитической химии. Литература по аналитической химии. 3. Химические методы обнаружения неорганических
- 3. Рекомендуемая литература
- 4. Новая литература
- 5. Определение предмета «Аналитическая химия»
- 6. Аналитическая химия, или аналитика – это раздел химической науки, разрабатывающий на основе фундаментальных законов химии и
- 7. Определение VIII Европейской конференции по аналитической химии (Эдинбург, 1993)- Аналитическая химия – это научная дисциплина, которая
- 8. Определение по Г.Кристиану со ссылкой на Чарльза Н.Рейли Аналитическая химия – это то, чем занимаются химики-
- 9. Аналитическая служба Административная система, обеспечивающая конкретный анализ определенных объектов с использованием методов, рекомендуемых аналитической химией, называется
- 10. Основные понятия аналитической химии: принцип, метод и методика анализа
- 11. Принцип анализа Явление, используемое для получения аналитической информации, называется принципом анализа. (Например, явление - поглощение света
- 12. Метод анализа Краткое изложение принципов, лежащих в основе анализа вещества (вне зависимости от определяемого компонента и
- 13. Методика анализа Методика анализа – это подробное описание хода выполнения конкретного анализа данного объекта с использованием
- 14. В зависимости от цели различают качественный, количественный и структурный анализ.
- 15. Качественный анализ Качественный анализ предполагает обнаружение или идентификацию компонентов анализируемого образца.
- 16. Количественный анализ В процессе количественного анализа происходит определение концентраций или масс компонентов.
- 17. Структурный анализ Цель структурного анализа – установление химического и пространственного строения исследуемого соединения.
- 18. Классификация видов анализа в зависимости от определяемого компонента
- 19. Классификация видов анализа в зависимости от массы или объема анализируемой пробы
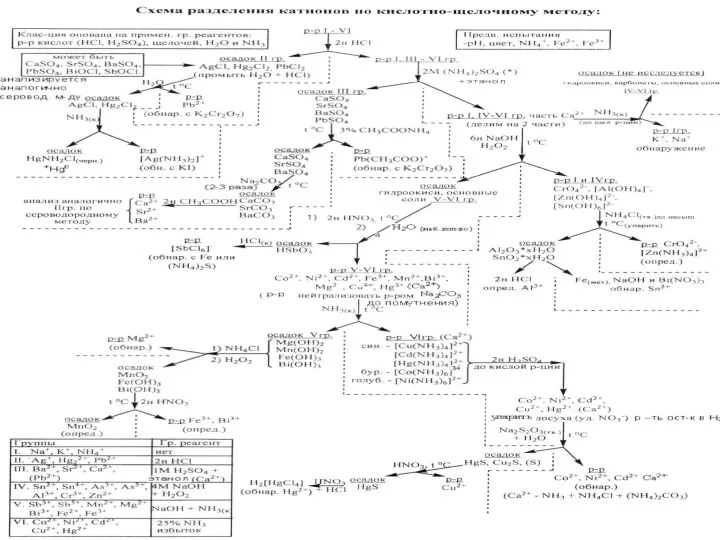
- 20. Классификация видов анализа в зависимости от процедуры проведения анализа Систематический –разделение смеси ионов на группы или
- 21. Характеристики аналитической реакции Избирательность ( селективность) – возможность определения в результате аналитической реакции определенного вещества (одного
- 22. Избирательность аналитической реакции (в зависимости от числа веществ) Специфические реакции – позволяют определять только одно вещество;
- 23. Методы аналитической химии
- 24. Методы аналитической химии при анализе образцов 1. Метод пробоотбора; 2. Метод разложения проб; 3. Метод разделения
- 25. Химические методы обнаружения неорганических веществ.
- 26. Химические методы обнаружения неорганических веществ
- 27. Химические методы обнаружения неорганических веществ основаны на проведении аналитических реакций. Аналитическими называются химические реакции, результат которых
- 28. Эффекты при аналитических реакциях 1. Образование и растворение осадков 2. Образование характерных кристаллов 3. Появление или
- 29. Понятие аналитической группы ионов
- 30. Понятие аналитической группы ионов Аналитическая группа ионов отличается от групп Периодической таблицы Менделеева Д.И. Аналитическая группа
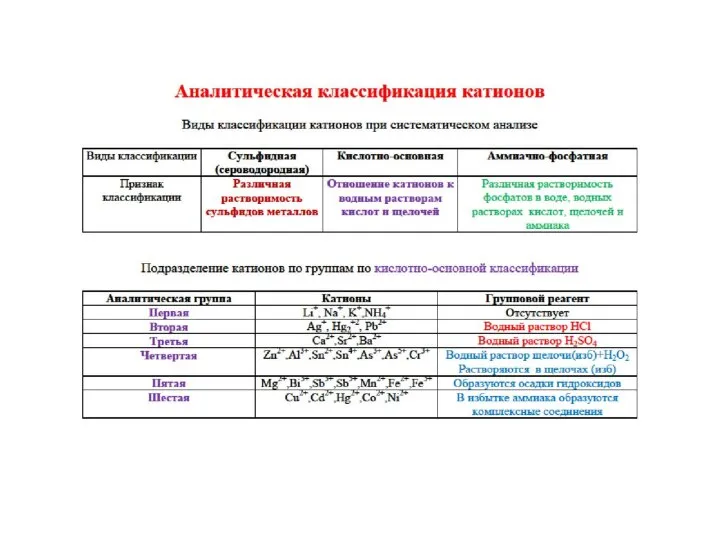
- 31. Аналитическая классификация катионов
- 35. Аналитическая классификация катионов Сульфидная; Кислотно-основная; Аммиачно-фосфатная;
- 36. Сульфидная Аналитическая классификация катионов Групповые реагенты – сульфид аммония, сероводород и карбонат аммония. Все катионы подразделяются
- 37. Кислотно-основная аналитическая классификация катионов Все катионы подразделяются на 6 аналитических групп. Используется различие в растворимости соединений
- 38. Аммиачно-фосфатная аналитическая классификация катионов В основу положена различная растворимость фосфатов в воде, водных растворах кислот, щелочей
- 39. Кислотно-основная классификация катионов
- 40. Первая аналитическая группа катионов -Li+, Na+, K+, NH4+
- 41. Реакции ионов Li+
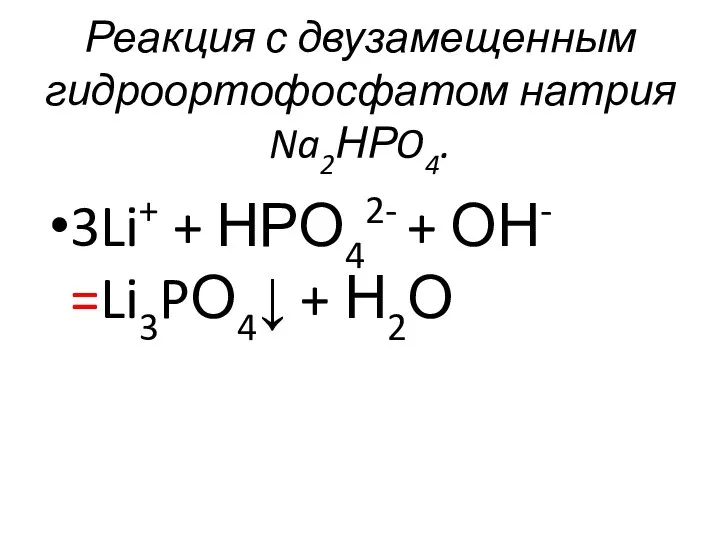
- 42. Реакция с двузамещенным гидроортофосфатом натрия Na2НРO4. 3Li+ + НРО42- + ОН- =Li3PО4↓ + Н2О
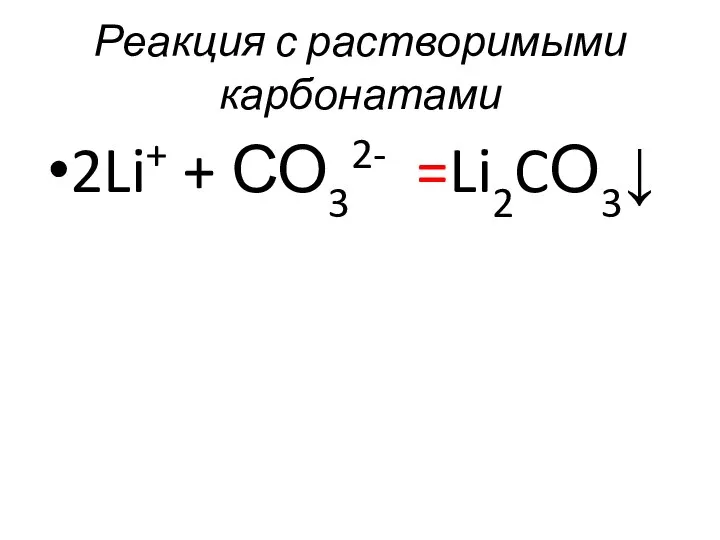
- 43. Реакция с растворимыми карбонатами 2Li+ + СО32- =Li2CО3↓
- 44. Реакция с растворимыми фторидами Li+ + F- = LiF↓
- 45. Реакции ионов Na+
- 46. Микрокристаллоскопическая реакция с цинкуранилацетатом (фармакопейная). Na+ + Zn[(UО2)3(CH3CОО)8] + СН3СОО- + 9Н2О =NaZn(UО2)3(CH3CОО)9∙9Н2О
- 47. .Реакция с гексагидроксостибатом (V) калия Na+ + [Sb(OH)6]- =Na[Sb(OH)6]↓
- 48. Реакции ионов K+
- 49. Реакция с гексанитрокобальтатом (III) натрия (фармакопейная) 2К+ + Na3[Co(NО2)6] = NaK2[Co(NО2)6↓ + 2Na+.
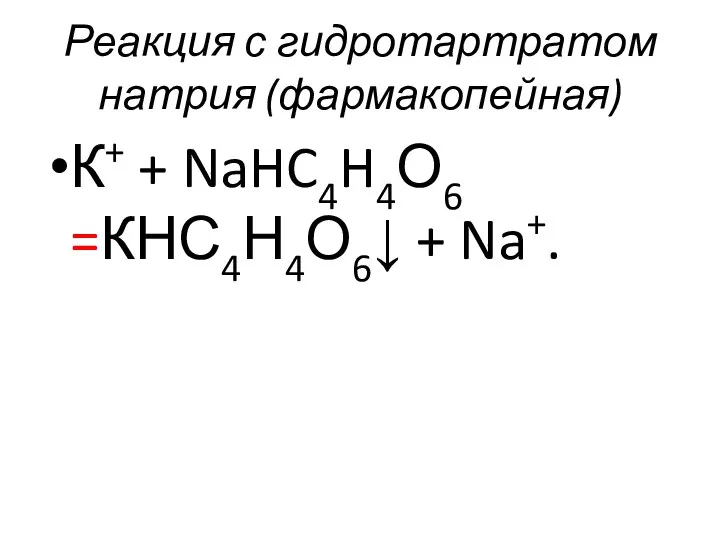
- 50. Реакция с гидротартратом натрия (фармакопейная) К+ + NaHC4H4О6 =КНС4Н4О6↓ + Na+.
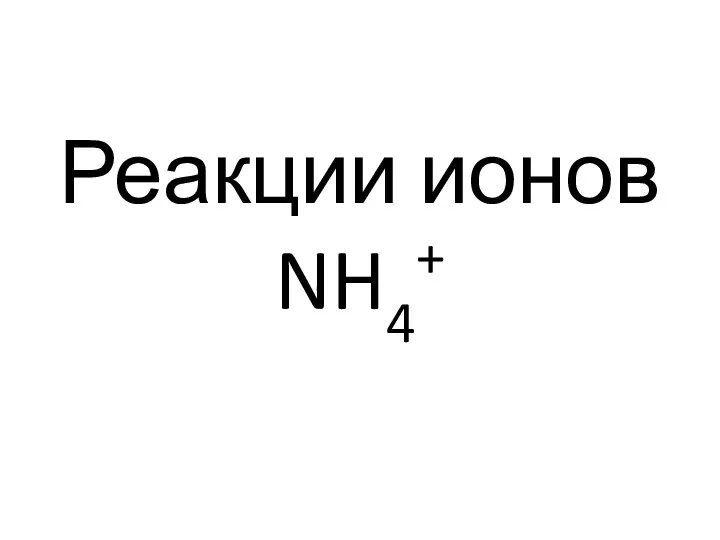
- 51. Реакции ионов NH4+
- 52. Реакция разложения солей аммония щелочами (фармакопейная) NH4+ + ОН- =NH3↑ + Н2О.
- 53. Реакция с реактивом Несслера — смесью раствора тетрайодомеркурama(II) калия K2[HgI4] с КОН (фармакопейная) NH4+ + 2[HgI4]2-
- 54. Анализ смеси катионов Li+, Na+, K+, NH4+ Сразу удаляют аммоний прокаливаем в щелочной среде, затем Li+–
- 55. Вторая аналитическая группа катионов -Ag+, Pb2+, Hg22+,
- 56. Реакции ионов Ag+
- 57. Реакция со щелочами 2Ag+ + 2ОН- Ag2O↓ + Н2О. Ag2O + 4NH3 + Н2О 2[Ag(NH3)2]+ +
- 58. Растворимые галогениды Ag+ + Сl- = AgCl↓; Ag+ + Br- = AgBr↓; Ag+ + I- =
- 59. Различие галогенидов серебра Осадок хлорида серебра растворим в растворе аммиака. Иодид серебра не растворяется в растворе
- 60. Хромат калия - осадок кирпично-красного цвета: 2Ag+ + CrО42- = Ag2CrО4↓
- 61. Гидроортофосфат натрия 3Ag+ + 2HPO42- = Ag3PO4↓ + H2PO4-
- 62. Реакция восстановления Ag+ до металлического серебра 4[Ag(NH3)2]OH + CH2O = 4Ag↓ + (NH4)2CO3 + 6NH3 +
- 63. Реакции ионов Pb2+
- 64. Действие щелочей и аммиака Pb2+ + 2OH- = Pb(OH)2 ↓
- 65. Растворимые галогениды Pb2+ +2Cl - = PbCl2 ↓ Pb2+ +2Br - = PbBr2 ↓ Pb2+ +2I
- 66. Осадки галогенидов свинца (II) растворимы в горячей воде и в присутствии избытка галогенид-ионов PbI2↓ + 2I-
- 67. Хромат калия образует желтый осадок Pb2+ + CrO42- = PbCrO4 ↓
- 68. Реакция с сульфид-ионами Pb2+ + S2- = PbS ↓
- 69. Реакции ионов Hg22+
- 70. Действие щелочей Hg2+ + 2OH- = Hg2O↓ + H2O
- 71. Водный раствор аммиака 2Hg22+ + 4NH3 + Н2О = [OHg2NH2]+ + 2Hg↓ + 3NH4+.
- 72. Растворимые хлориды Hg22+ + 2Сl- = Hg2Cl2↓.
- 73. Растворимые иодиды Hg22+ + 2I- = Hg2I2↓.
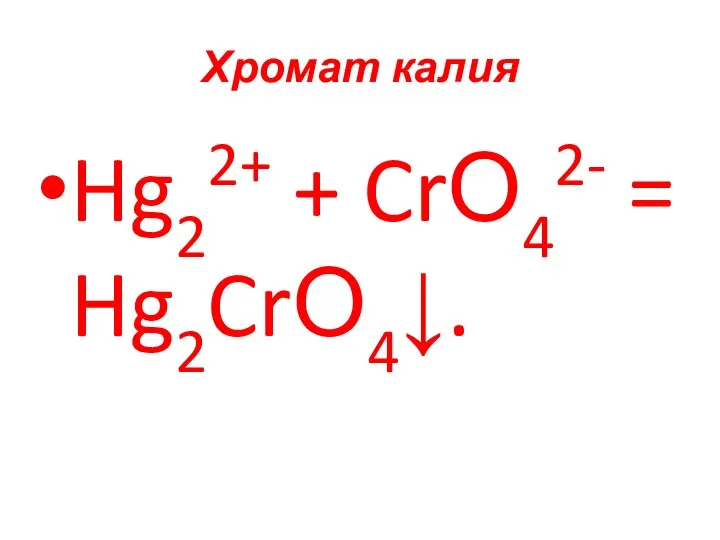
- 74. Хромат калия Hg22+ + CrО42- = Hg2CrО4↓.
- 75. Восстановление ртути (I) до металлической ртути. Hg22+ + Сu = 2Hg↓ + Сu2+.
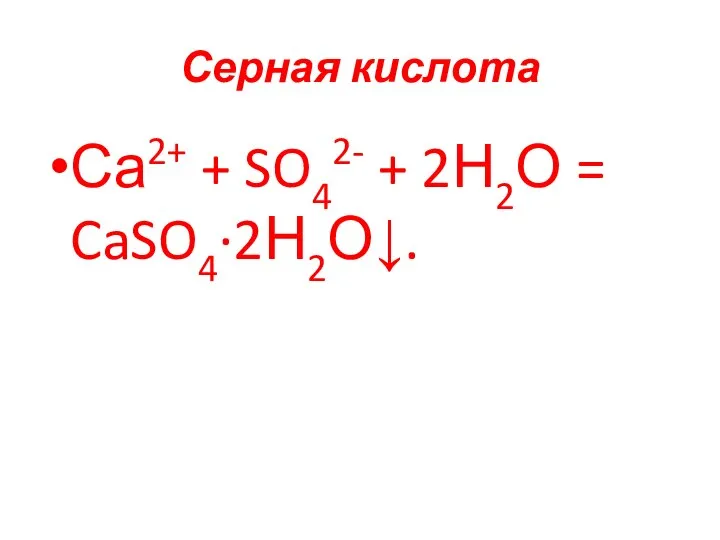
- 76. Серная кислота Са2+ + SO42- + 2Н2О = CaSO4∙2Н2О↓.
- 77. Третья аналитическая группа катионов -Ca2+ , Sr2+, Ba2+,
- 78. Реакции ионов Ca2+
- 79. Карбонат аммония Са2+ + СO32- = СаСO3↓.
- 80. Оксалат аммония Са2+ + С2O42- = СаС2О4↓
- 81. Гексацианоферрат (II) калия Са2+ + К+ + NH4++ [Fe(CN)6]4- = NH4KCa[Fe(CN)6]↓.
- 82. Реакции ионов Sr2+
- 83. Серная кислота, растворимые сульфаты и гипсовая вода (насыщенный водный раствор сульфата кальция) Sr2++ SO42- = SrSO4↓.
- 84. Карбонат аммония Sr2+ + СО32- = SrCO3↓.
- 85. Оксалат аммония Sr2+ + С2O42- = SrC2O4↓.
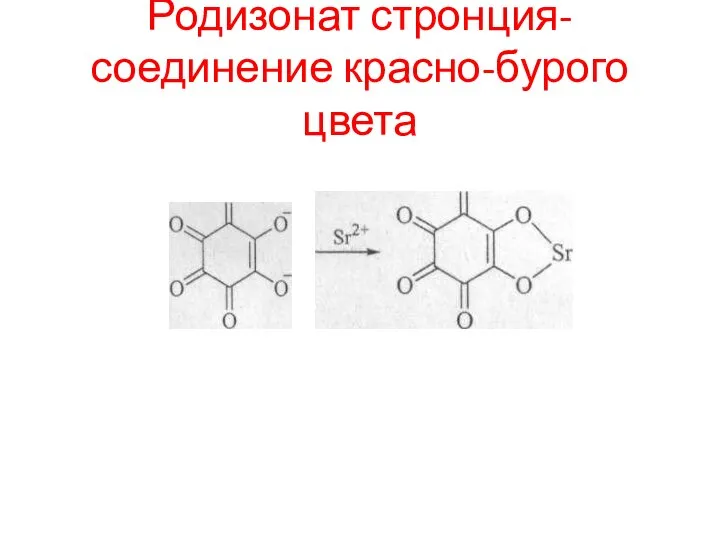
- 86. Родизонат стронция- соединение красно-бурого цвета
- 87. Реакции ионов Ba2+
- 88. Серная кислота и растворимые сульфаты Ва2+ + SO42- = BaSO4↓.
- 89. Карбонат аммония Ва2+ + СO32- = BaCO3↓.
- 90. Оксалат аммония Ва2+ + С2O42- = BaC2O4↓.
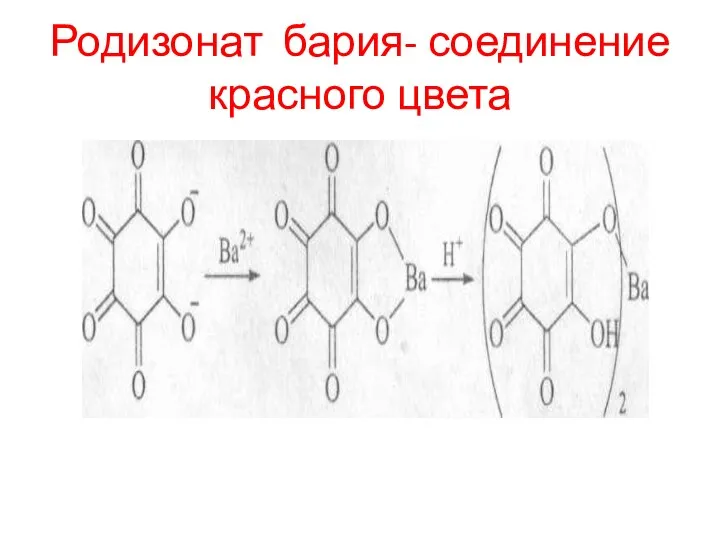
- 91. Родизонат бария- соединение красного цвета
- 92. Хромат или дихромат калия дают осадки ярко-желтого цвета Ва2+ + СгO42- = ВаСrO4↓; 2Ва2+ + Сг2O72-
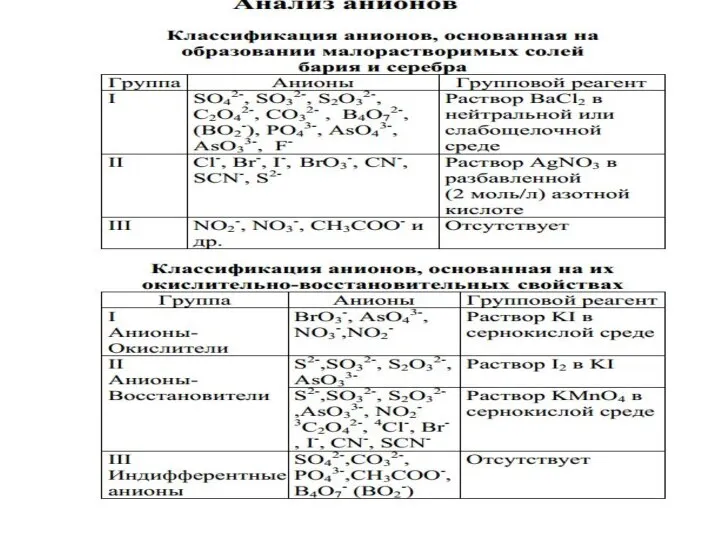
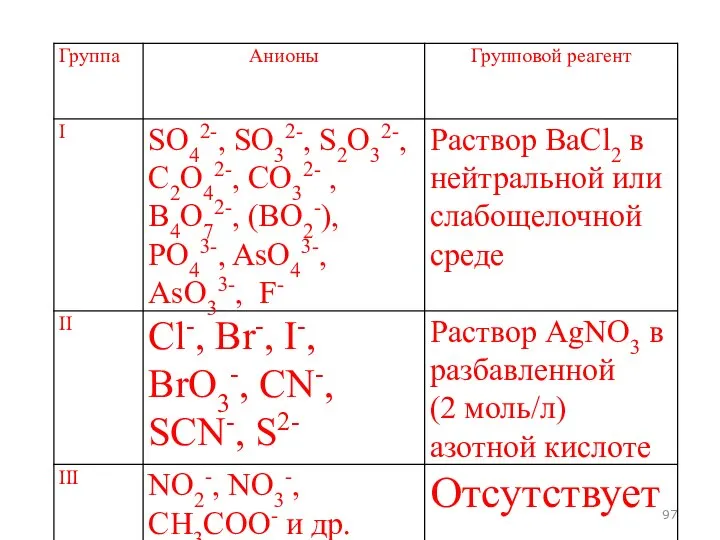
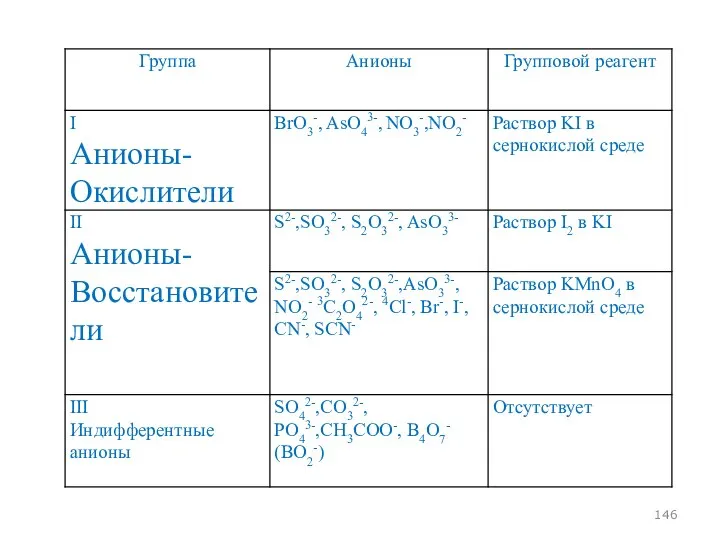
- 93. АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ АНИОНОВ
- 95. Главная цель групповых реакций Скрининг (отсеивание) анионов, которые не присутствуют в смеси.
- 96. Классификация анионов, основанная на образовании малорастворимых солей бария и серебра
- 98. Окраска бариевых солей Соли бесцветны, за исключением хроматов
- 99. ОВР - свойства SO32-, S2O32-, C2O42-, AsO33-, - восстановители AsO43-, CrO42- -окислители
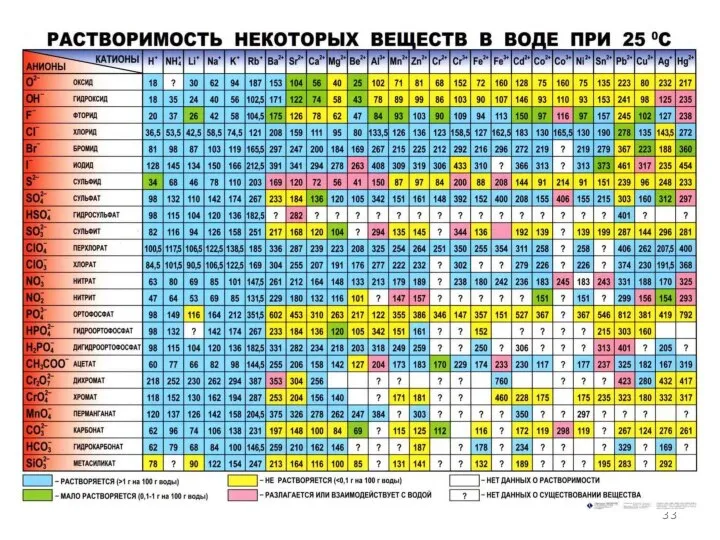
- 100. Растворимость в воде и минеральных кислотах BaSO4 – плохо растворим в воде и минеральных кислотах, BaCrO4
- 101. 1. СУЛЬФИТ-ИОНЫ Реакции анионов I аналитической группы
- 102. Реакции Сульфит-ионов Соли бария Соли серебра Разбавленные кислоты Окислители Восстановители Фуксин Нитропруссид натрия
- 103. Реакция с нитратом серебра Ag2SO3(белый осадок)+ Na2SO3 =2Na[Ag(SO3 ) 2]
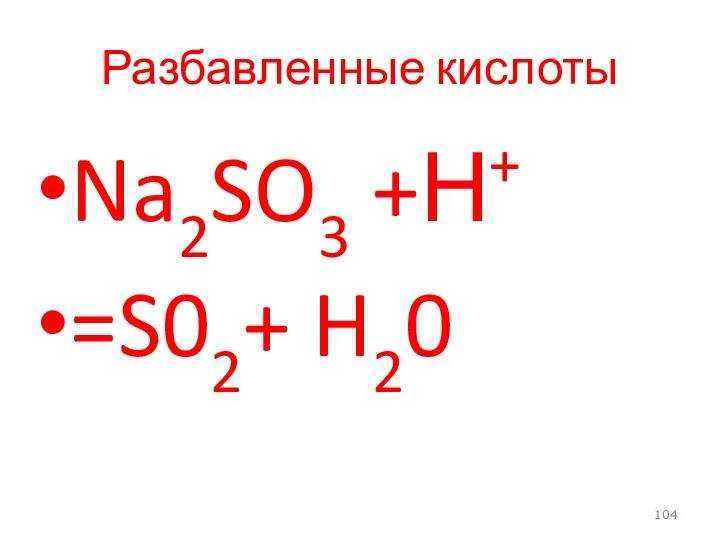
- 104. Разбавленные кислоты Na2SO3 +Н+ =S02+ H20
- 105. Реакции с окислителями
- 106. Реакции с восстановителями
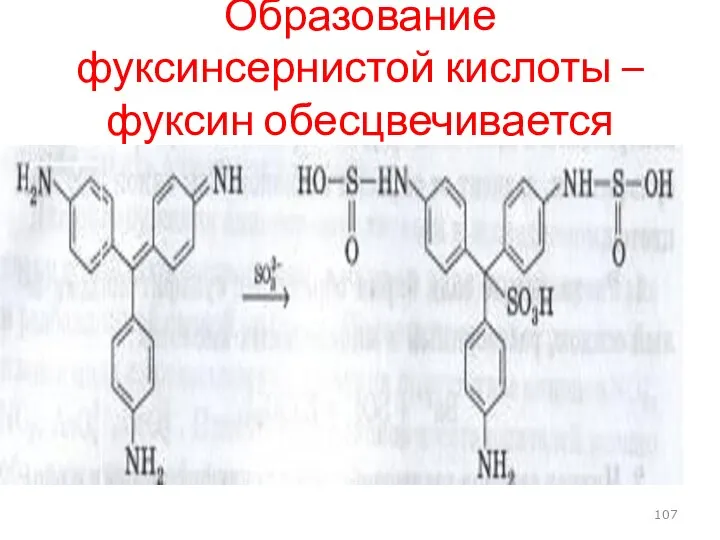
- 107. Образование фуксинсернистой кислоты – фуксин обесцвечивается
- 108. Нитропруссид натрия - Na2[Fe(CN)5NO] – КРАСНОЕ ОКРАШИВАНИЕ, состав продукта неизвестен
- 109. 2.ТИОСУЛЬФАТ-ИОНЫ Реакции анионов I аналитической группы
- 110. Реакции Тиосульфат--ионов Соли бария Соли серебра Разбавленные кислоты Окислители (KMnO4 в кислой среде) Восстановители (иод) Нитропруссид
- 111. Нитрат серебра Ag2S 2 O3(белый осадок)+ Na2S 2 O3 =2Na 3[Ag(S2O3)2]
- 112. Основная аналитическая реакция в фармхимии 2S2O32-+I2 =S4062-+2I-
- 113. 3.СУЛЬФАТ-ИОНЫ Реакции анионов I аналитической группы
- 114. Реакции сульфат--ионов Соли бария Соли свинца Родизонат бария
- 115. 4. КАРБОНАТ-ИОНЫ Реакции анионов I аналитической группы
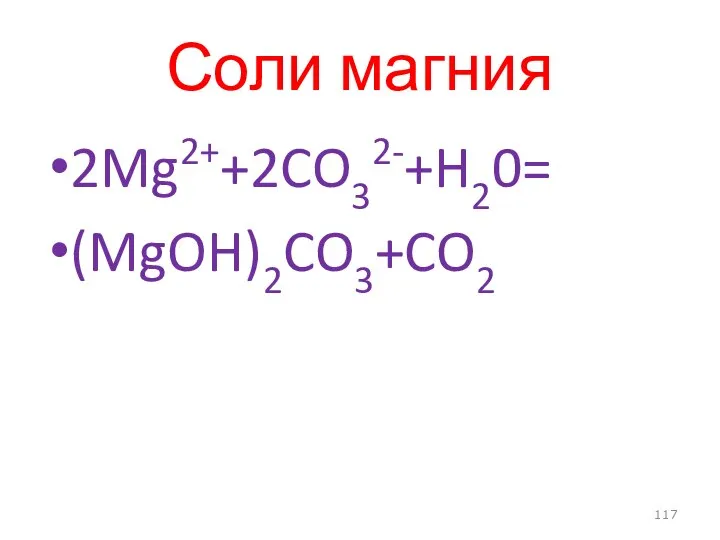
- 116. Реакции карбонат--ионов Соли бария Разбавленные кислоты Соли магния
- 117. Соли магния 2Mg2++2CO32-+H20= (MgOH)2CO3+CO2
- 118. 3. ОКСАЛАТ-ИОНЫ Реакции анионов I аналитической группы
- 119. Реакции оксалат--ионов Соли бария Соли кальция Окислители (KMnO4 в кислой среде)
- 120. Окислители (KMnO4 в кислой среде) 2MnO4-+5C2O42-+16H+=2Mn2++ 10CO2+8H2O
- 121. 5. БОРАТ-ИОНЫ Реакции анионов I аналитической группы
- 122. Реакции Борат-ионов С куркумином С хинализарином Этиловый эфир борной кислоты
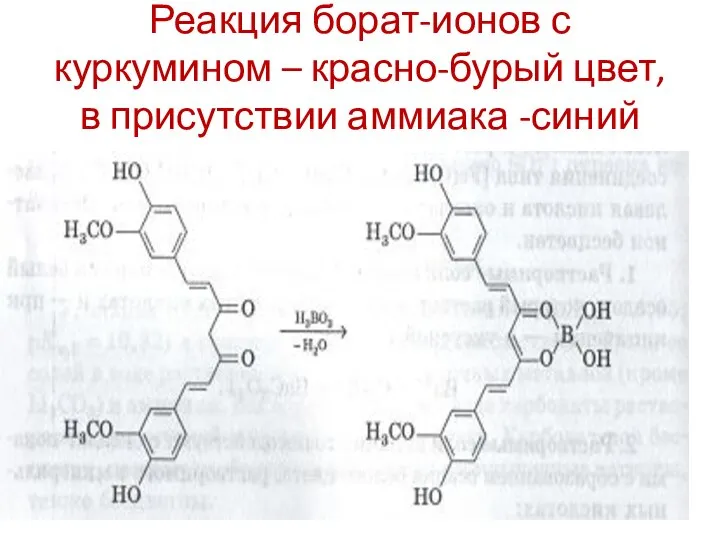
- 123. Реакция борат-ионов с куркумином – красно-бурый цвет, в присутствии аммиака -синий
- 124. Образование и горение этилового эфира борной кислоты
- 125. Реакция борат-инов с хинализарином
- 126. 6. СИЛИКАТ-ИОНЫ Реакции анионов I аналитической группы
- 127. Реакции силикат-ионов Соли бария Нитрат серебра Разбавленные кислоты Образование фторида кремния Молибдат аммония
- 128. Образование желтого силиката серебра 2Ag++SiO32-= =Ag2SiO3
- 129. Образование фторида кремния Na2SiO3+6HF= SiF4+3H2O+2NaF
- 130. 7. ФТОРИД-ИОНЫ Реакции анионов I аналитической группы
- 131. Реакции ФТОРИД-ионов Соли бария Тиоцианат железа Цирконий-ализариновый комплекс Образование фторида кремния (травление стекла)
- 132. Обесцвечивание «кровавой раны» Fe(SCN)3+6F-=[FeF6]3-+3SCN-
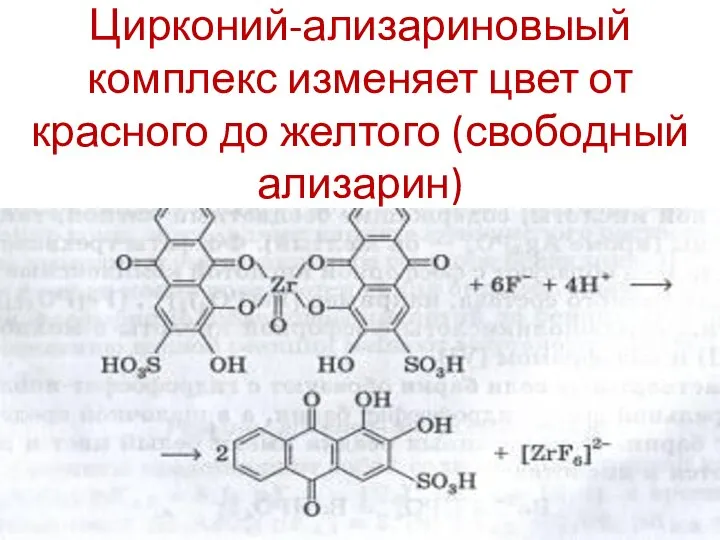
- 133. Цирконий-ализариновыый комплекс изменяет цвет от красного до желтого (свободный ализарин)
- 134. 8. ФОСФАТ-ИОНЫ Реакции анионов I аналитической группы
- 135. Реакции фосфат-ионов Соли бария Нитрат серебра Магнезиальная смесь Молибдат аммония Образование молибденовой сини
- 136. Образование гетерополисоединений с молибдатом аммония (NH4)3[PMo12O40]
- 137. ОБРАЗОВАНИЕ МОЛИБДЕНОВОЙ СИНИ Гетерополимолебде-новоая кислота и ее соли восстанавливаются до продукта синего цвета, неизвестного состава
- 138. 9-10. АРСЕНИТ И АРСЕНАТ-ИОНЫ Реакции анионов I аналитической группы
- 139. Образование арсина 4Zn+AsO42-+11H+= AsH3+4Zn2++4H2O
- 140. Реакция Гутцайта
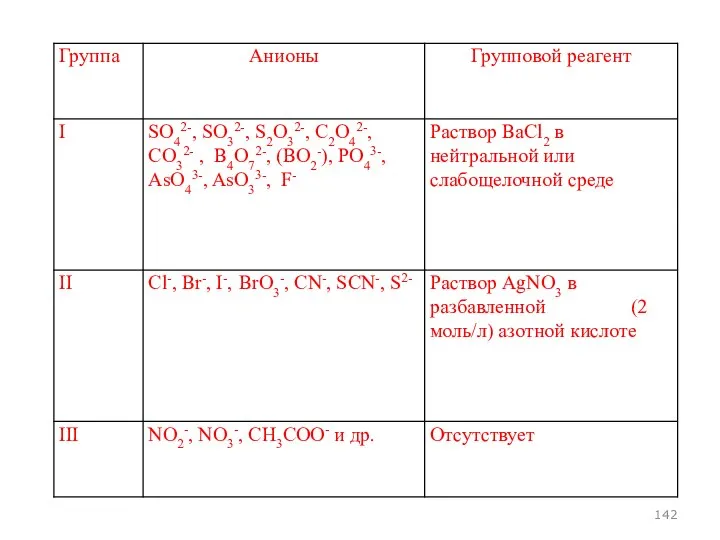
- 141. Реакции Арсенит и арсенат-ионов Соли бария Нитрат серебра Сероводород Молибдат аммония Иод/иодид калия Восстановление до арсина
- 143. Классификация анионов, основанная на их окислительно-восстановительных свойствах
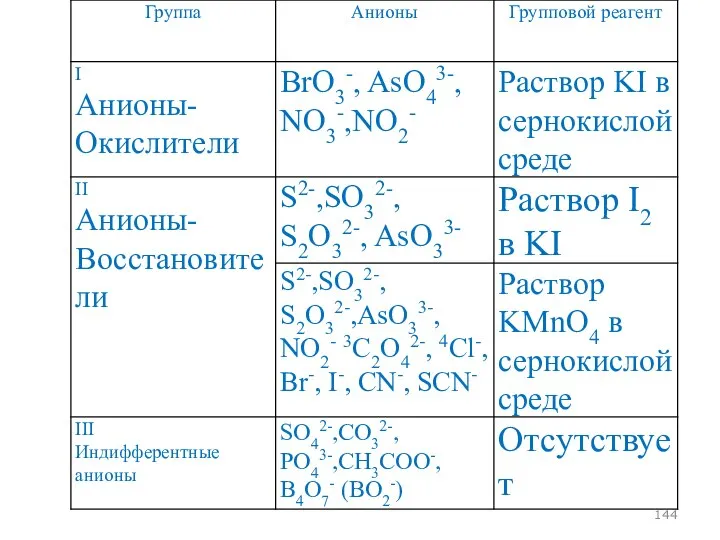
- 145. Классификация анионов, основанная на их окислительно-восстановительных свойствах
- 148. Скачать презентацию





































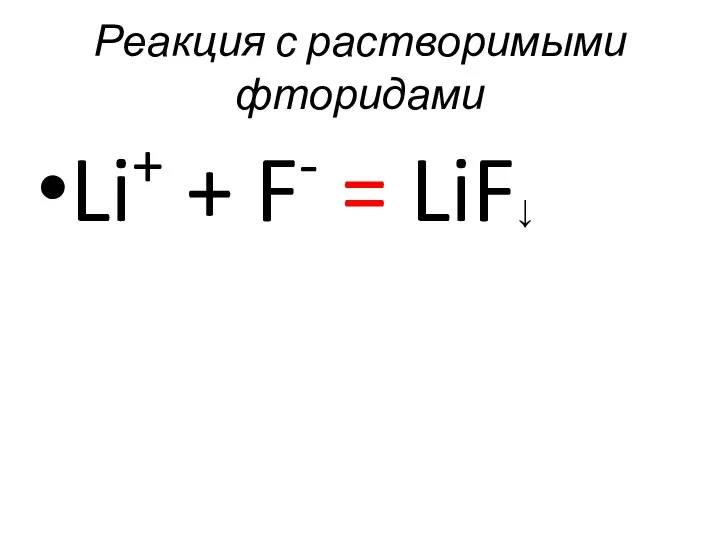
![Микрокристаллоскопическая реакция с цинкуранилацетатом (фармакопейная). Na+ + Zn[(UО2)3(CH3CОО)8] + СН3СОО- + 9Н2О =NaZn(UО2)3(CH3CОО)9∙9Н2О](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-45.jpg)
![.Реакция с гексагидроксостибатом (V) калия Na+ + [Sb(OH)6]- =Na[Sb(OH)6]↓](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-46.jpg)

![Реакция с гексанитрокобальтатом (III) натрия (фармакопейная) 2К+ + Na3[Co(NО2)6] = NaK2[Co(NО2)6↓ + 2Na+.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-48.jpg)

![Реакция с реактивом Несслера — смесью раствора тетрайодомеркурama(II) калия K2[HgI4] с](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-52.jpg)








![Реакция восстановления Ag+ до металлического серебра 4[Ag(NH3)2]OH + CH2O = 4Ag↓](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-61.jpg)








![Водный раствор аммиака 2Hg22+ + 4NH3 + Н2О = [OHg2NH2]+ + 2Hg↓ + 3NH4+.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-70.jpg)







![Гексацианоферрат (II) калия Са2+ + К+ + NH4++ [Fe(CN)6]4- = NH4KCa[Fe(CN)6]↓.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-80.jpg)
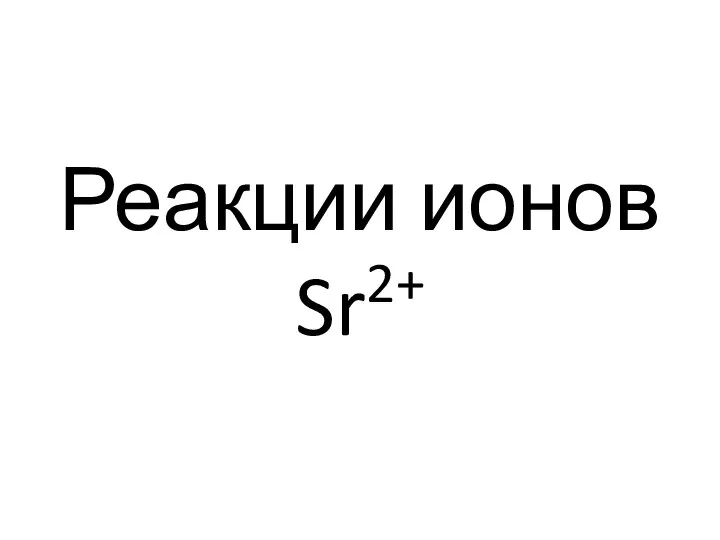



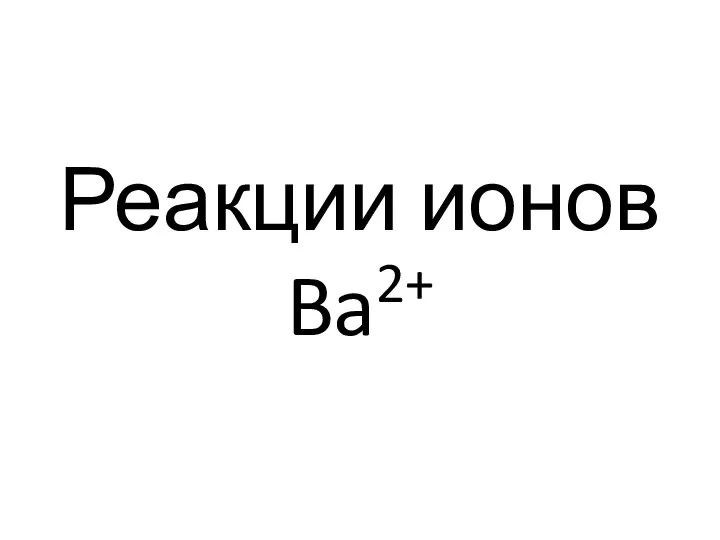












![Реакция с нитратом серебра Ag2SO3(белый осадок)+ Na2SO3 =2Na[Ag(SO3 ) 2]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-102.jpg)


![Нитропруссид натрия - Na2[Fe(CN)5NO] – КРАСНОЕ ОКРАШИВАНИЕ, состав продукта неизвестен](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-107.jpg)


![Нитрат серебра Ag2S 2 O3(белый осадок)+ Na2S 2 O3 =2Na 3[Ag(S2O3)2]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-110.jpg)


















![Обесцвечивание «кровавой раны» Fe(SCN)3+6F-=[FeF6]3-+3SCN-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-131.jpg)


![Образование гетерополисоединений с молибдатом аммония (NH4)3[PMo12O40]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394466/slide-135.jpg)







 Химия сверхкритических жидкостей
Химия сверхкритических жидкостей Презентация Химический состав мороженного
Презентация Химический состав мороженного Аминокислоты
Аминокислоты Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Дмитрий Иванович Менделеев (1834–1907)
Дмитрий Иванович Менделеев (1834–1907) Яковлева Татьяна Алексеевна Ярославль, 2009 г.
Яковлева Татьяна Алексеевна Ярославль, 2009 г.  Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола
Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола Гидролиз органических веществ
Гидролиз органических веществ Лекарственная форма порошки
Лекарственная форма порошки Математический аппарат квантовой механики
Математический аппарат квантовой механики Жиры (триглицериды)
Жиры (триглицериды) Аттестационная работа. Способ формирования метапредметных результатов обучения при обучении химии в условиях реализации ФГОС
Аттестационная работа. Способ формирования метапредметных результатов обучения при обучении химии в условиях реализации ФГОС Субстраты для гидропоники
Субстраты для гидропоники Альдегидтер
Альдегидтер Anionic Polymerization
Anionic Polymerization Воздух
Воздух Теория строения химических соединений А. М. Бутлерова
Теория строения химических соединений А. М. Бутлерова Дисперсные системы (продолжение)
Дисперсные системы (продолжение) Диоксины, глобальные экотоксиканты
Диоксины, глобальные экотоксиканты Загальна характеристика рослинних кормiв. (Тема 1)
Загальна характеристика рослинних кормiв. (Тема 1) Технология производства хлорбензола
Технология производства хлорбензола Химиялық формула
Химиялық формула БЕРИЛИЙ, МАГНИЙ И ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
БЕРИЛИЙ, МАГНИЙ И ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ оксиды - св-ва — уч-ся
оксиды - св-ва — уч-ся Алкиндер
Алкиндер Кислотные дожди
Кислотные дожди Фосфор и его соединения
Фосфор и его соединения Твердоконтактные электрохимические платформы для потенциометрических измерений
Твердоконтактные электрохимические платформы для потенциометрических измерений