Содержание
- 2. Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода.
- 3. Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода.
- 4. Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода.
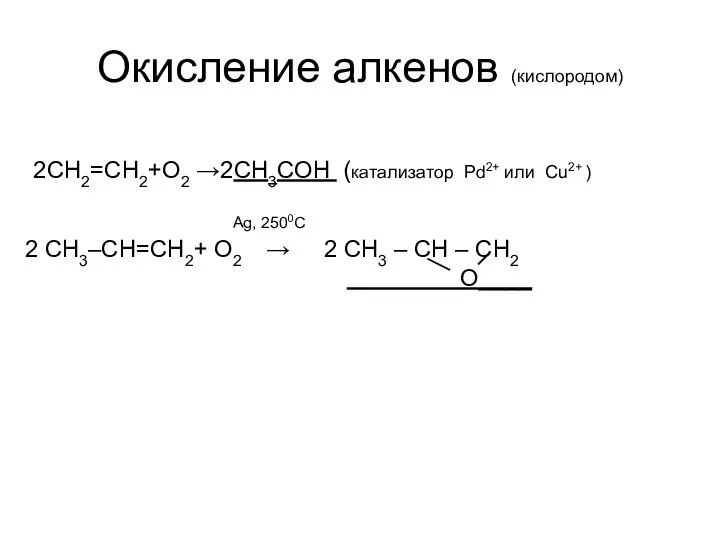
- 5. Окисление алкенов (кислородом) 2CH2=CH2+O2 →2СН3СОН (катализатор Pd2+ или Cu2+ ) Ag, 2500C 2 CH3–CH=CH2+ O2 →
- 6. Окисление алкинов (кислая среда) CH3–C≡C–СН2 –CH3+KMnO4+H2SO4→СН3СООН+С2Н5СООН +MnSO4 +K2SO4+H2O C5H8 +4H2O – 6е → С2Н4О2+С3Н6О2 +6Н+ 5
- 7. Окисление алкинов (нейтральная среда) CН≡CH+KMnO4→КООС – СООК+MnO2+KOH + H2O C2H2 +4H2O – 8е → 2СОО- +10Н+
- 8. Окисление алкинов (нейтральная среда) СН3 – C≡CH+H2O+KMnO4→СН3СООK+КНСО3 +MnO2+KOH C3H4 +5H2O – 8е → CH3СОО- + HCO3-
- 9. Окисление алкинов (щелочная среда) CH3–C≡CH+KMnO4+KOH→СН3СООК+К2СО3 +K2MnO4+ H2O C3H4 +11OH- – 8е → СН3СОО- + СО32- +6H2O
- 10. Окисление аренов (кислая среда) С6H5 – CH3 +KMnO4+H2SO4→С6Н5СООН+MnSO4 +K2SO4+H2O C7H8 +2H2O – 6е → С7Н6О2 +6Н+
- 11. Окисление аренов (кислая среда) С6H5СН2 – CH3 +KMnO4+H2SO4→С6Н5СООН +CO2+ MnSO4 +K2SO4+H2O C8H10 +4H2O – 12е →
- 12. Окисление аренов (щелочная среда) С6H5 – CH3 +KMnO4+KOH→С6Н5СООК + K2MnO4+ H2O C7H8 +7OH- – 6е →
- 13. Окисление аренов (щелочная среда) С6H5СН2–CH3+KMnO4+KOH→С6Н5СООК +К2СО3+K2MnO4+H2O C8H10 +15OH- – 12е → С6Н5СОО- + CO32- +10H2O 1
- 14. Окисление аренов (нейтральная среда) С6H5 – CH3 +KMnO4→С6Н5СООK+MnO2+KOH + H2O C7H8 +2H2O – 6е → С6Н5СОО-
- 15. Окисление аренов (нейтральная среда) С6H5СН2 – CH3+KMnO4→С6Н5СООK+ К2СО3+ MnO2+KOH + H2O C8H10 +5H2O – 12е →
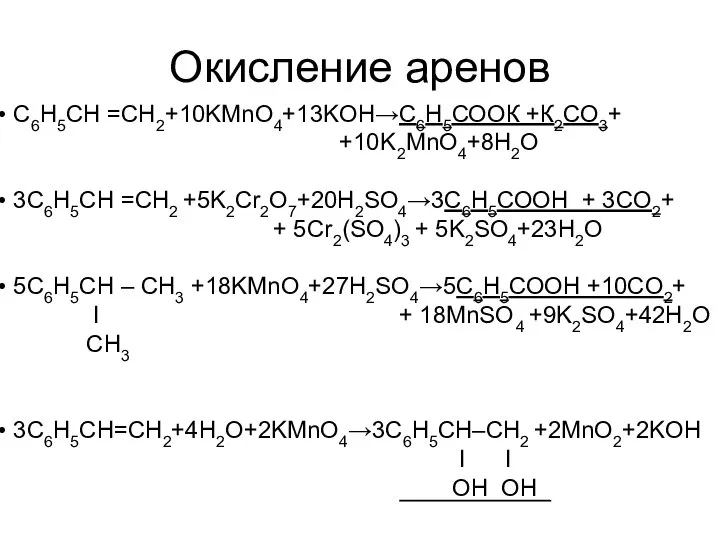
- 16. Окисление аренов С6H5СН =CH2+10KMnO4+13KOH→С6Н5СООК +К2СО3+ +10K2MnO4+8H2O 3С6H5СН =CH2 +5K2Cr2O7+20H2SO4→3С6Н5СООН + 3CO2+ + 5Cr2(SO4)3 + 5K2SO4+23H2O 5С6H5СН
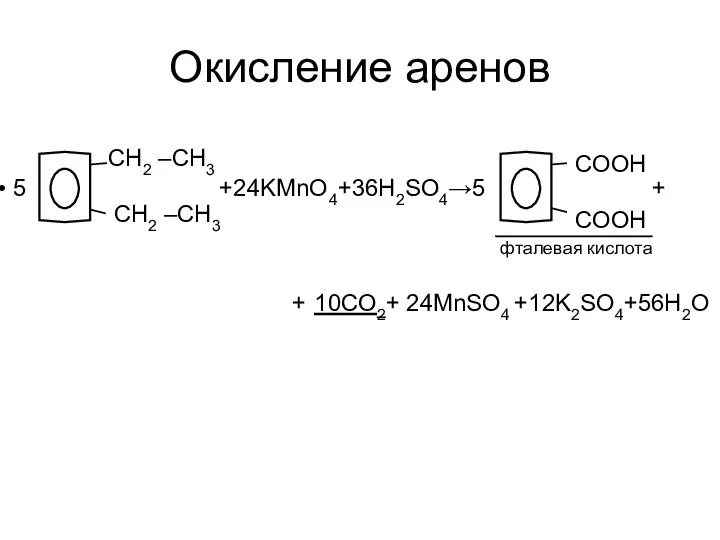
- 17. Окисление аренов 5 +24KMnO4+36H2SO4→5 + фталевая кислота + 10CO2+ 24MnSO4 +12K2SO4+56H2O CH2 –CH3 CH2 –CH3 COOH
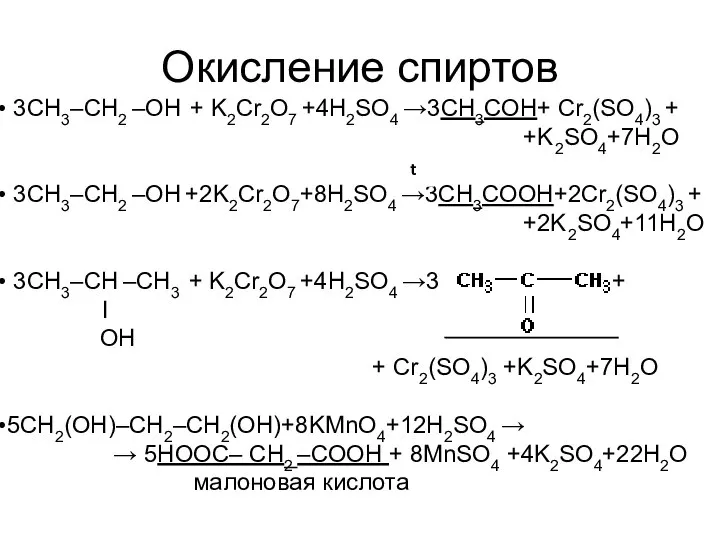
- 18. Окисление спиртов 3CH3–CH2 –ОН + K2Cr2O7 +4H2SO4 →3СН3СОН+ Cr2(SO4)3 + +K2SO4+7H2O 3CH3–CH2 –ОН +2K2Cr2O7+8H2SO4 →3СН3СОOН+2Cr2(SO4)3 +
- 19. Окисление альдегидов 3CH3–CОН +2[Ag(NH3)2]OH→3СН3СОONH4+2Ag +3NH3+7H2O HCOOH +2[Ag(NH3)2]OH→ (NH4)2CO3 +H2O +2Ag +2NH3 CH3–CОН + 2KMnO4 +3KOH →СН3СОOK+
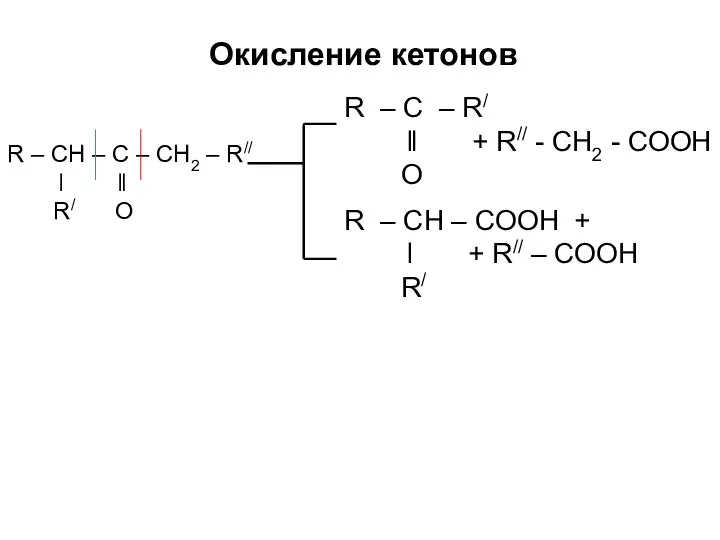
- 20. R – CH – C – CH2 – R// ǀ ǁ R/ O Окисление кетонов R
- 22. Скачать презентацию













![Окисление альдегидов 3CH3–CОН +2[Ag(NH3)2]OH→3СН3СОONH4+2Ag +3NH3+7H2O HCOOH +2[Ag(NH3)2]OH→ (NH4)2CO3 +H2O +2Ag +2NH3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1398094/slide-18.jpg)
 Задачи на смеси и сплавы
Задачи на смеси и сплавы Прибор “октис-2”
Прибор “октис-2” Кристаллооптический метод в петрографии
Кристаллооптический метод в петрографии Роль ферментов в формировании потребительских свойств продовольственных товаров
Роль ферментов в формировании потребительских свойств продовольственных товаров Пластмасса
Пластмасса Aromatik uglevodorodlar (Arenlar)
Aromatik uglevodorodlar (Arenlar) Презентация Поспеловой С.В. учителя химии ГОУ школа №122 Центрального р-на Санкт-Петербурга Алюминий и его соединения
Презентация Поспеловой С.В. учителя химии ГОУ школа №122 Центрального р-на Санкт-Петербурга Алюминий и его соединения Генетическая связь между основными классами органических соединений
Генетическая связь между основными классами органических соединений Химические опасности. Нитраты
Химические опасности. Нитраты Підготувала Учениця 11 класу Лемак Андріана
Підготувала Учениця 11 класу Лемак Андріана  КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко Эволюция антропогенных загрязнений в окружающей среде. Роль физико-химических явлений
Эволюция антропогенных загрязнений в окружающей среде. Роль физико-химических явлений Классификация неорганических веществ
Классификация неорганических веществ Влияние эфирного масла и конкрета из шалфея мускатного на организм человека Подготовила студентка 4 курса группа 42 TF Даной Ян
Влияние эфирного масла и конкрета из шалфея мускатного на организм человека Подготовила студентка 4 курса группа 42 TF Даной Ян Обобщающий урок по теме «Неметаллы» 9 класс
Обобщающий урок по теме «Неметаллы» 9 класс Характеристики ковалентной связи .Длина связи. Энергия связи. Полярность связи
Характеристики ковалентной связи .Длина связи. Энергия связи. Полярность связи Федосовой Таисии 8 «в»
Федосовой Таисии 8 «в» Медициналық тәжірибедегі потенциометриялар
Медициналық тәжірибедегі потенциометриялар Галогены
Галогены Классы неорганических веществ
Классы неорганических веществ Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Семь чудес света и роль металлов в их создании
Семь чудес света и роль металлов в их создании Спирты и их влияние на здоровье человека
Спирты и их влияние на здоровье человека Оцтова кислота
Оцтова кислота Валентность и степень окисления. Химическая связь
Валентность и степень окисления. Химическая связь Роль химической науки в производстве искусственной пищи
Роль химической науки в производстве искусственной пищи Презентация по Химии "Химическая посуда" - скачать смотреть бесплатно
Презентация по Химии "Химическая посуда" - скачать смотреть бесплатно Химия 9 класс. Введение - повторение
Химия 9 класс. Введение - повторение