Презентация Поспеловой С.В. учителя химии ГОУ школа №122 Центрального р-на Санкт-Петербурга Алюминий и его соединения
Содержание
- 2. Положение в Периодической системе Алюминий располагается в 3 периоде, в главной подгруппе 3 группы. Порядковый номер
- 3. Строение атома алюминия Заряд ядра атома алюминия +13 В атоме 3 энергетических уровня Электронная оболочка атома
- 4. Нахождение в природе По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния
- 5. Получение алюминия Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы калия
- 6. Физические свойства плотность (при 20°С) 2698,9 кг/м3; tпл 660,24°С; tкип около 2500°С; Алюминий сочетает весьма ценный
- 7. Химические свойства Окисляется на воздухе: 4Al + 3O2 = 2Al2O3 4 Al0 - 3ē → Al+3
- 8. Химические свойства Взаимодействует с кислотами: 2Al + 6HCl = 2AlCl3 + 3H2↑ 2Al + 6H+ +
- 9. Химические свойства Вытесняет металлы из их оксидов (алюминотермия): 8Al + 3Fe3O4 = 9Fe + 4Al2O3 8
- 10. Соединения алюминия. Оксид Очень твердый порошок белого цвета. Образуется: а) при окислении или горении алюминия: 4Al
- 11. Химические свойства оксида алюминия Al2O3 по характеру амфотерный оксид. Взаимодействует: а) с кислотами: Al2O3 + 3H2SO4
- 12. Гидроксид алюминия Белый нерастворимый в воде порошок Проявляет амфотерные свойства. Взаимодействует: а) с кислотами: Al(OH)3 +
- 14. Скачать презентацию











 Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Нефть, классификация, применение, основные показатели ,особенности кодировки
Нефть, классификация, применение, основные показатели ,особенности кодировки Композиты на основе полибензоксазинов
Композиты на основе полибензоксазинов Презентация по Химии "Полімери" - скачать смотреть бесплатно
Презентация по Химии "Полімери" - скачать смотреть бесплатно Основні класи неорганічних речовин
Основні класи неорганічних речовин Химические формулы. Классы неорганических веществ. Урок №1
Химические формулы. Классы неорганических веществ. Урок №1 Методология, принципы и методы изучения МПИ
Методология, принципы и методы изучения МПИ Минералы и Близнецы
Минералы и Близнецы 8 класс
8 класс  Эмульсии и эмульгаторы
Эмульсии и эмульгаторы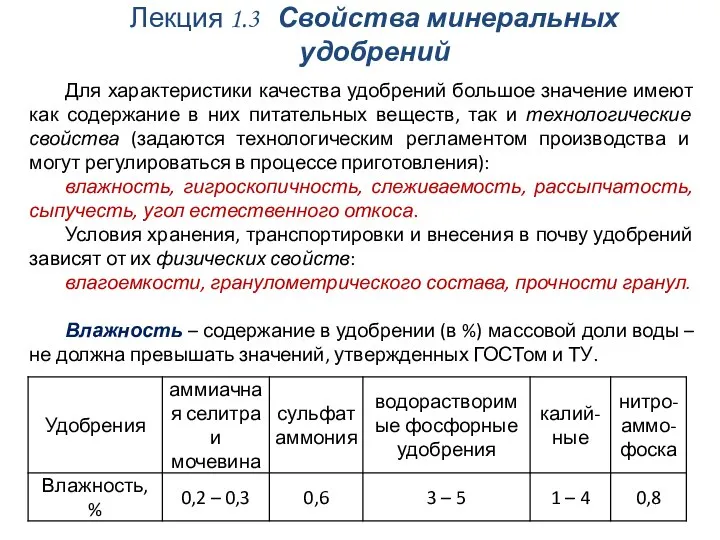 Свойства минеральных удобрений
Свойства минеральных удобрений Электрическая проводимость растворов
Электрическая проводимость растворов Презентация по Химии "Показатели воды: её жесткость и кислотность" - скачать смотреть
Презентация по Химии "Показатели воды: её жесткость и кислотность" - скачать смотреть  Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева
Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева Силикатная промышленность
Силикатная промышленность Кислотные дожди
Кислотные дожди Общая и неорганическая химия
Общая и неорганическая химия Білки. Функції білків в організмі
Білки. Функції білків в організмі Органические вещества
Органические вещества Безопасная пластмасса
Безопасная пластмасса Этиленовые, олефины, непредельные алкены
Этиленовые, олефины, непредельные алкены Методы диффузионной металлизации
Методы диффузионной металлизации Гипоксия
Гипоксия Презентация по Химии "Етери та естери" - скачать смотреть бесплатно
Презентация по Химии "Етери та естери" - скачать смотреть бесплатно Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно
Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно Химия в нашей жизни
Химия в нашей жизни Поверхностные явления. Лекция 15
Поверхностные явления. Лекция 15 Хімічні речовини у побуті підготували Стебко Марія, Бондар Аліна 11-Ф
Хімічні речовини у побуті підготували Стебко Марія, Бондар Аліна 11-Ф