Содержание
- 3. Общие формулы углеводородов: СnH2n+2 –алканы (все связи одинарные) СnH2n –циклоалканы (цикл с одинарными связями) СnH2n –алкены
- 4. Запомните! Суффиксы: - одинарная связь - ан - двойная связь - ен - две двойных -
- 5. 1) соединяться друг с другом в цепи различного строения: открытые (неразветвленные, разветвленные) и замкнутые; 2) образовывать
- 6. Структурные формулы молекул органических соединений
- 7. Отличия органических соединений от неорганических. Органические соединения отличаются от неорганических рядом характерных особенностей: почти все органические
- 8. Типы изомерии.
- 11. Скачать презентацию
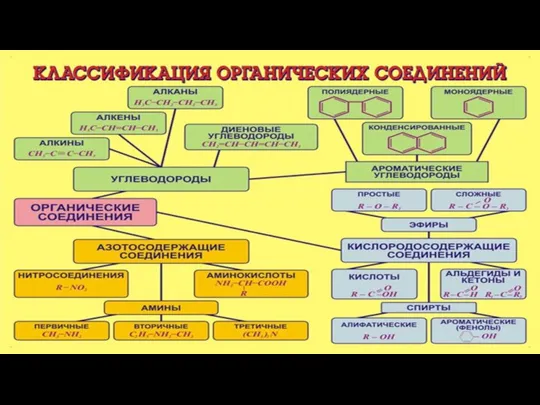






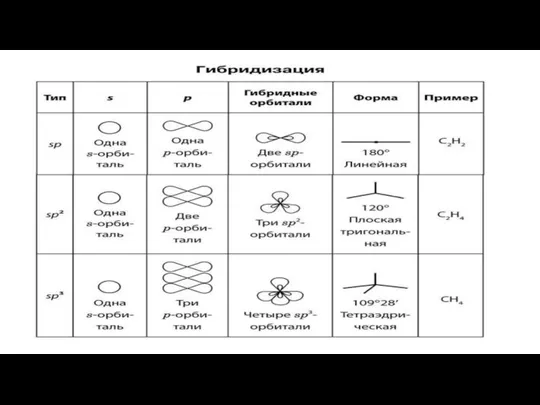
 СПИРТЫ
СПИРТЫ  Круговорот углерода в природе. Изготовлено: А.С.Большаков
Круговорот углерода в природе. Изготовлено: А.С.Большаков Контроль в процессе обучения химии на старшей ступени школы
Контроль в процессе обучения химии на старшей ступени школы Лед – как состояние воды
Лед – как состояние воды Презентация по Химии "Средства для борьбы с насекомыми" - скачать смотреть
Презентация по Химии "Средства для борьбы с насекомыми" - скачать смотреть 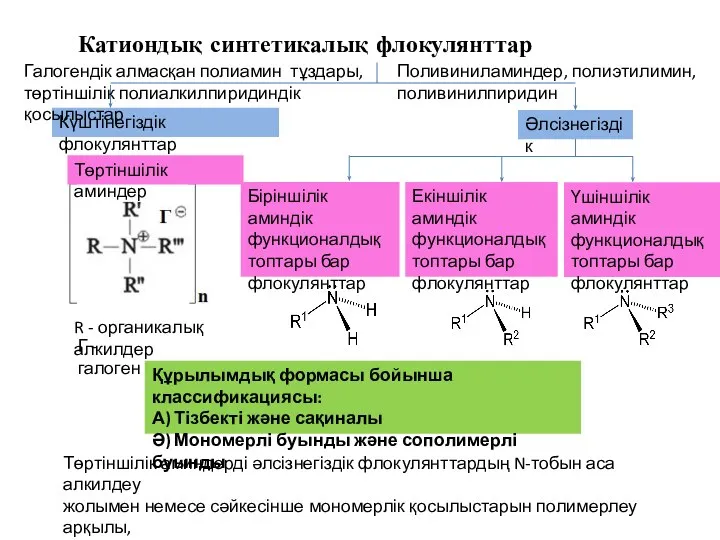 Катиондық синтетикалық флокулянттар
Катиондық синтетикалық флокулянттар Кислоты: классификация, реакции, применение
Кислоты: классификация, реакции, применение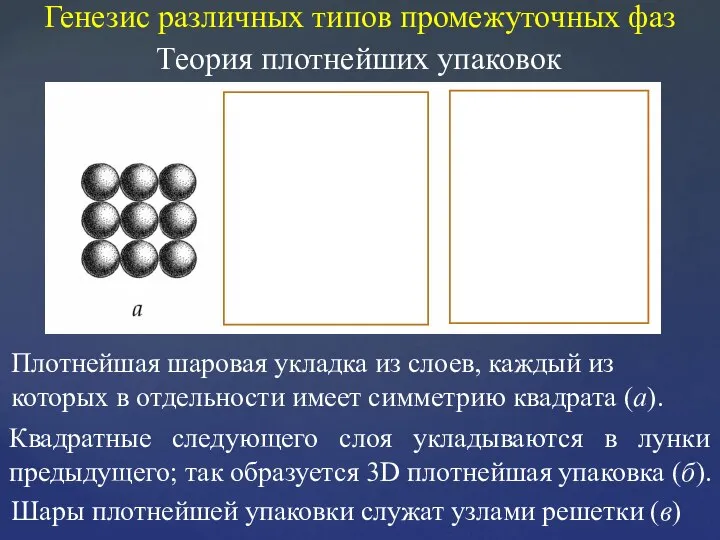 Генезис различных типов промежуточных фаз. Теория плотнейших упаковок
Генезис различных типов промежуточных фаз. Теория плотнейших упаковок Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Добування кисню та вивчення його властивостей
Добування кисню та вивчення його властивостей Химия и физика пигментов
Химия и физика пигментов Поліетелен Застосування поліетилену Автор Фурка Т.А.
Поліетелен Застосування поліетилену Автор Фурка Т.А.  Уравнения химической реакции 8 класс
Уравнения химической реакции 8 класс Карбонатна кислота. Карбонати. Підготувала: Учениця 10 класу Прилуцької ЗОШ І-ІІІ ст. № 13 Імені Святителя Іоасафа Бєлгородсько
Карбонатна кислота. Карбонати. Підготувала: Учениця 10 класу Прилуцької ЗОШ І-ІІІ ст. № 13 Імені Святителя Іоасафа Бєлгородсько Изомерия органических соединений. 10 класс
Изомерия органических соединений. 10 класс Эмульгаторы. Коллоиды. Гелеобразующие и увлажняющие вещества в косметическом производстве
Эмульгаторы. Коллоиды. Гелеобразующие и увлажняющие вещества в косметическом производстве Кислоты. Состав кислот
Кислоты. Состав кислот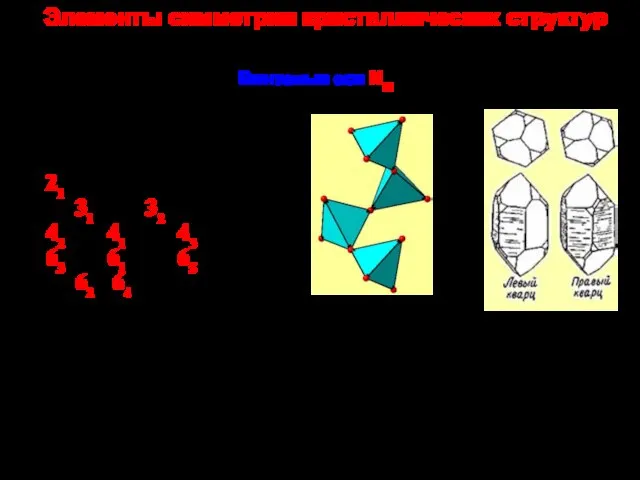 Элементы симметрии кристаллических структур
Элементы симметрии кристаллических структур Аналитическая химия Преподаватель Ельчищева Юлия Борисовна
Аналитическая химия Преподаватель Ельчищева Юлия Борисовна  Торий
Торий Характеристика и свойства истинных растворов
Характеристика и свойства истинных растворов Химические формулы. Атомная и молекулярная массы
Химические формулы. Атомная и молекулярная массы Энергетический обмен
Энергетический обмен Основные классы неорганических соединений
Основные классы неорганических соединений Обмен липидов
Обмен липидов Сложные вопросы ЕГЭ по химии
Сложные вопросы ЕГЭ по химии Гидроксид аммония
Гидроксид аммония Производные аминоалкилбензолов. (Тема 3)
Производные аминоалкилбензолов. (Тема 3)