Содержание
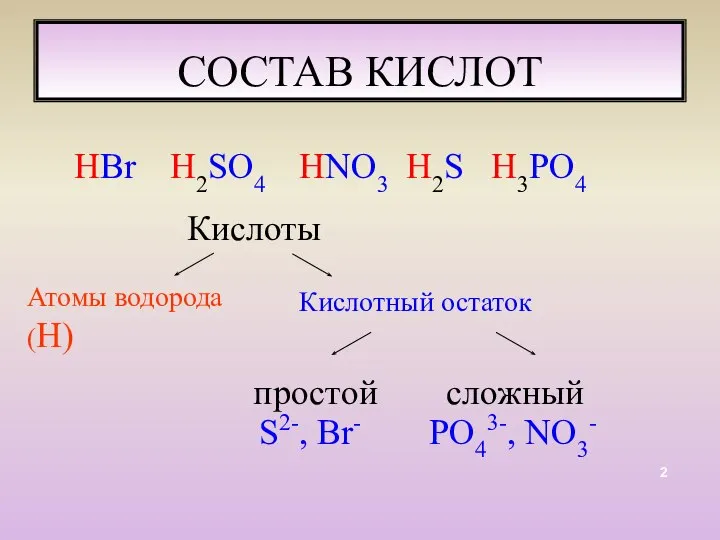
- 2. СОСТАВ КИСЛОТ HВr H2SO4 HNO3 H2S H3PO4 Кислоты Атомы водорода(Н) Кислотный остаток простой сложный S2-, Br-
- 3. Кислоты - это сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка.
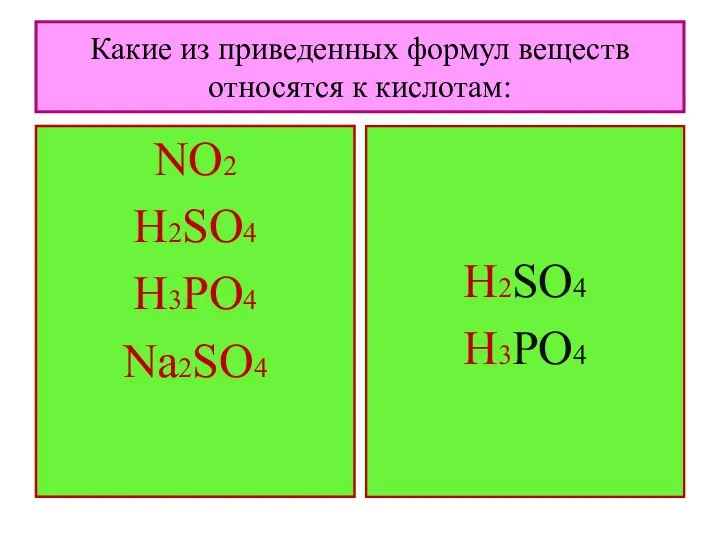
- 4. Какие из приведенных формул веществ относятся к кислотам: NO2 H2SO4 H3PO4 Na2SO4 H2SO4 H3PO4
- 5. Классификация кислот По содержанию атомов кислорода в кислоте: Беcкислородные - HCI, НВr, HI Кислородсодержащие - НNО3,
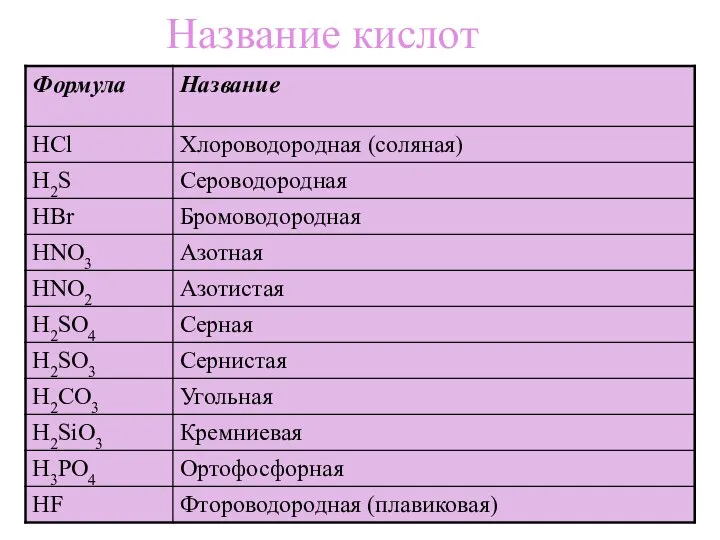
- 6. Название кислот
- 7. Действие кислот на индикаторы Вывод: лакмус и метилоранж можно использовать для определения кислоты + лакмус -
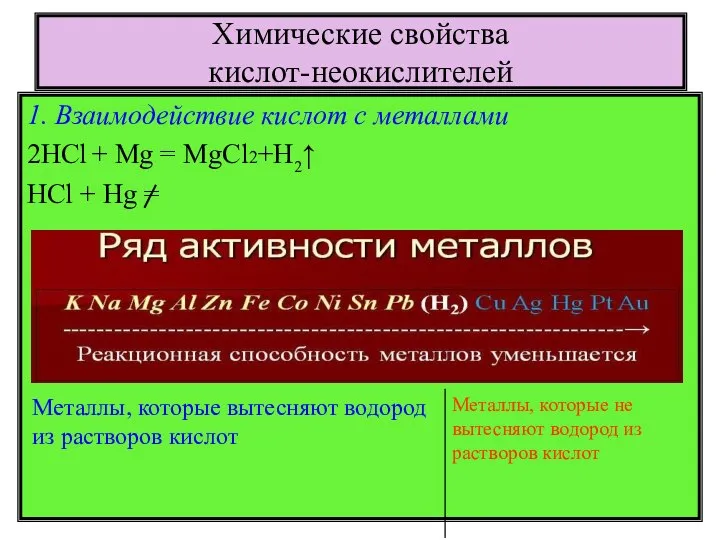
- 8. Химические свойства кислот-неокислителей 1. Взаимодействие кислот с металлами 2HCl + Mg = MgCl2+H2↑ HCl + Hg
- 9. С какими из перечисленных металлов реагирует соляная кислота Ca Cu Ag Zn Ca + 2HCl =
- 10. 2. Взаимодействие кислот с основными оксидами H2SO4+ MgO = MgSO4+H2O 3. Взаимодействие кислот с основаниями –
- 11. 5. Неустойчивые кислоты угольная и сернистая разлагаются на газ и воду: H2CO3 ↔ H2O + CO2↑
- 12. С какими из перечисленных веществ будет взаимодействовать раствор серной кислоты CO2 ZnO Fe(OH)2 NaCl BaCl2 CO2
- 14. Скачать презентацию







 Crystal Defects and Noncrystalline Structure–Imperfection
Crystal Defects and Noncrystalline Structure–Imperfection Синтетические каучуки
Синтетические каучуки Химия в жизни художника
Химия в жизни художника Презентация по Химии "Ломоносов Михайло Васильевич" - скачать смотреть
Презентация по Химии "Ломоносов Михайло Васильевич" - скачать смотреть  Алкины. Номенклатура и изомерия
Алкины. Номенклатура и изомерия pH жидкостей, необходимых для человека
pH жидкостей, необходимых для человека  Химическая промышленность
Химическая промышленность Элементы третьего периода, периодической системы Д. И. Менделеева
Элементы третьего периода, периодической системы Д. И. Менделеева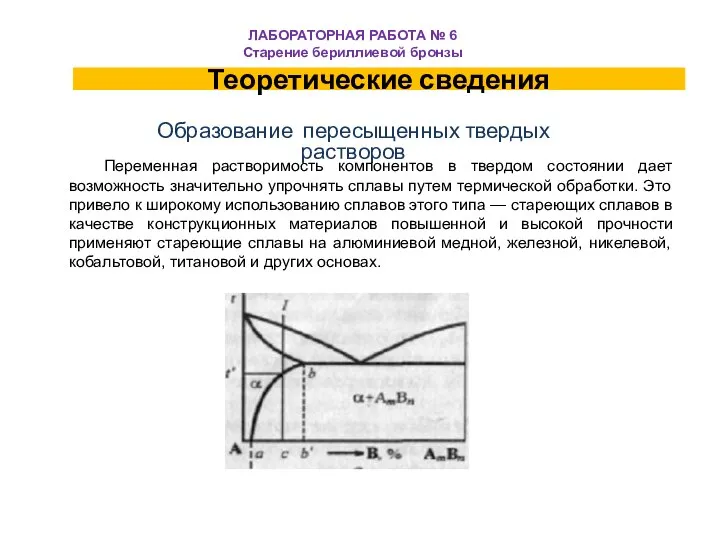 Старение бериллиевой бронзы
Старение бериллиевой бронзы Золото. 79-й элемент таблицы
Золото. 79-й элемент таблицы Химия гетероциклических соединений
Химия гетероциклических соединений Фосфор. Получение. Химические свойства
Фосфор. Получение. Химические свойства Олимпиада по химии
Олимпиада по химии Химический состав фракций нефти
Химический состав фракций нефти Витамин В
Витамин В Общая характеристика элементов IVA-группы. Углерод и кремний
Общая характеристика элементов IVA-группы. Углерод и кремний Препараты гормонов стероидной структуры
Препараты гормонов стероидной структуры Буферные системы крови
Буферные системы крови Растворы электролитов
Растворы электролитов Презентация по Химии "Общая характеристика подгруппы углерода. Углерод" - скачать смотреть
Презентация по Химии "Общая характеристика подгруппы углерода. Углерод" - скачать смотреть  Карбоновые кислоты
Карбоновые кислоты Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Литология. Глинистые породы
Литология. Глинистые породы 20141105_otkrytyy_urok_v_7-m_klasse_spetsialnoy_korrektsionnoy_shkoly_viii_vida_po_teme_khranenie_mineralnykh_udobreniy
20141105_otkrytyy_urok_v_7-m_klasse_spetsialnoy_korrektsionnoy_shkoly_viii_vida_po_teme_khranenie_mineralnykh_udobreniy Комплексные соединения
Комплексные соединения Пробоподготовка (HPLC, instrumental analysis)
Пробоподготовка (HPLC, instrumental analysis) Презентация по Химии "Презентация Золото" - скачать смотреть
Презентация по Химии "Презентация Золото" - скачать смотреть