Органикалық қосылыстар құрылысының теориялық негіздері және олардың реакцияға қабілеттілігін анықтаушы факторлар
Содержание
- 2. Жоспар 1) Органикалық қосылыстар дегеніміз не? Органикалық қосылыстардың жіктелуі. 2) Органикалық қосылыстардың изомериясы және номенклатурасы. 3)
- 3. Органикалық химия (ОХ) ОХ - көмірсутектер және олардың туындыларының қасиеттерін, құрамын және құрылымын зерттейтін ғылым органикалық
- 4. Биоорганикалық химия БиоОХ- тірі организмдегі процестердің негізінде жататын заттарды, олардың биологиялық функцияларымен тікелей байланыстыра қарастырады. Организмді
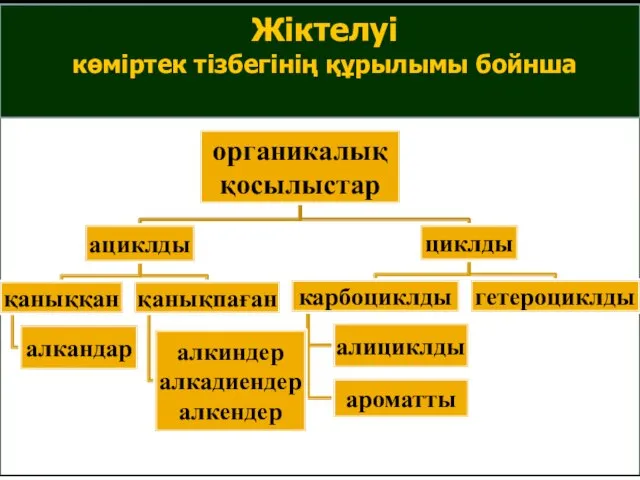
- 5. Жіктелуі көміртек тізбегінің құрылымы бойнша
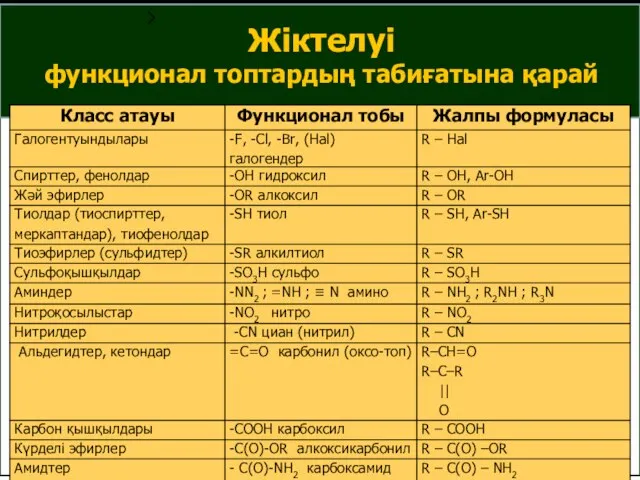
- 6. Жіктелуі функционал топтардың табиғатына қарай
- 7. Жіктелуі Бір функционал тобы бар қосылыстар аталады монофункционалды бірнеше функционал тобы болса – полифункционалды әр түрлі
- 8. Химиялық байланыс ОҚ байланыстардың негізгі түрі коваленттік байланыс, яғни байланысатын атомдардың электрондарының жұптасуынан түзілетін химиялық байланыс
- 9. Номенклатура Әрбір жеке қосылысты атауға мүмкіндік беретін ережелер жүйесін – номенклатура деп атайды. ИЮПАК (IUРАС –теориялық
- 10. Номенклатуралық терминдер Молекуланың аталуын қою үшін қосылыс келесі құрылымдық элементтерді бөледі: көмірсутекті радикал бастаушы құрылым орынбасушы
- 11. Көмірсутекті радикал – бір немесе бірнеше сутек атомын алғанда, бір немесе бірнеше валенттілігі бос қалған, молекула
- 12. Номенклатуралық терминдер Бастаушы құрылым – басты көміртек тізбегі және карбо – және гетероциклдердегі циклды құрылым. Орынбасушы
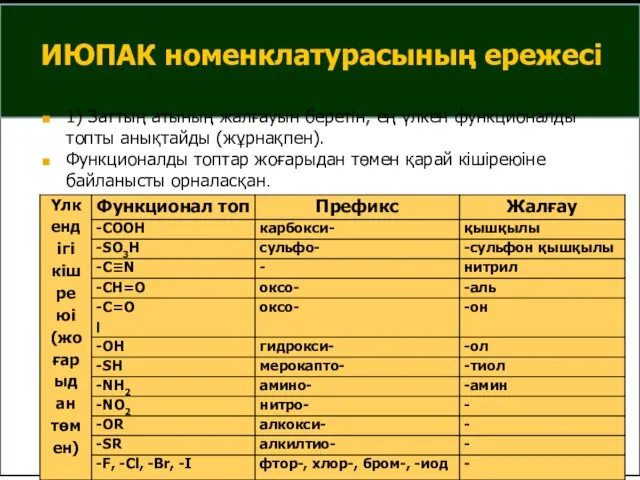
- 13. 1) Заттың атының жалғауын беретін, ең үлкен функционалды топты анықтайды (жұрнақпен). Функционалды топтар жоғарыдан төмен қарай
- 14. ИЮПАК номенклатурасының ережесі 2) Бастапқы құрлысын анықтайды. Ол үшін ен ұзын неғұрлым көп орынбасушысы, қанықпаған байланыстары
- 15. ИЮПАК номенклатурасының ереже 5) Алфавит ретімен аталатын орынбасушылардың (кіші функционал топтар - префикстер, көміртегісіз орынбасушылар, көміртекті
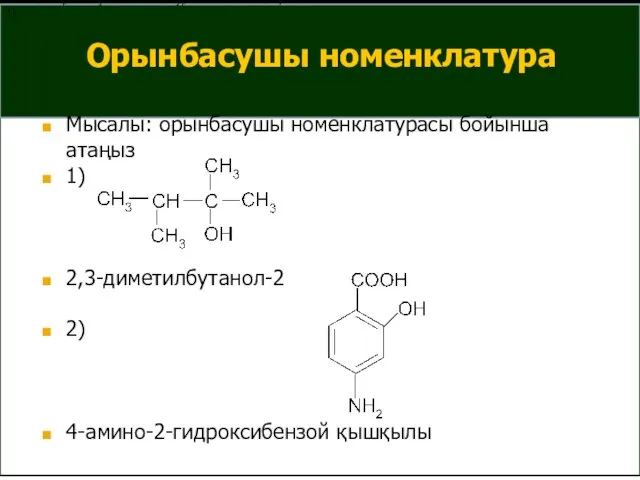
- 16. Орынбасушы номенклатура Мысалы: орынбасушы номенклатурасы бойынша атаңыз 1) 2,3-диметилбутанол-2 2) 4-амино-2-гидроксибензой қышқылы Мысалы: орынбасушы номенклатурасы бойынша
- 17. Осы номенклатура бойынша атаулар негізіне гомолог қатарындағы қарапайым (бірінші) өкілі алынады. Қалған қосылыстар сутек атомының орынбасумен
- 18. Радикало-функционалды номенклатура Органикалық радикалдың атауын қосатын, қосылыстың химиялық класын анықтайтын, мінездемелік функционалды топтың аты негізгі атауына
- 19. Изомерлер Изомерлер – құрамы бірдей, бірақ атомдардың байланысу реті әртүрлі немесе кеңістіктегі орналасуы, қасиеттері әртүрлі қосылыстар.
- 20. Структуралық изомерлер Структуралық изомерлер өздерінің химиялық құрлысы яғни атомдардың арасындағы байланыстардың табиғаты немесе реті бойынша ажыратылады.
- 21. Стереоизомерлер Стереоизмерлер - молекуладағы атомдардың кеңістіктегі орналасуымен бөлектенеді. Стереохимияда негізгі екі түсінік бар: конфигурация конформацияны
- 22. Конфигурация Конфигурация – молекуладағы атомдардың кеңістікте белгілі ретпен орналасуы. Конфигурациялық изомерлерге жатады: оптикалық изомерлер (асимметриялық көміртек
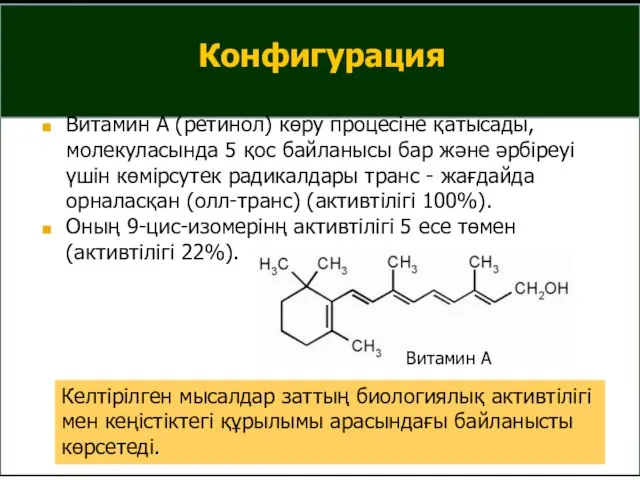
- 23. Конфигурация Витамин А (ретинол) көру процесіне қатысады, молекуласында 5 қос байланысы бар және әрбіреуі үшін көмірсутек
- 24. Конформация Конформация – деп белгілі бір конфигурациядағы молекуланың атомдарының бір немесе бірнеше σ-байланыстар айналасында бұрылу нәтижесінде
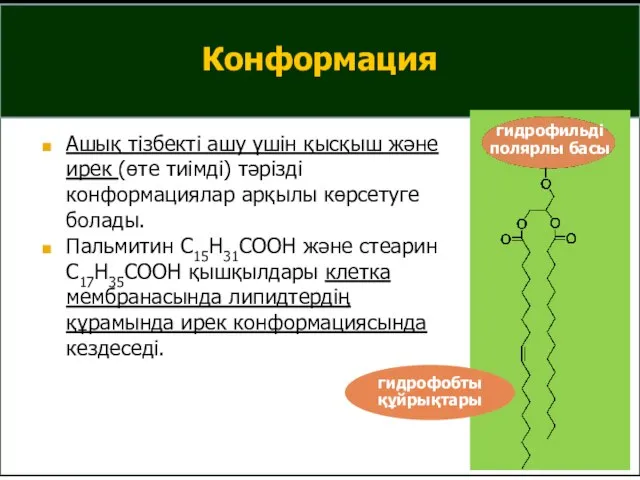
- 25. Конформация Ашық тізбекті ашу үшін қысқыш және ирек (өте тиімді) тәрізді конформациялар арқылы көрсетуге болады. Пальмитин
- 26. Электртерістілігі (ЭТ) Органикалық қосылыстардың құрамындағы элементтердің электртерістілігі, яғни атомдарды өзара байланыстыратын валенттік электрондарды тарту қабілеті әртүрлі
- 27. Электртерістірігі Америка химигі Лайнус Полинг атомдардың электртерістірігінің сандық сипаттамасын (Полинг қатары) ұсынды. Электртерістілігі әртүрлі атомдар байланысқан
- 28. Полярлануы Байланыстың полярлануы, байланыс электрондарының сыртқы электр өрісінің әсерінен ығысу мөлшері. Полярлануына қарай π - байланыс
- 29. Электрондық эффектілер Барлық молекула құратын атомдар байланыста болады және өзара бірімен әсерлесуді сезінеді. Бұл әсерлер электрондық
- 30. 1. Индуктивті эффект бұл орынбасушының әсерінен электрондар тығыздығының σ - байланыс арқылы берілуі. Индуктивті эффекттің пайда
- 31. Индуктивті эффект Индуктивті эффектіні байланыс бойынша түзу стрелкамен көрсетеді, стрелканың ұшы ЭТ жоғары атомға қарай бағытталады.
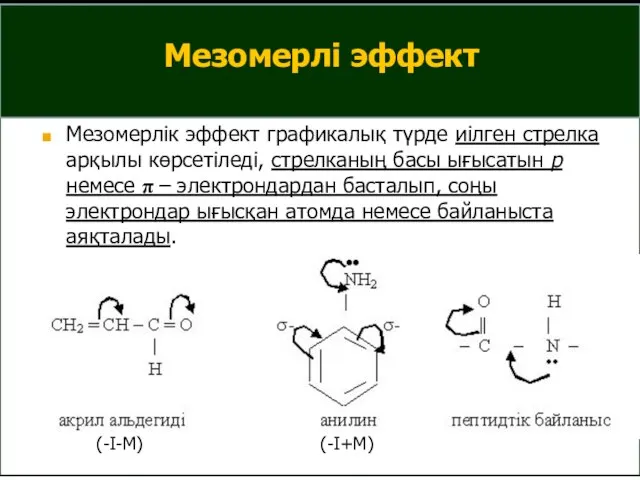
- 32. 2. Мезомерлі эффект (қабысу эффектісі) бұл орынбасушының әсерінен электрондар тығыздығының π- байланыстардың жүйесімен таралуы. Мезомерлі эффект
- 33. Мезомерлі эффект Мезомерлік эффект графикалық түрде иілген стрелка арқылы көрсетіледі, стрелканың басы ығысатын р немесе π
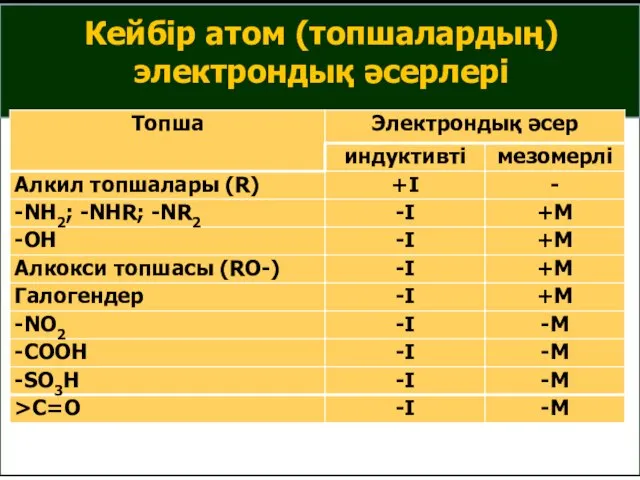
- 34. Кейбір атом (топшалардың) электрондық әсерлері
- 35. Субстрат және реагент Құрамындағы көміртек атомының жаңа байланыстың түзілуі жүретін зат молекуласы, ереже бойынша субстрат (органикалық
- 36. Органикалық реакцияның жіктелуі Органикалық реакциялар бірнеше әдіспен жіктеледі: соңғы нәтижесіне қарай және субстрат пен реагентте байланыстың
- 37. Органикалық реакцияның жіктелуі Субстрат пен реагенттегі байланыстардың сипаты бойынша жіктелуі Субстратта байланыстың үзілуіне қарап барлық химиялық
- 38. Коваленттік байланыстың ыдырауы Гомолититтік ыдырау Радикалдық реакцияларда субстратта байланыс гомолиттік болып бөлінеді және осы кезде бос
- 39. Электрофилді механизм Егер субстраттың реакциялық орталығы электрон тығыздығы жоғары болса (δ-) (электронды жақсы көреді), ал реагент
- 40. Нуклеофильді механизм Субстраттың реакциялық орталығында ішінара оң заряд (δ+) пайда болғанда, реакция нуклеофильді механизм бойынша жүреді.
- 42. Скачать презентацию































 Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Гноеродные (пиогенные) кокки
Гноеродные (пиогенные) кокки Кислород и оксиген
Кислород и оксиген Класс органических соединений фенолы
Класс органических соединений фенолы Нафтены
Нафтены Токсикология пестицидов
Токсикология пестицидов Реакции ионного обмена
Реакции ионного обмена Характеристика элемента по положению в периодической системе
Характеристика элемента по положению в периодической системе Электроповерхностные явления. Строение двойного электрического слоя
Электроповерхностные явления. Строение двойного электрического слоя Статическая биохимия. Ферменты. Механизм действия. Регуляция. Классификация. (Лекция 2)
Статическая биохимия. Ферменты. Механизм действия. Регуляция. Классификация. (Лекция 2) Омега 3
Омега 3 Химия элементов VIA группы. Сера
Химия элементов VIA группы. Сера Аттестационная работа. Задачи на смеси и сплавы
Аттестационная работа. Задачи на смеси и сплавы Возникновение органической химии, как науки
Возникновение органической химии, как науки Углеводы. Глюкоза. Простые эфиры. Димедрол
Углеводы. Глюкоза. Простые эфиры. Димедрол Получение этилена и опыты с ним. (Практическая работа 2)
Получение этилена и опыты с ним. (Практическая работа 2) Презентация по Химии "Жири" - скачать смотреть бесплатно
Презентация по Химии "Жири" - скачать смотреть бесплатно Липиды. Классификация, строение, свойства, биологическая роль
Липиды. Классификация, строение, свойства, биологическая роль Нитраты. Ход исследовательской работы
Нитраты. Ход исследовательской работы Термодинамические возможности получения меди с применением программного комплекса АСТРА-4
Термодинамические возможности получения меди с применением программного комплекса АСТРА-4 Алюминий и его свойства
Алюминий и его свойства Сложные эфиры. Жиры
Сложные эфиры. Жиры Белки. Строение аминокислот
Белки. Строение аминокислот Оксидтер, жіктелуі, аталуы, алу жолдары, химиялық қасиеттері
Оксидтер, жіктелуі, аталуы, алу жолдары, химиялық қасиеттері Кольцевые силикаты
Кольцевые силикаты Периодический закон и периодическая система химических элементов д.и.менделеева в свете учения о строении атома
Периодический закон и периодическая система химических элементов д.и.менделеева в свете учения о строении атома Виробництво Алюмінію Ярова М. Шагієва К.
Виробництво Алюмінію Ярова М. Шагієва К.  Полівінілхлорид
Полівінілхлорид