Содержание
- 2. «Жизнь есть способ существования белковых тел…» (Ф.Энгельс) Белки – это высокомолекулярные органические соединения, представляющие собой биополимер,
- 3. 1.Аминогруппа 3.Радикал ( они разные у всех аминокислот) 2.Карбоксильная группа В аминокислотах выделяют три функциональные группы:
- 4. Образование пептидной связи Аминокислоты могут реагировать друг с другом: карбоксильная группа одной аминокислоты реагирует с аминогруппой
- 5. Структура белка Первичная структура – это полипептидная цепь линейной формы из последовательно соединенных пептидной связью (–
- 6. Структура белка Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку
- 7. Структура белка Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот
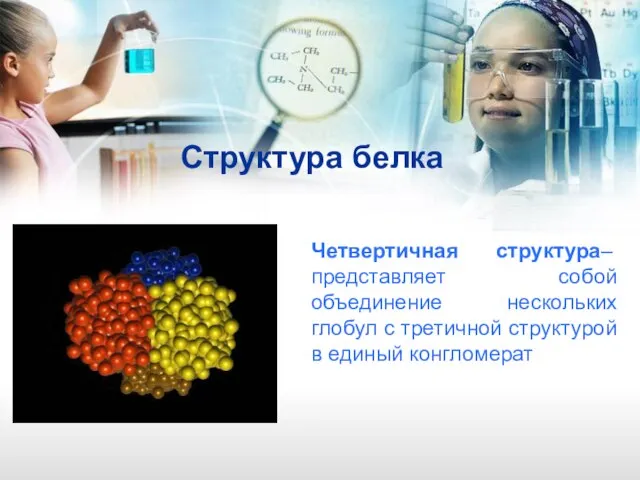
- 8. Структура белка Четвертичная структура– представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат
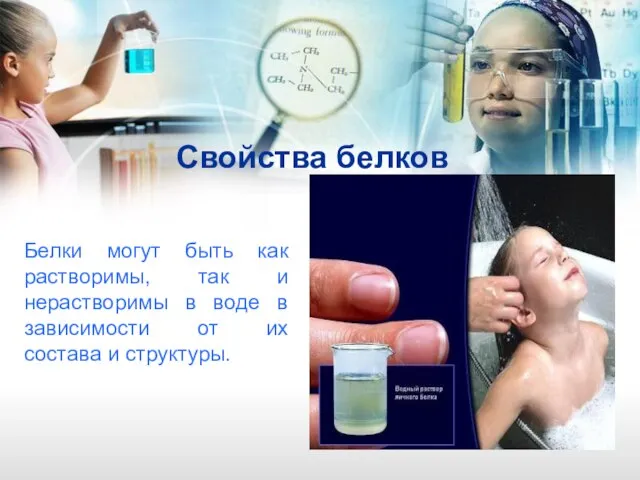
- 9. Свойства белков Белки могут быть как растворимы, так и нерастворимы в воде в зависимости от их
- 10. Свойства белков Водорастворимые белки образуют коллоидные растворы
- 11. Свойства белков При обработке хлоридом натрия белки высаливаются из раствора. Этот процесс обратим.
- 12. Свойства белков Кислоты, щелочи и высокая температура разрушают структуру белков и приводят к их денатурации. Белки
- 13. Свойства белков Поместите кусочек прессованного творога в пробирку и добавьте несколько капель азотной кислоты. Осторожно нагрейте.
- 14. Свойства белков Налейте в пробирку 2 мл яичного белка. Добавьте такой же объем концентрированного раствора гидроксида
- 15. Понятия: Гидролиз белков – разрушение первичной структуры белка. Денатурация – полное разрушение пространственной структуры белка. Обратимая
- 16. Денатурация. Резкое изменение условий, например, нагревание или обработка белка кислотой или щёлочью приводит к потере четвертичной,
- 17. Белки: Простые: Состоят только из аминокислотных остатков Сложные могут включать: - ионы металла (металлопротеиды) -пигмент (хромопротеиды),
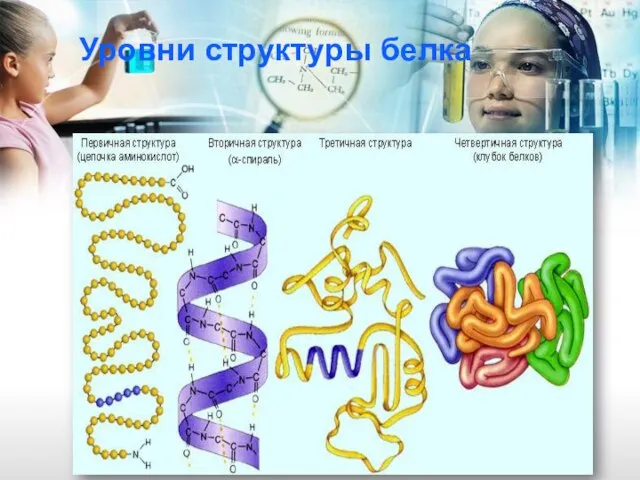
- 18. Уровни структуры белка
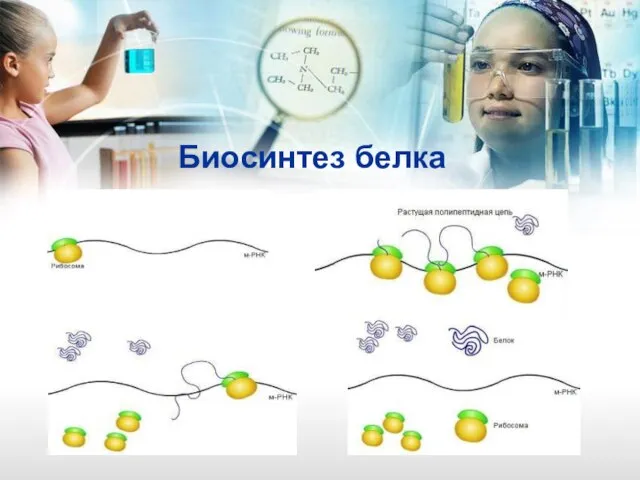
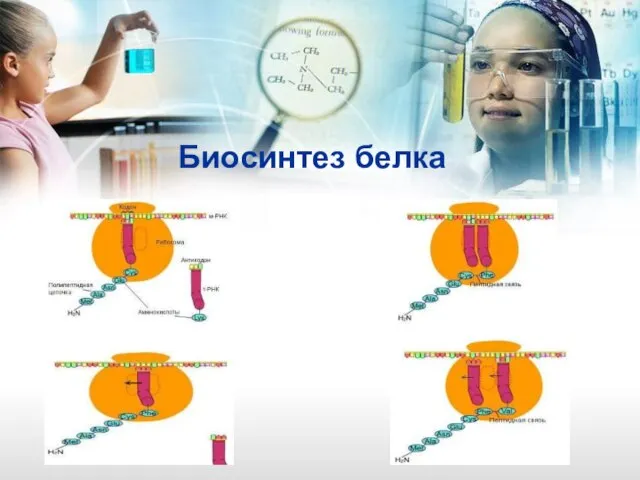
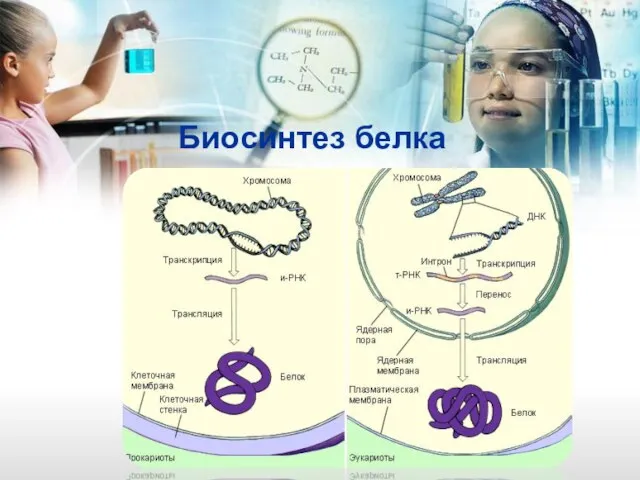
- 19. Биосинтез белка
- 20. Биосинтез белка
- 21. Биосинтез белка
- 22. Функции белков
- 24. Скачать презентацию















 Ксантановая камедь
Ксантановая камедь Презентация по Химии "Коррозии" - скачать смотреть
Презентация по Химии "Коррозии" - скачать смотреть  Крахмал и целлюлоза
Крахмал и целлюлоза "We know it only takes one critically short telomere to make a cell die, so it's clear that the more really short telomeres a person has the faster problems will develop.“ Carol Greider Образ жизни и длина теломер
"We know it only takes one critically short telomere to make a cell die, so it's clear that the more really short telomeres a person has the faster problems will develop.“ Carol Greider Образ жизни и длина теломер Оксиды Na
Оксиды Na Атомы. Молекулы. Химические элементы
Атомы. Молекулы. Химические элементы Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов Аммиак. Строение атома азота
Аммиак. Строение атома азота Материальный баланс аппарата
Материальный баланс аппарата Классификация топлива. Показатели качества топлива (Лекция 1)
Классификация топлива. Показатели качества топлива (Лекция 1) Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Закономерности химических реакций
Закономерности химических реакций Аттестационная работа. Образовательная программа дополнительного образования «Нанотехнологии»
Аттестационная работа. Образовательная программа дополнительного образования «Нанотехнологии» Коррозийное воздействие бензинов а металлы
Коррозийное воздействие бензинов а металлы Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева
Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть
Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть  Техника безопасности для учащихся в кабинете химии
Техника безопасности для учащихся в кабинете химии Циклоалканы. Физические свойства циклоалканов
Циклоалканы. Физические свойства циклоалканов Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности
Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности Как «архангельский мужик … стал разумен и велик». О Михаиле Васильевиче Ломоносове
Как «архангельский мужик … стал разумен и велик». О Михаиле Васильевиче Ломоносове  Периодический закон и ПСХЭ Д.И. Менделеева в свете учения о строении атома
Периодический закон и ПСХЭ Д.И. Менделеева в свете учения о строении атома Технология получения многослойного и малослойного графена
Технология получения многослойного и малослойного графена Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са
Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са Липиды - жиры и жироподобные органические соединения, практически нерастворимые в воде
Липиды - жиры и жироподобные органические соединения, практически нерастворимые в воде Щелочные металлы
Щелочные металлы Распределение лучистой энергии в спектре солнечной радиации до поступления в атмосферу и в спектре абсолютно черного тела
Распределение лучистой энергии в спектре солнечной радиации до поступления в атмосферу и в спектре абсолютно черного тела Презентация по Химии "Строение атома и периодическая система химических элементов" - скачать смотреть
Презентация по Химии "Строение атома и периодическая система химических элементов" - скачать смотреть