Содержание
- 2. ОСАДИТЕЛЬНОЕ ТИТРОВАНИЕ
- 3. В аналитической химии известно много реакций, которые сопровождаются образованием малорастворимых соединений. Из них в количественном анализе
- 4. Осадительное титрование Методы осаждения дают возможность количественно определять соединения, анионы которых образуют осадки с катионами: серебра:
- 5. Осадительное титрование Аргентометрия Ag+ + Hal- → AgHal↓ Меркурометрия Hg22+ + 2Hal- → Hg2Hal2↓
- 6. Аргентометрический титриметрический метод анализа основан на применении в качестве осадителя стандартного раствора серебра нитрата: При приготовлении
- 7. Разбавленные стандартные растворы AgNO3 (0,05М, 0,02 М, 0,01М) готовят последовательным разбавлением 0,1 М стандартного раствора AgNO3.
- 8. Способы определения конечной точки титрования Безындикаторные способы Хлорид-ионы определяют по так называемому методу равного помутнения. Бромид-
- 9. Осадительное титрование Аргентометрия Метод Мора Hal- + Ag+ → AgHal↓ (белый) ПР(AgCl) = 1,78·10-10 S(AgCl) =
- 10. Осадительное титрование Аргентометрия Метод Мора Условия титрования: 2Ag2CrO4↓ + 2Н+ → 4Ag+ + Cr2O7 2- +
- 11. Условия титрования по методу Мора 1. Титрование следует проводить в нейтральной или слабощелочной средах (6,5 ≤
- 12. 2. В растворе должны отсутствовать: катионы (Pb2+, Ba2+, Hg2+ и др.) образующие с анионами индикатора осадки
- 13. Метод Мора применим для определения хлоридов и бромидов, в том числе фармацевтических препаратов в состав которых
- 14. Осадительное титрование Аргентометрия Метод Фольгарда основан на титровании раствора, содержащего ионы серебра стандартными растворами NH4NCS или
- 15. Осадительное титрование Аргентометрия Метод Фаянса-Ходакова HInd ↔ H+ + Ind– Ag+ + I– → AgI↓ первичный
- 16. Приготовление раствора NH4NCS Аммония тиоцианат не является стандартным веществом так как соль гигроскопична. Поэтому из нее
- 17. Условия титрования по методу Фольгарда: Титрование следует выполнять в кислой среде для предотвращения гидролиза индикатора –
- 18. В анализируемом растворе должны отсутствовать: соли ртути (I), (II), реагирующие с NCS- -ионами: Нg22+ + 2NCS-
- 19. Определение ионов Ag+ по методу Фольгарда (прямое титрование) Концентрацию ионов серебра определяют прямым титрованием их стандартным
- 20. Определение анионов по методу Фольгарда (обратное титрование) Для определения анионов используется обратное титрование. Суть определения: к
- 21. При определении хлоридов возникает ошибка за счет нечеткого установления конечной точки титрования. Это связано с протеканием
- 22. Чаще для устранения этой ошибки к анализируемому раствору прибавляют органический растворитель, не смешивающийся с водой (четыреххлористый
- 23. При определение иодидов по методу Фольгарда возникает ошибка за счет протекания окислительно-восстановительной реакции: +e + Fe3+
- 24. По методу Фольгарда можно определять: катионы Ag+ – прямым титрованием; анионы – Cl-, Br-, I-, NCS-
- 25. Осадительное титрование Аргентометрия Метод Фаянса-Ходакова Метод Фаянса-Ходакова основан на прямом титровании анионов (галогенидов, цианидов, тиоцианатов) стандартным
- 26. Условия титрования по методу Фаянса-Ходакова 1. Титрование следует выполнять при определенном значении рН , так как
- 27. 2. Титрование с адсорбционным индикатором следует проводить при большой поверхности осадка. Это достигается, когда осадок присутствует
- 28. Метод Фаянса-Ходакова применим для определения: Cl-, Br-, I-, CN-, NCS- – ионов. Существенным ограничением метода аргентометрии
- 29. Осадительное титрование Меркурометрия Hg22+ + 2Cl- → Hg2Cl2↓ Hg22+ + 2Br- → Hg2Br2↓ Hg22+ + 2I-
- 30. Приготовление стандартного раствора Hg2(NO3)2 Ртути (I) нитрат не является стандартным веществом, так как соль гигроскопична, неустойчива
- 31. В качестве индикаторов используют: красный раствор железа (III) тиоцианата [Fe(NCS)3], его применение основано на том, что
- 32. дифенилкарбазон (1% раствор в 95% спирте), адсорбционный индикатор. Его применение основано на том, что после полного
- 33. Осадительное титрование Меркурометрия Индикаторы: 3Hg22+ + 2[Fe(NCS)3] → 3[Hg(NCS)2] + 2Fe3+ дифенилкарбазон (1%-ный раствор в 95%-ном
- 34. Условия титрования Среда анализируемого раствора должна быть кислая, для этого раствор подкисляют азотной кислотой, чтобы предотвратить
- 35. Определению мешают: сульфат-ионы – их следует устранить, осаждая избытком бария нитрата; ионы железа (III) – их
- 36. Меркурометрический метод анализа имеет преимущество перед аргентометрическим методом: галогениды ртути (I) менее растворимы, чем соответствующие соли
- 37. Методы комплексообразования (комплексиметрия) Меркуриметрическое титрование Hg2+ + 2Cl– → [HgCl2] Индикаторы: Na2[Fe(CN)5NO] → 2Na+ + [Fe(CN)5NO]2–
- 38. Методы комплексообразования (комплексиметрия) Меркуриметрическое титрование Индикаторы: дифенилкарбазид (1) или продукт его окисления – дифенилкарбазон (2): 1
- 39. Методы комплексообразования (комплексиметрия) Меркуриметрическое титрование Определение хлорид- и бромид-ионов: Hg2+ + Cl- → [HgCl]+ [HgCl]+ +
- 40. Методы комплексообразования (комплексиметрия) Меркуриметрическое титрование Определение тиоционат-ионов: 2NCS– + Hg2+ → [Hg(NCS)2] 3Hg22+ + 2[Fe(NCS)3] →3[Hg(NCS)2]
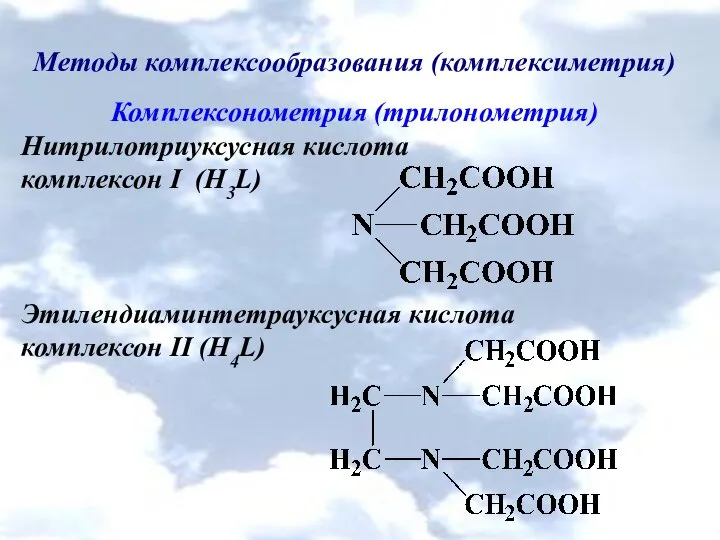
- 41. Методы комплексообразования (комплексиметрия) Комплексонометрия (трилонометрия) Нитрилотриуксусная кислота комплексон І (H3L) Этилендиаминтетрауксусная кислота комплексон ІІ (H4L)
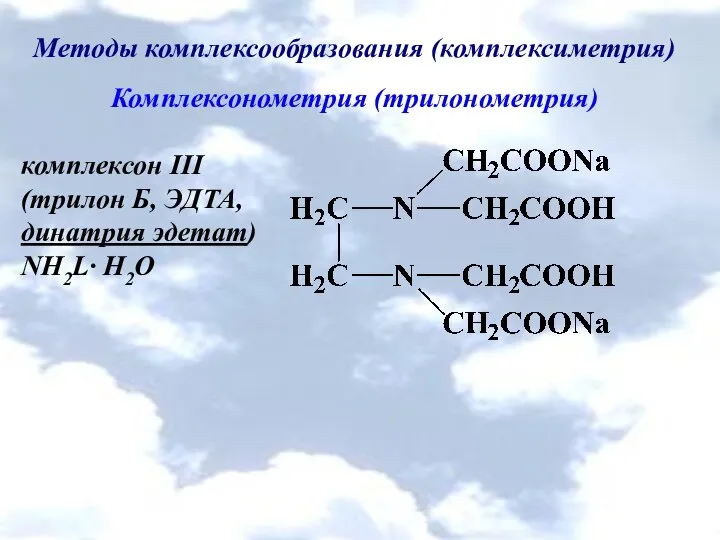
- 42. Методы комплексообразования (комплексиметрия) Комплексонометрия (трилонометрия) комплексон ІІІ (трилон Б, ЭДТА, динатрия эдетат) NH2L∙ H2O
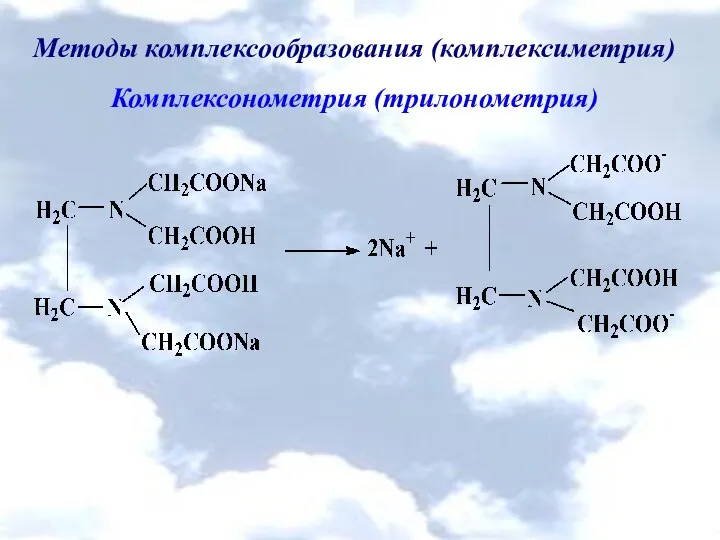
- 43. Методы комплексообразования (комплексиметрия) Комплексонометрия (трилонометрия)
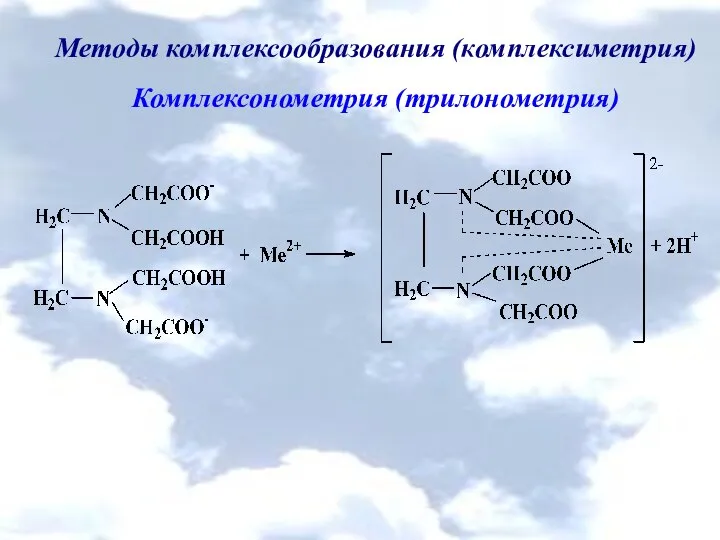
- 44. Методы комплексообразования (комплексиметрия) Комплексонометрия (трилонометрия)
- 45. Методы комплексообразования (комплексиметрия) Комплексонометрия (трилонометрия) H2L2- + Me2+ → [MeL]2- + 2H+ H2L2- + Me3+ →
- 47. Скачать презентацию





























![В качестве индикаторов используют: красный раствор железа (III) тиоцианата [Fe(NCS)3], его](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396319/slide-30.jpg)

![Осадительное титрование Меркурометрия Индикаторы: 3Hg22+ + 2[Fe(NCS)3] → 3[Hg(NCS)2] + 2Fe3+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396319/slide-32.jpg)



![Методы комплексообразования (комплексиметрия) Меркуриметрическое титрование Hg2+ + 2Cl– → [HgCl2] Индикаторы:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396319/slide-36.jpg)



![Методы комплексообразования (комплексиметрия) Комплексонометрия (трилонометрия) H2L2- + Me2+ → [MeL]2- +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396319/slide-44.jpg)
 Растворение как физико-химический процесс. Растворимость. Типы растворов
Растворение как физико-химический процесс. Растворимость. Типы растворов Строение соединения С4Н802
Строение соединения С4Н802 Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля
Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия
Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия Бензол: строение и свойства
Бензол: строение и свойства Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, как серная кислота…» (Д. И. Менделеев)
Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, как серная кислота…» (Д. И. Менделеев) Моделирование химико-технологической системы. Эмпирические, физические, математические методы моделирования
Моделирование химико-технологической системы. Эмпирические, физические, математические методы моделирования План розміщення добрив у польовій сівозміні. (Лабораторна робота 22)
План розміщення добрив у польовій сівозміні. (Лабораторна робота 22) Мел - полезное ископаемое моего села
Мел - полезное ископаемое моего села Побочная подгруппа II группы. Цинк, ртуть и их соединения
Побочная подгруппа II группы. Цинк, ртуть и их соединения Історія відкриття періодичної системи хімічних елементів Д. І. Меделєєва
Історія відкриття періодичної системи хімічних елементів Д. І. Меделєєва Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Химия в сельском хозяйстве.
Химия в сельском хозяйстве.  Вода и другие макронутриенты (органические кислоты, дубильные вещества, пигменты и фитонциды)
Вода и другие макронутриенты (органические кислоты, дубильные вещества, пигменты и фитонциды) Химические реакции
Химические реакции Алмазы. Естественный рост. Искуственое выращивание
Алмазы. Естественный рост. Искуственое выращивание Липиды молока и молочных продуктов. Группы липидов
Липиды молока и молочных продуктов. Группы липидов Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Закон сохранения массы вещества и химические уравнения (8 класс)
Закон сохранения массы вещества и химические уравнения (8 класс) Нефть и способы её переработки
Нефть и способы её переработки Гетероциклы с одним гетероатомом
Гетероциклы с одним гетероатомом Основные понятия и законы химии. Эквивалент. Закон эквивалентов. Закон титрования
Основные понятия и законы химии. Эквивалент. Закон эквивалентов. Закон титрования Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Витаминдер. Майда еритін витаминдер
Витаминдер. Майда еритін витаминдер Состояние электронов в атоме
Состояние электронов в атоме Баксанская нейтринная обсерватория
Баксанская нейтринная обсерватория Соединения химических элементов
Соединения химических элементов Работу выполнили учащиеся 8А класса: Арзамазова Евгения, Максименко Полина, Рахвалова Ангелина Руководитель: учи
Работу выполнили учащиеся 8А класса: Арзамазова Евгения, Максименко Полина, Рахвалова Ангелина Руководитель: учи