Содержание
- 2. Основные понятия химии.
- 3. Химия – это наука о составе, строении, свойствах и превращениях веществ. Вещество – один из видов
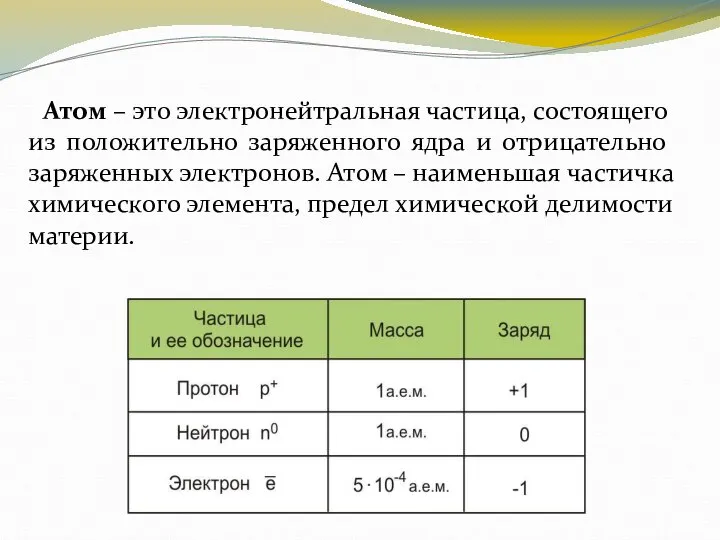
- 4. Атом – это электронейтральная частица, состоящего из положительно заряженного ядра и отрицательно заряженных электронов. Атом –
- 5. Молекула – это отдельная электронейтральная частица, образующаяся при возникновении ковалентных связей между атомами одного или нескольких
- 6. Химический элемент – это совокупность атомов с одинаковым зарядом ядра. Вещества, образованные одним химическим элементом, называют
- 7. Состав веществ. Изменение веществ.
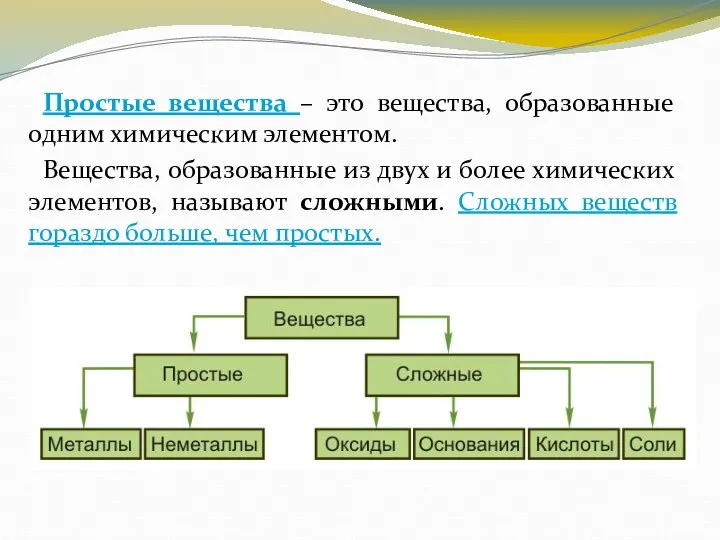
- 8. Простые вещества – это вещества, образованные одним химическим элементом. Вещества, образованные из двух и более химических
- 9. Различают в качественный и количественный состав веществ. Качественный состав – это совокупность химических элементов и (или)
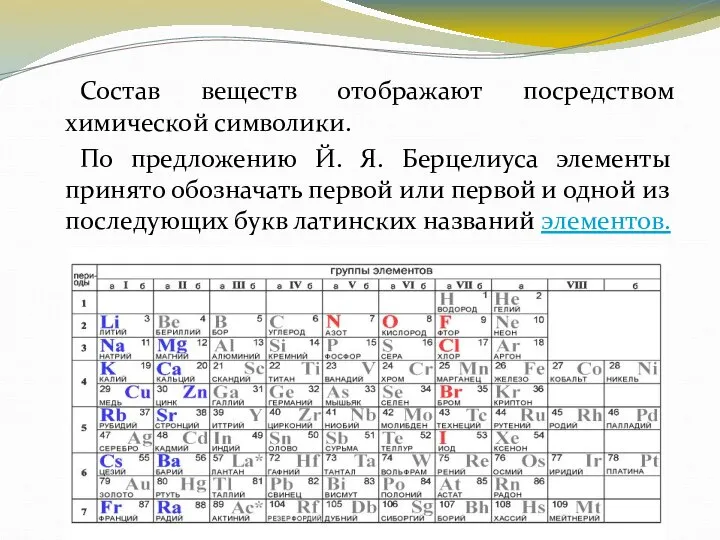
- 10. Состав веществ отображают посредством химической символики. По предложению Й. Я. Берцелиуса элементы принято обозначать первой или
- 11. Химический знак (символ) – несет значительную информацию. Он обозначает название элемента, один его атом, один моль
- 12. Химическая формула – это способ отображения химического состава вещества. Она обозначает название вещества, одну молекулу его,
- 13. Формулы вещества составляют на основании еще одного важнейшего понятия в химии – валентности. Валентность – это
- 14. Относительная атомная масса ( ) химического элемента – это величина, показывающая отношение средней массы атома природной
- 15. Относительная атомная масса – одна из основных характеристик химического элемента. Относительная молекулярная масса ( ) равна
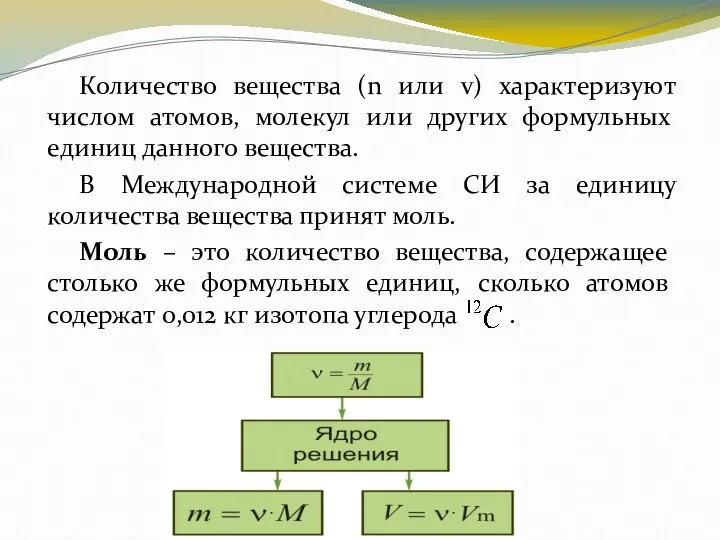
- 16. Количество вещества (n или v) характеризуют числом атомов, молекул или других формульных единиц данного вещества. В
- 18. Массу одного моля называют молярной массой и обозначают буквой М:
- 19. Из этого выражения можно определить число молекул или атомов, содержащихся в одном месте любого вещества, которое
- 20. Основные законы химии
- 21. Закон сохранения массы. Был открыт М. В. Ломоносовым и сформулирован А. Лавуазье: Масса веществ, вступивших в
- 22. Стехиометрия – раздел химии, в котором рассматриваются массовые и объемные соотношения между реагирующими веществами, вывод химических
- 23. Закон постоянства состава вещества. Сформулирован Ж.-Л. Прустом в 1799 г.: Всякое чистое вещество независимо от способа
- 24. Современная формулировка закона постоянства состава вещества таков: Состав соединений молекулярной структуры является постоянным независимо от способа
- 25. Закон Авогадро. Сформулирован А. Авогадро в результате проведения многочисленных экспериментов: В равных объемах различных газов при
- 26. Из закона Авогадро вытекают 2 следствия: Один моль любого газа при одинаковых условиях занимает один и
- 27. Массы двух разных газов, занимающих одинаковый объем при одинаковых условиях, относятся между собой как их молярные
- 28. Найдите относительные молекулярные массы веществ, состав которых описывается формулами: Рассчитайте относительные молекулярные массы медного купороса и
- 29. Сколько молекул содержится в 32 г сернистого газа ? Какова масса молекул аммиака ? Какова масса
- 31. Скачать презентацию
























 Көміртек
Көміртек Оксиды, свойства и способы получения
Оксиды, свойства и способы получения Аттестационная работа. Мини-проекты на уроках химии. 8 класс
Аттестационная работа. Мини-проекты на уроках химии. 8 класс Поделочный камень родонит
Поделочный камень родонит Сурьма Работу выполнила: Ученица 9»Г» класса Ваулина Оксана
Сурьма Работу выполнила: Ученица 9»Г» класса Ваулина Оксана Интернет-тренажеры
Интернет-тренажеры Презентация по Химии "Железо20031" - скачать смотреть бесплатно
Презентация по Химии "Железо20031" - скачать смотреть бесплатно Понятие о спиртах
Понятие о спиртах Пиридин. Строение пиридина
Пиридин. Строение пиридина Железо и его соединения
Железо и его соединения ХІМІЯ В КОСМЕТИЦІ
ХІМІЯ В КОСМЕТИЦІ  Особенности коррозии в морской воде
Особенности коррозии в морской воде Новинки СН старт: июль 2016 Профессиональная химия PRO service
Новинки СН старт: июль 2016 Профессиональная химия PRO service Значение органической химии Кондрашов Алексей | 9 А класс
Значение органической химии Кондрашов Алексей | 9 А класс  Химическая связь и строение органических соединений
Химическая связь и строение органических соединений Способы количественного определения белка
Способы количественного определения белка Введение в биохимию. Значение биохимии для врача. Химия белка
Введение в биохимию. Значение биохимии для врача. Химия белка Нафта, вугілля, природний газ як вуглеводнева сировина. Основні види палива та їх значення в енергетиці країни
Нафта, вугілля, природний газ як вуглеводнева сировина. Основні види палива та їх значення в енергетиці країни Гидролиз солей урок химии (11 класс) частный случай реакции ионного обмена одно из химических свойств солей
Гидролиз солей урок химии (11 класс) частный случай реакции ионного обмена одно из химических свойств солей История появления стекла и все сведения о нем Цель: 1.Узнать о теории происхождения стекла. 2..Изучить состав стекла. 3.Ознакоми
История появления стекла и все сведения о нем Цель: 1.Узнать о теории происхождения стекла. 2..Изучить состав стекла. 3.Ознакоми Презентация по химии Гидролиз
Презентация по химии Гидролиз  Феноли (бензенол)
Феноли (бензенол) Предмет и задачи биохимии. Белки. (Лекция 1)
Предмет и задачи биохимии. Белки. (Лекция 1) Лигандообменные равновесия и процессы. Строение комплексных соединений
Лигандообменные равновесия и процессы. Строение комплексных соединений Основные понятия и законы химии
Основные понятия и законы химии Карбоновые кислоты
Карбоновые кислоты Многоатомные спирты
Многоатомные спирты Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия
Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия