Содержание
- 2. Цели и задачи биохимии Биохимия – дословно «химия жизни» Цель: изучение химических ( т.е. молекулярных) основ
- 3. Применение знаний биохимии в медицине: 1. Решение проблем сохранения здоровья, в том числе проблем рационального питания;
- 4. Белки. Строение, свойства, функции Белки (синоним:протеины; от греч.protos-первый) Белки-высокомолекулярные азотсодержащие биополимеры или сополимеры, имеющие трехмерную пространственную
- 5. 1. Белки. Функции. В организме человека содержится свыше 50000 индивидуальных белков, выполняющих жизненноважные функции. Функции: Специфические
- 6. Белки. Химический состав. Мономер природного белка – альфа- аминокислоты. В составе белков человека – 20 протеиногенных
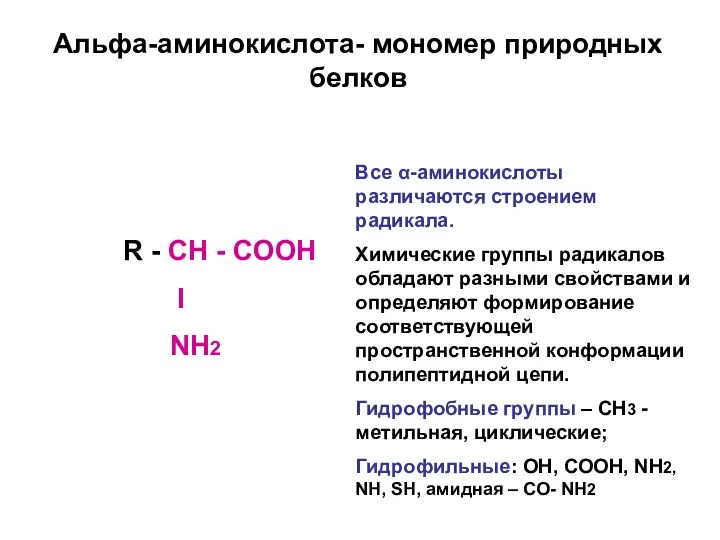
- 7. Альфа-аминокислота- мономер природных белков R - CН - СООН I NН2 Все α-аминокислоты различаются строением радикала.
- 8. Пространственная структура (конформация) Все индивидуальные белки отличаются первичной структурой, конформацией, строением активного центра и функциями. Молекулы
- 9. Пространственная структура (продолжение) Четвертичная (олигомерные белки) - ассоциация нескольких (четное кол-во) протомеров с третичным уровнем (нековалентные
- 10. Структура белка. Домены Для высокомолекулярных белков в структуре характерно наличие доменов. Домены- это участки полипептидной цепи,
- 11. Шапероны. Фолдинг Фолдинг – процесс формирования трехмерной структуры при участии белков шаперонов Шапероны (shaperon - с
- 12. УЧАСТИЕ ШАПЕРОНОВ В ФОЛДИНГЕ БЕЛКОВ РИБОСОМА мРНК синтезирован ный белок ШАПЕРОНЫ 60 БЕЛОК ШАПЕРОНОВЫЙ КОМПЛЕКС нативный
- 13. Центр связывания (активный центр). Взаимодействие белка с лигандами Для осуществления своих функции – напр.каталитической, транспортной, рецепторной,
- 14. Физико-химические свойства белков. Высокая молекулярная масса – варьирует в широких пределах, т.к. варьирует кол-во в молекуле
- 15. Растворимость Факторы влияющие на растворимость: а. рН среды. Изменяя рН среды , меняется степень диссоциации функциональных
- 16. Факторы, влияющие на растворимость б. ионная сила ( концентрация ионов в растворе): Степень раствор. Ионн. сила
- 17. Классификация. Существуют классификации по молекулярной массе, по выполняемым функциям, по локализации в клетке, по локализации в
- 18. Классификация (продолжение) Принцип классификации: Наличие простетической ( небелковой группы): простые белки – состоят только из альфа
- 19. Простые белки На основании условно выработанных критериев – м. м; ам.состав, растворимость, условиях осаждения – простые
- 20. Простые белки ( продолжение) Проламины и глютелины – растительные белки. Особенность – не растворяются в воде.
- 21. Сложные белки (протеиды) Сложные белки в зависимости от химической природы небелкового компонента делят на следующие классы
- 22. Сложные белки (продолжение) Нуклеопротеиды. Небелковый компонент – ДНК, РНК. Связь между положительно заряженными аминокислотных остатков аргинина
- 24. Скачать презентацию




















 Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Классификация минералов
Классификация минералов Водород- зеленое топливо
Водород- зеленое топливо Основы строения сплавов. (3)
Основы строения сплавов. (3) Основы физической органической химии. Сигма-ро анализ
Основы физической органической химии. Сигма-ро анализ Соли, их классификация и свойства
Соли, их классификация и свойства Химическая связь
Химическая связь Смеси и растворы
Смеси и растворы Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Уравнения химических реакций
Уравнения химических реакций Сера в таблице Д.И. Менделеева
Сера в таблице Д.И. Менделеева Основания, их классификация, способы получения и свойства. 8 класс
Основания, их классификация, способы получения и свойства. 8 класс Презентация по Химии "Готовимся к экзамену по химии" - скачать смотреть бесплатно
Презентация по Химии "Готовимся к экзамену по химии" - скачать смотреть бесплатно Химическая связь и ее типы
Химическая связь и ее типы Вдоль по радуге
Вдоль по радуге Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии»
Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии» Презентация Степень окисления
Презентация Степень окисления 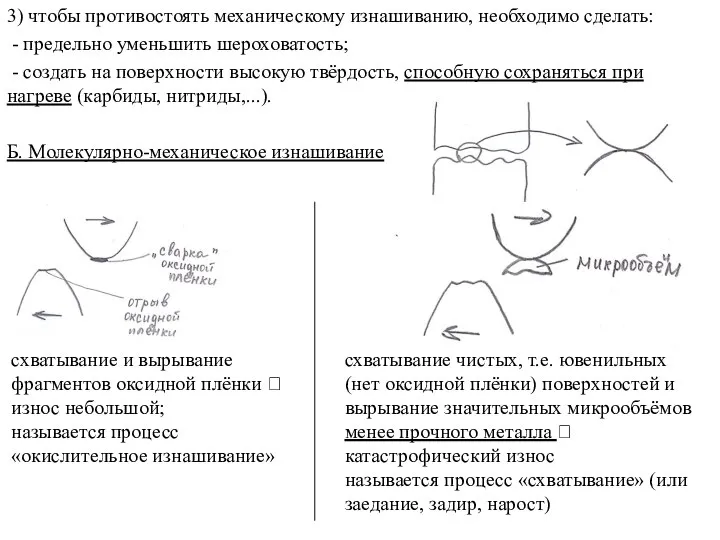 Молекулярно-механическое изнашивание
Молекулярно-механическое изнашивание Терпены и стероиды
Терпены и стероиды Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона
Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона Предмет химии. Основные задачи курса
Предмет химии. Основные задачи курса Горение твердого топлива
Горение твердого топлива Природні й синтетичні органічні сполуки в житті людини
Природні й синтетичні органічні сполуки в житті людини Химия и сельское хозяйство
Химия и сельское хозяйство  Кривые титрования
Кривые титрования Основания и их свойства
Основания и их свойства Аппаратура ионообменных процессов
Аппаратура ионообменных процессов История микроскопа
История микроскопа