Содержание
- 2. План лекции: 1. Методы качественного анализа. 2. Аналитические реакции и их виды. 3. Условия проведения аналитических
- 7. Анализ вещества можно проводить Сухим путем Мокрым путем
- 13. Реактивы, для выполнения аналитических реакций делятся: Специфические Избирательные (селективные) Групповые
- 14. Специфические реактивы образуют характерный осадок или окрашивание только с определённым ионом
- 15. НАПРИМЕР: Реактив К3[Fе(СN)6]- красная кровяная соль образует тёмно-синий осадок только с ионами Fе2+
- 16. 3 FеSO4+ 2K3[Fe(CN)6]→ Fe3[Fe(CN)6]2 ↓ + 3K2SO4 Ионное уравнение: 3Fe2+ + 2[Fe(CN)6]3- → Fe3[Fe(CN)6]2 ↓
- 17. Избирательные (селективные) реактивы реагируют с несколькими ионами, которые могут принадлежать к одной или к разным группам
- 18. Реактив КI реагирует с ионами Рb2+, Аg+, Нg22+(II группа), Нg2+ и Сu2+(VI группы) НАПРИМЕР:
- 19. Групповой реактив вступает в реакцию со всеми ионами данной группы
- 21. Для аналитических реакций важнейшими требованиями являются: специфичность чувствительность
- 22. Специфичность чем меньше количество ионов вступает в реакцию с данным реактивом, тем более специфична данная реакция
- 23. Нр, реакция открытия ионов Fe3+ с реактивом K4[Fe(CN)6] (жёлтая кровяная соль) является специфичной, т.к. благодаря образованию
- 24. Чувствительность чем меньшее количество вещества может быть определено с помощью данного реактива, тем более чувствительна эта
- 25. Условия проведения аналитической реакции: Концентрация раствора Среда раствора Температура
- 26. Кислотно – щелочной метод качественного анализа Разработан в 1947г. советскими учёными: С.Д.Бесковым и О.А.Слизковской
- 27. основан на различной растворимости в воде хлоридов и сульфатов, а также гидроксидов в воде, избытке щелочи
- 28. Классификация катионов
- 29. I группа катионов К+ , Na+ , NH4+ ГРУППОВОЙ РЕАКТИВ ОТСУТСТВУЕТ
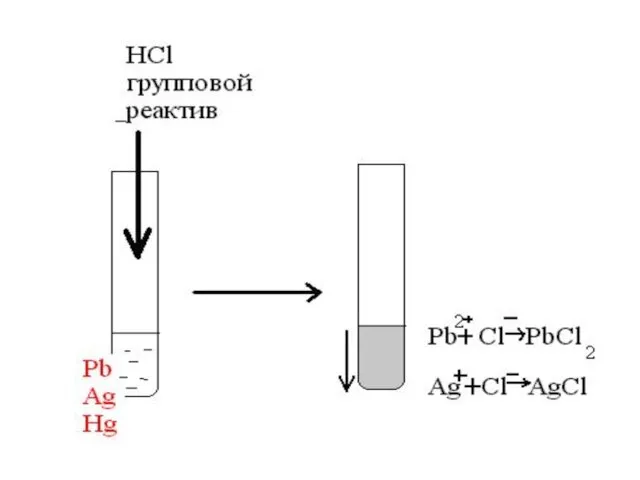
- 30. I I группа катионов Ag+ , Pb2+ , Hg22+ ГРУППОВОЙ РЕАКТИВ HCL СОЛЯНАЯ КИСЛОТА
- 31. I I I группа катионов Ba2+, Ca2+ ГРУППОВОЙ РЕАКТИВ H2SO4 СЕРНАЯ КИСЛОТА
- 32. I V группа катионов Al3+ , Cr3+, Zn2+ ГРУППОВОЙ РЕАКТИВ NaOH избыток ГИДРОКСИД НАТРИЯ
- 33. V группа катионов Fe2+ , Fe3+ , Mn2+ , Mg2+ ГРУППОВОЙ РЕАКТИВ NaOH ГИДРОКСИД НАТРИЯ
- 34. VI группа катионов Cu2+ , Hg2+ ГРУППОВОЙ РЕАКТИВ NH4OH ВОДНЫЙ Р-Р АММИАКАv421.mpg
- 36. Контрольные вопросы: На чем основаны химические методы анализа? Какими свойствами должны обладать аналитические реакции? Какие аналитические
- 37. Cпасибо за внимание!
- 39. Скачать презентацию













![НАПРИМЕР: Реактив К3[Fе(СN)6]- красная кровяная соль образует тёмно-синий осадок только с ионами Fе2+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/489844/slide-14.jpg)
![3 FеSO4+ 2K3[Fe(CN)6]→ Fe3[Fe(CN)6]2 ↓ + 3K2SO4 Ионное уравнение: 3Fe2+ + 2[Fe(CN)6]3- → Fe3[Fe(CN)6]2 ↓](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/489844/slide-15.jpg)





![Нр, реакция открытия ионов Fe3+ с реактивом K4[Fe(CN)6] (жёлтая кровяная соль)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/489844/slide-22.jpg)














 Свойства растворов высокомолекулярных веществ. Набухание
Свойства растворов высокомолекулярных веществ. Набухание Фосфор. Получение. Химические свойства
Фосфор. Получение. Химические свойства Геологические структуры МПИ. Группа доминерализационных структур
Геологические структуры МПИ. Группа доминерализационных структур Ауа. Ауаның құрамы №1 көрсетілім «Ауа мен оттегіде жану реакциясы»
Ауа. Ауаның құрамы №1 көрсетілім «Ауа мен оттегіде жану реакциясы» Кислотоустойчивость пробиотических культур
Кислотоустойчивость пробиотических культур Исторические картины В. И. Сурикова
Исторические картины В. И. Сурикова Химия крови. Диффузия, тургор, осмос в клетке
Химия крови. Диффузия, тургор, осмос в клетке Синтез гидрозолей Cu с использованием солей гуминовых кислот
Синтез гидрозолей Cu с использованием солей гуминовых кислот Основы органической химии. Углеводороды. Алкины
Основы органической химии. Углеводороды. Алкины Щелочные АКБ
Щелочные АКБ Интернет-семинар (вебинар). Методика подготовки к олимпиадам и интеллектуальным турнирам по химии. Часть 1
Интернет-семинар (вебинар). Методика подготовки к олимпиадам и интеллектуальным турнирам по химии. Часть 1 Презентация по Химии "Жёсткость воды" - скачать смотреть
Презентация по Химии "Жёсткость воды" - скачать смотреть  Натрій. Знаходження в періодичній системі і основні характеристики
Натрій. Знаходження в періодичній системі і основні характеристики Рідкі кристали та їх властивості Класифікація та застосування
Рідкі кристали та їх властивості Класифікація та застосування  КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ Мило. Мийні засоби
Мило. Мийні засоби  Природный газ
Природный газ Контейнерная химия: комплексоны, комплексообразование, применение
Контейнерная химия: комплексоны, комплексообразование, применение Моносахариды, глюкоза
Моносахариды, глюкоза Алюминий және оның қосылыстары
Алюминий және оның қосылыстары Общие сведения о катализе и катализаторах
Общие сведения о катализе и катализаторах Основные классы неорганических соединений
Основные классы неорганических соединений Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Жидкостная хроматография
Жидкостная хроматография Редкие химические элементы
Редкие химические элементы Пластмассы, резины и композиционные материалы
Пластмассы, резины и композиционные материалы Кислотность почвы
Кислотность почвы Методическая разработка урока МНОГОАТОМНЫЕ СПИРТЫ
Методическая разработка урока МНОГОАТОМНЫЕ СПИРТЫ