Содержание
- 2. Предмет электрохимии Превращение химической энергии в электрическую Особенности свойств растворов электролитов Электропроводность растворов Процессы электролиза Работа
- 3. Электропроводность растворов Удельная электропроводимость Молярная электрическая проводимость Закон Кольрауша Кондуктометрическое титрование
- 4. Проводники электрического тока Первого рода: все металлы, их сплавы, графит Электронная проводимость При повышении температуры их
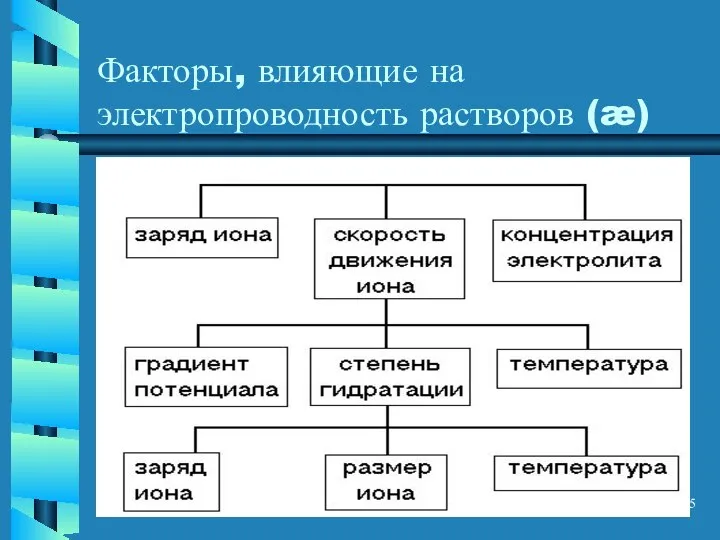
- 5. Факторы, влияющие на электропроводность растворов (æ)
- 6. Заряд иона Чем больше заряд иона и чем больше скорость его перемещения, тем большее количество электричества
- 7. Градиент потенциала (напряженность, Е) При небольшой напряженности электрического поля æ постоянна Начиная с Е = 104
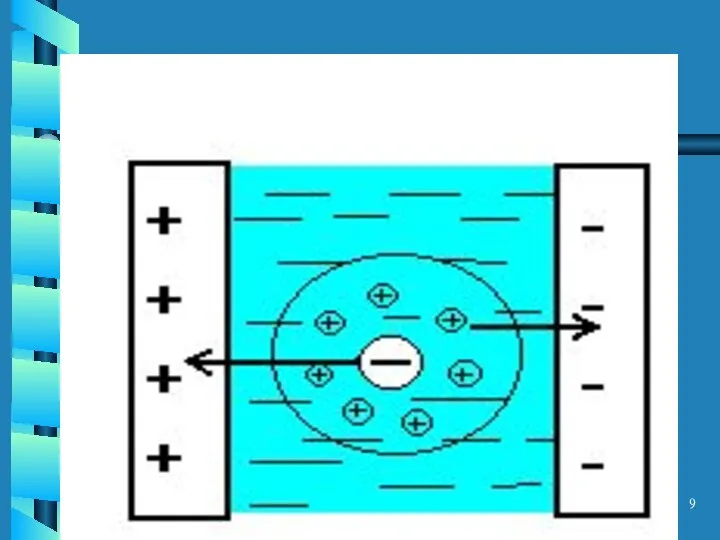
- 8. Электрофоретический эффект Торможение носителей поля за счет того, что ионы противоположного знака под действием электрического поля
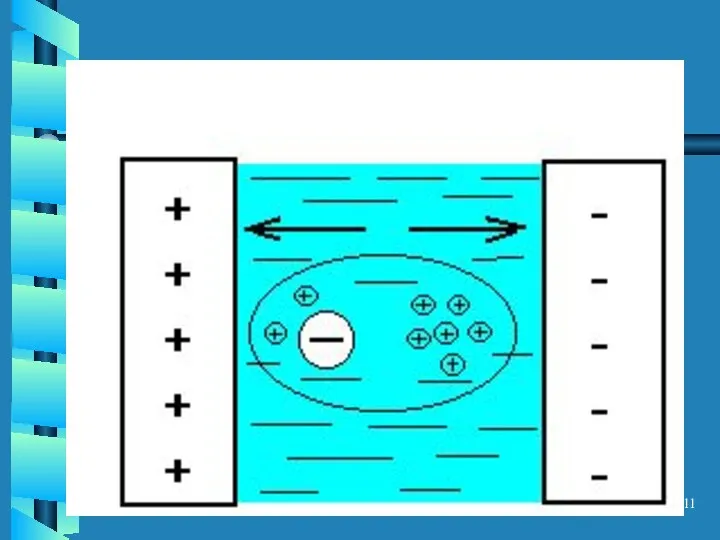
- 10. Релаксационный эффект Торможение носителей в связи с тем, что ионы при движении расположены асимметрично по отношению
- 12. Температура При увеличении температуры скорость движения ионов возрастает Температура усиливает тепловое движение и уменьшает вязкость среды
- 13. Степень гидратации Чем больше гидратация иона, тем меньше его скорость Ион в растворе окружен оболочкой из
- 14. Заряд и размер иона Чем больше заряд иона, тем больше степень гидратации Чем больше диаметр иона,
- 15. Температура Чем выше температура, тем меньше степень гидратации Частичная дегидратация ионов в результате усиления колебательных движений
- 16. Электрическая подвижность (U°) Скорость движения иона в растворе при бесконечном разведении и постоянной температуре при градиенте
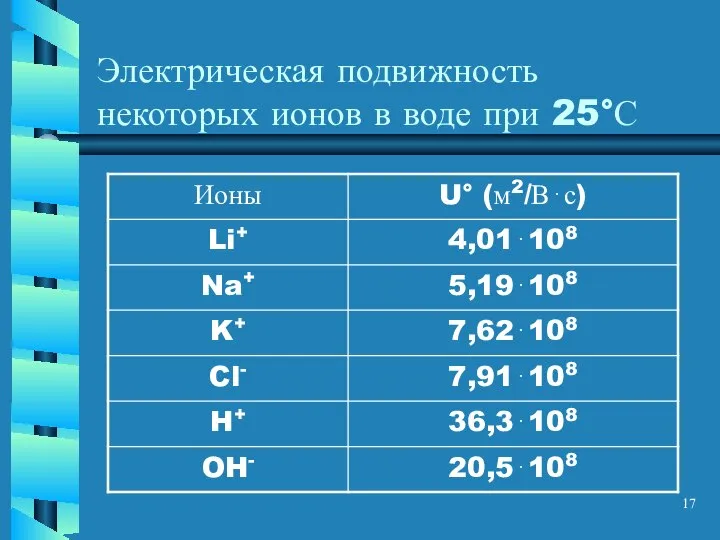
- 17. Электрическая подвижность некоторых ионов в воде при 25°С
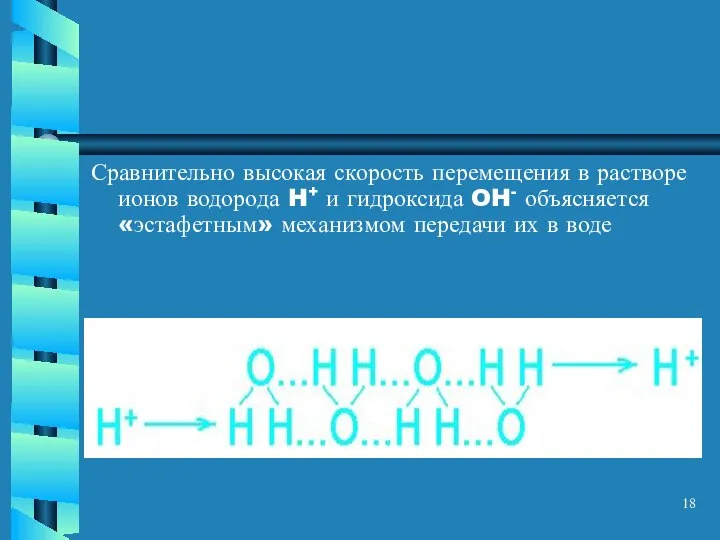
- 18. Сравнительно высокая скорость перемещения в растворе ионов водорода H+ и гидроксида OH- объясняется «эстафетным» механизмом передачи
- 19. Электропроводность Величина обратная сопротивлению проводника тока 1 L = ------- (Ом-1) R l R = ρ
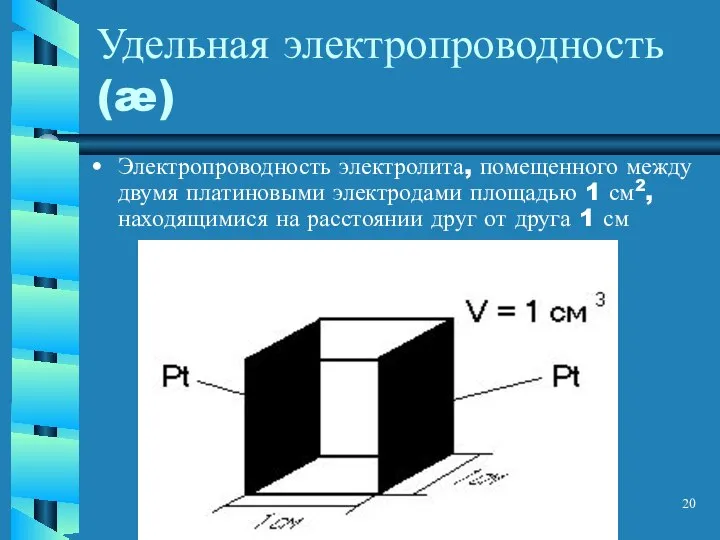
- 20. Удельная электропроводность(æ) Электропроводность электролита, помещенного между двумя платиновыми электродами площадью 1 см2, находящимися на расстоянии друг
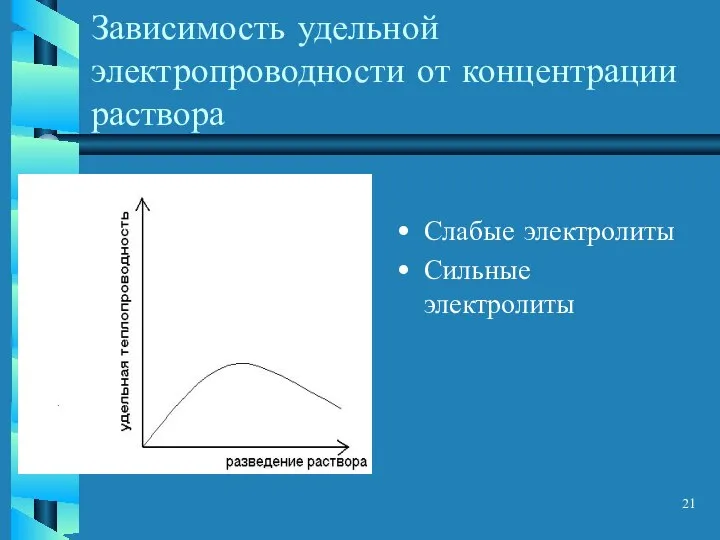
- 21. Зависимость удельной электропроводности от концентрации раствора Слабые электролиты Сильные электролиты
- 22. Молярная электропроводность (λ) Электропроводность раствора электролита, содержащего 1 моль эквивалента электролита, помещенного между двумя платиновыми пластинками,
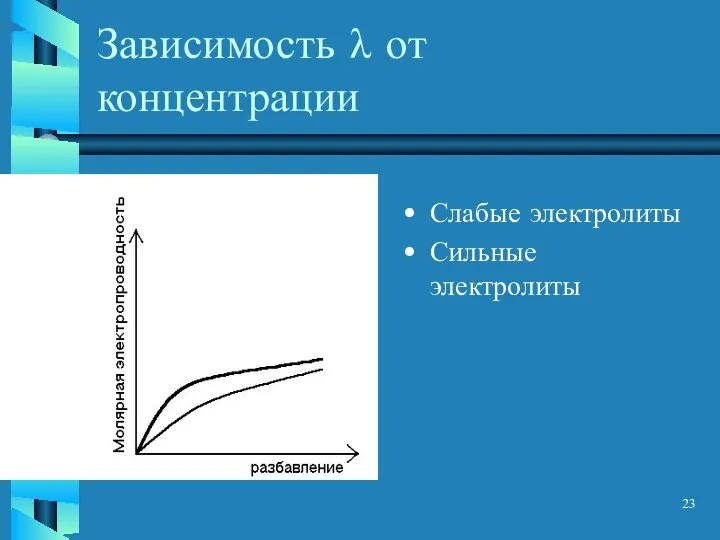
- 23. Зависимость λ от концентрации Слабые электролиты Сильные электролиты
- 24. Связь удельной и молярной электропроводности 1000⋅æ = æ⋅1000⋅V(л) = ------------- (см3) С æ λ = -----------
- 25. Закон Кольрауша При бесконечном разведении раствора электролита катионы и анионы проводят электрический ток независимо друг от
- 26. Математическое выражение закона λ∞ = lК + lА , где lК = U°К ⋅ F lА
- 27. Практическое значение электропроводности Кондуктометрия – метод анализа, основанный на определении электропроводности жидких сред Измерение степени и
- 28. Кондуктометрия = λ∞ ⋅ α λ = ----- λ∞ λ∞ = lК + lА α2⋅С КД
- 29. Ионное произведение воды [H+] = C ⋅ α 1000 C = --------- = 55,5 моль/л 18
- 30. Кондуктометрическое титрование Метод анализа, в котором точка эквивалентности определяется по изменению электропроводности раствора в ходе титрования
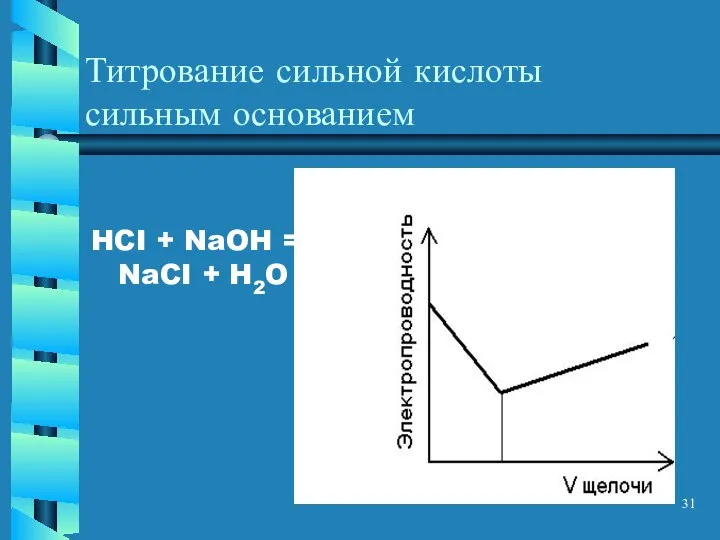
- 31. Титрование сильной кислоты сильным основанием HCI + NaOH = NaCI + H2O
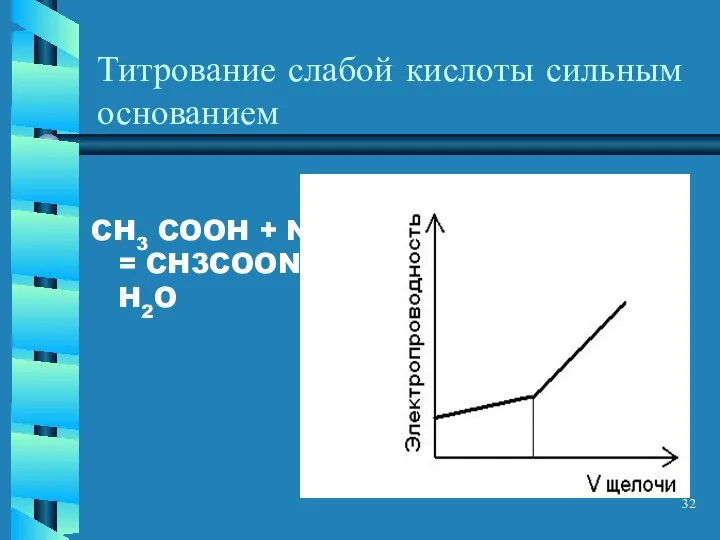
- 32. Титрование слабой кислоты сильным основанием CH3 COOH + NaOH = CH3COONa + H2O
- 33. Зависимость L тканей от частоты переменного тока В норме: С увеличением частоты переменного тока реактивное (емкостное)
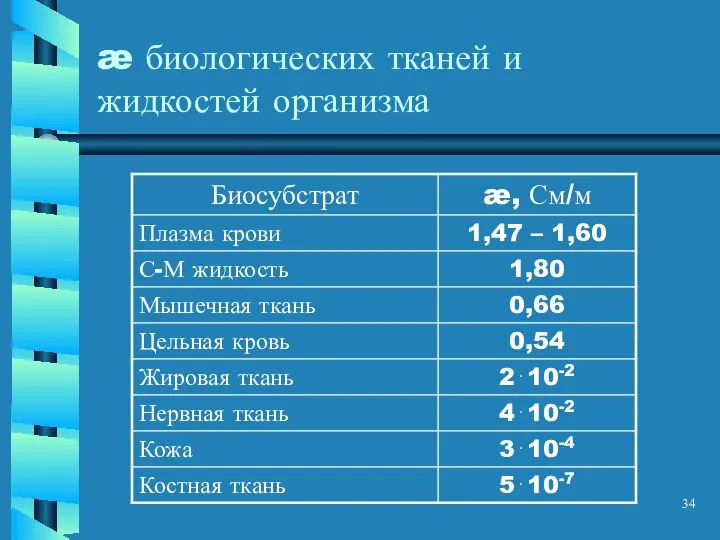
- 34. æ биологических тканей и жидкостей организма
- 36. Скачать презентацию



















![Ионное произведение воды [H+] = C ⋅ α 1000 C =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407505/slide-28.jpg)


 Пластические массы
Пластические массы Строение белков
Строение белков Железо, его характеристики, свойства и соединения
Железо, его характеристики, свойства и соединения Наноматериалы
Наноматериалы Химические формулы
Химические формулы Арены Ароматические углеводороды Непредельные циклические углеводороды
Арены Ароматические углеводороды Непредельные циклические углеводороды М.В.Ломоносов- великий сын России Презентацию подготовила учитель химии МОУ «Куженерская средняя общеобразовательная школа №
М.В.Ломоносов- великий сын России Презентацию подготовила учитель химии МОУ «Куженерская средняя общеобразовательная школа № Презентація уроку «Речовини. Фізичні властивості речовин. Властивості твердих тіл, рідин та газів» Підготувала: учитель хімії ви
Презентація уроку «Речовини. Фізичні властивості речовин. Властивості твердих тіл, рідин та газів» Підготувала: учитель хімії ви Chemistry
Chemistry Химическая связь в твердых телах. Классификация твердых тел по типу химической связи
Химическая связь в твердых телах. Классификация твердых тел по типу химической связи Органическая химия Предельные углеводороды
Органическая химия Предельные углеводороды Расчёты по уравнению реакции
Расчёты по уравнению реакции Використання неметалів та їх сполук , кругообіг неметалів у природі
Використання неметалів та їх сполук , кругообіг неметалів у природі  Применение нанопорошков при получении керамических материалов
Применение нанопорошков при получении керамических материалов Татьяна Леонидовна Быкова, учитель химии, Муниципальное общеобразовательное учреждение «Средняя общеобразовательная школ
Татьяна Леонидовна Быкова, учитель химии, Муниципальное общеобразовательное учреждение «Средняя общеобразовательная школ Амінооцтова кислота. Її будова і властивості
Амінооцтова кислота. Її будова і властивості Технология адсорбционной осушки газа
Технология адсорбционной осушки газа Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение
Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение Идеальный газ в молекулярно-кинетической теории. Среднее значение квадрата скорости молекул
Идеальный газ в молекулярно-кинетической теории. Среднее значение квадрата скорости молекул Относительная атомная и относительная молекулярная масса
Относительная атомная и относительная молекулярная масса Алка́ны
Алка́ны Лекарственные средства, производные барбитуровой кислоты
Лекарственные средства, производные барбитуровой кислоты Підготувала: Учениця 10-Б класу Іщенко Інна
Підготувала: Учениця 10-Б класу Іщенко Інна  Автомобильные пластичные смазки
Автомобильные пластичные смазки Первоначальные химические понятия
Первоначальные химические понятия Элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева
Элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева ОВР в органической химии Автор: Тятин Павел Владимирович, 11М класс, МОУ лицей №6 Руководитель: Дробот Светлана Сергеевна , учит
ОВР в органической химии Автор: Тятин Павел Владимирович, 11М класс, МОУ лицей №6 Руководитель: Дробот Светлана Сергеевна , учит Диагностика магматических горных пород
Диагностика магматических горных пород