Содержание
- 2. Общая характеристика элемента. Железо — элемент побочной подгруппы восьмой группы четвёртого периода Периодической системы химических элементов
- 3. Характеристика железа, как элемента Периодической системы. 4 период, 4 ряд, 8 группа, побочная подгруппа, порядковый номер
- 4. Основные физические свойства железа. Железо — типичный металл, в свободном состоянии — серебристо-белого цвета с сероватым
- 5. Степени окисления Fe0 +2 +2; +3; +3 S, Cu+2 ,HCl(раз) , I2 O2 H2O Cl2 HNO3
- 6. Основные химические свойства железа. С кислородом железо реагирует при нагревании. При сгорании железа на воздухе образуется
- 7. При взаимодействии железа с концентрированнойсерной кислотой (~70%) реакция протекает с образованием сульфата железа(III): 2Fe + 6H2SO4
- 8. При хранении водных растворов солей железа(II) наблюдается окисление железа(II) до железа(III): 4FeCl2 + O2 + 2H2O
- 9. Соединения железа(III) в растворах восстанавливаются металлическим железом: Fe + 2FeCl3 → 3FeCl2. Гидроксид железа(III) Fe(OH)3 проявляет
- 10. 2Fe + 6H2SO4(k)=Fe2(SO4)3 + 3SO2+6H2O Fe+ 6HNO3(k) – ПЕРЕХОДИТ В ПАССИВНОЕ СОСТОЯНИЕ Fe + CuSO4 =
- 11. Взаимодействие железа с разбавленной азотной кислотой даёт разнообразные соединения азота Fe0 + HNO3 (p) = Fe
- 12. Уравнивание реакций. 5Fe0 + 12 HN+5 O3 (p) = 5Fe +3(NO3 )2 + N20 +6 H2
- 13. Железная окалина Fе3О4 Смешанный (геми-) оксид FеО ● Fе2О3 Природный минерал «бурый железняк» Fе3О4 + 8HCl
- 14. Получение феррата (VI) Fе2О3 + КNO3 + KOH → K2FeO4 + КNO2 + H2O Поработайте с
- 15. Получение феррата (VI) Fе2О3 + 3КNO3 + 4KOH → 2K2FeO4 + 3КNO2 +2 H2O 2Fе (+3)
- 16. Получение железа 3CO + Fe2O3 → 2Fe + 3CO2↑ Fe2O3 + 3H2 → 2Fe + 3H2O(при
- 17. Применение железа Железо — один из самых используемых металлов, на него приходится до 95 % мирового
- 18. Уникальные ферромагнитные свойства ряда сплавов на основе железа способствуют их широкому применению в электротехнике для магнитопроводов
- 19. Биологическое значение железа. В живых организмах железо является важным микроэлементом, катализирующим процессы обмена кислородом (дыхания). В
- 21. Скачать презентацию








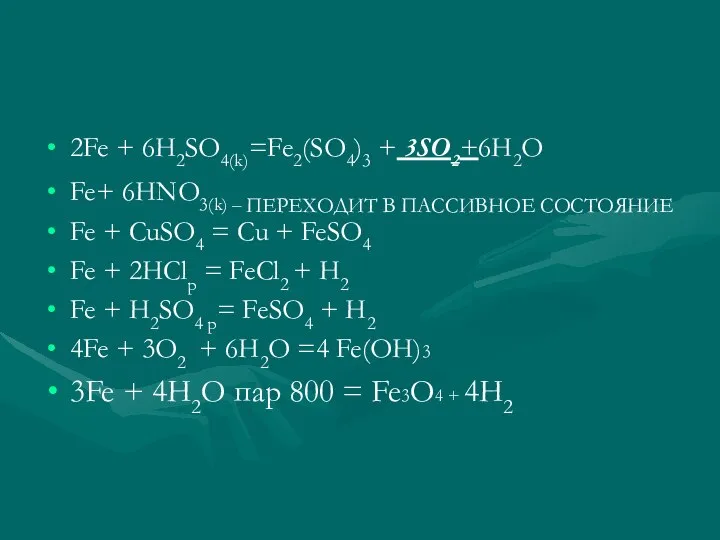









 Газообразное состояние вещества
Газообразное состояние вещества Жер қыртысының заттық және химиялық құрамы
Жер қыртысының заттық және химиялық құрамы Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Углеводороды
Углеводороды Кислоты, их состав и названия
Кислоты, их состав и названия Химический эквивалент
Химический эквивалент Элементы третьего периода, периодической системы Д. И. Менделеева
Элементы третьего периода, периодической системы Д. И. Менделеева Витамины
Витамины Изопроцессы в идеальном газе
Изопроцессы в идеальном газе Элемент металлического происхождения марганец
Элемент металлического происхождения марганец Коррозия металлов
Коррозия металлов В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми
В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми  Естествознание. Раздел II. Химия с элементами экологии Урок по теме:
Естествознание. Раздел II. Химия с элементами экологии Урок по теме: Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата. (Тема 6)
Переваривание углеводов в пищеварительном тракте. Гликолиз. Окислительное декарбоксилирование пирувата. (Тема 6) Дисперсные системы: получение и свойства. Часть 2
Дисперсные системы: получение и свойства. Часть 2 Тяжелые р – элементы -полуметаллы
Тяжелые р – элементы -полуметаллы Химические средства гигиены и косметики
Химические средства гигиены и косметики Химическая связь и ее виды
Химическая связь и ее виды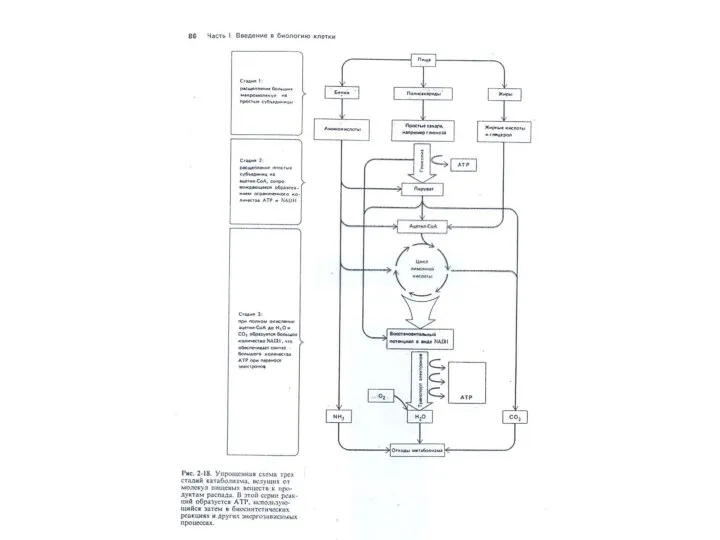 Введение в биологию клетки. (Лекция 6)
Введение в биологию клетки. (Лекция 6) Фізичні та хімічні властивості солей
Фізичні та хімічні властивості солей  Кафедра химической технологии лекарственных веществ (ХТЛВ)
Кафедра химической технологии лекарственных веществ (ХТЛВ) Презентация по химии Переработка нефти
Презентация по химии Переработка нефти Химические свойства водорода H2
Химические свойства водорода H2 Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно
Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно Эмпирические правила
Эмпирические правила Новые пути использования парафиновых углеводородов
Новые пути использования парафиновых углеводородов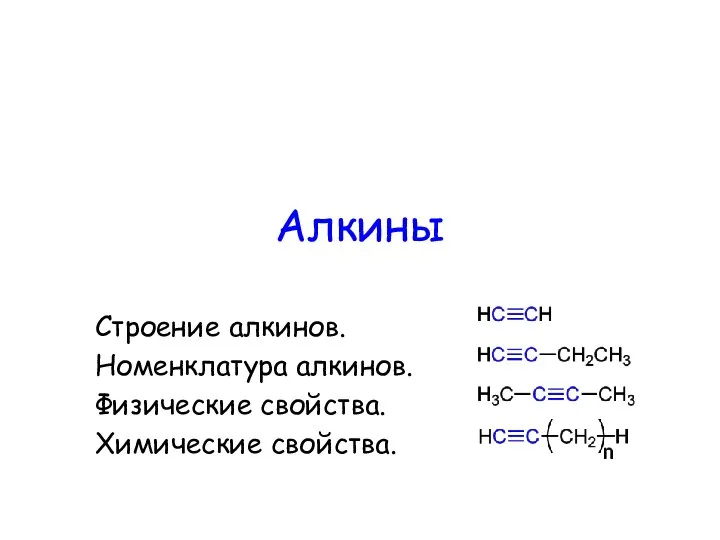 Алкины. Строение алкинов. Номенклатура алкинов. Физические свойства. Химические свойства
Алкины. Строение алкинов. Номенклатура алкинов. Физические свойства. Химические свойства Урок по теме Алюминий .Строение.Свойства. Учитель: Деревянко Н.Г.
Урок по теме Алюминий .Строение.Свойства. Учитель: Деревянко Н.Г.