Содержание
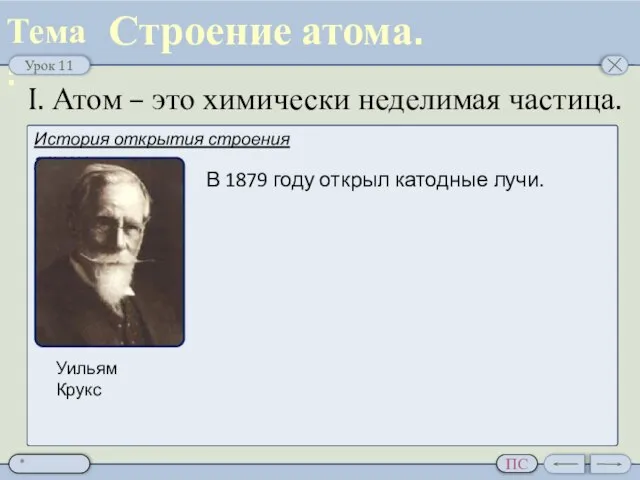
- 2. I. Атом – это химически неделимая частица. Строение атома. История открытия строения атома Уильям Крукс В
- 3. I. Атом – это химически неделимая частица. Строение атома. История открытия строения атома Дж. Томсон. Доказал,
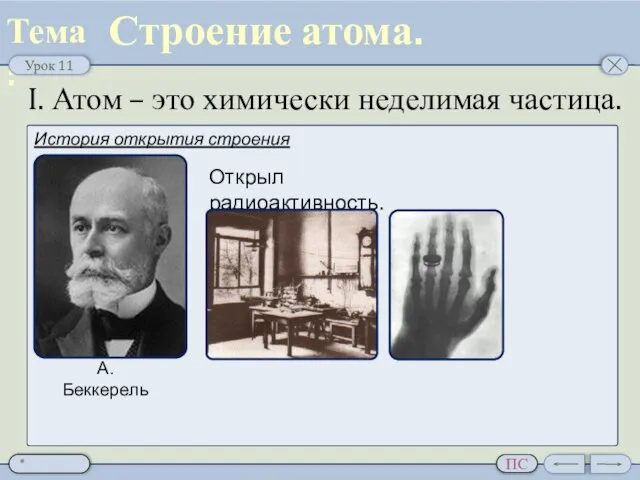
- 4. I. Атом – это химически неделимая частица. Строение атома. История открытия строения атома А. Беккерель Открыл
- 5. I. Атом – это химически неделимая частица. Строение атома. История открытия строения атома Доказал, что атом
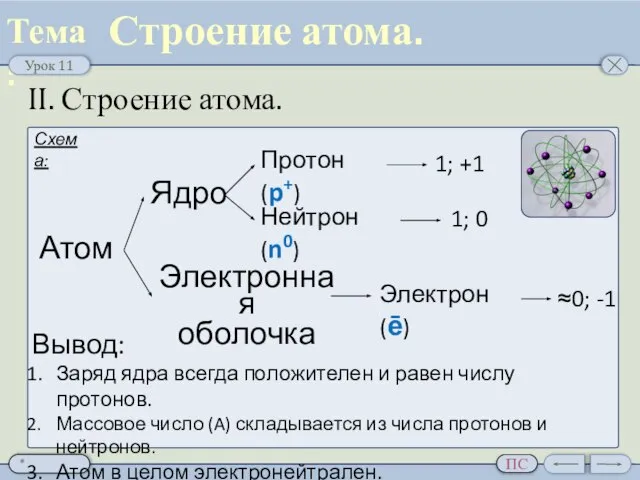
- 6. II. Строение атома. Строение атома. Схема: Атом Ядро Электронная оболочка Протон (p+) Нейтрон (n0) Электрон (ē)
- 7. II. Строение атома. Строение атома. Пример: Характеристика атома фосфора Р +15 31 0 Заряд ядра атома
- 9. Скачать презентацию



 Химический состав клетки. Рибонуклеиновые кислоты, АТФ
Химический состав клетки. Рибонуклеиновые кислоты, АТФ Органическая химия
Органическая химия Химические свойства металлов. Коррозия металлов
Химические свойства металлов. Коррозия металлов Химическое сопротивление алюминий и его сплавов
Химическое сопротивление алюминий и его сплавов Шоу «Юный химик»
Шоу «Юный химик» Бензол и его свойства
Бензол и его свойства Основания
Основания Муравьиная и уксусная кислоты
Муравьиная и уксусная кислоты Ароматические соединения. Лекция 10
Ароматические соединения. Лекция 10 Презентация по Химии "Жиры" - скачать смотреть
Презентация по Химии "Жиры" - скачать смотреть  Введение. Биохимия
Введение. Биохимия Кругообіг води в природі
Кругообіг води в природі  Виробництво та способи виробництва сталі
Виробництво та способи виробництва сталі  Нуклеин қышқылдары. ДНҚ репликациясы
Нуклеин қышқылдары. ДНҚ репликациясы Щелочноземельные металлы
Щелочноземельные металлы Электронные эффекты заместителей. Типы химических реакций
Электронные эффекты заместителей. Типы химических реакций Periodic Table of the Elements
Periodic Table of the Elements Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии
Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии Электроды 1 рода
Электроды 1 рода Колообіг нітрогену в природі
Колообіг нітрогену в природі Хімія для розвитку біо- та нанотехнологій
Хімія для розвитку біо- та нанотехнологій Гетерофункционалды органикалық қосылыстар
Гетерофункционалды органикалық қосылыстар Белоктар – биополимерлер
Белоктар – биополимерлер Алюминий
Алюминий Закономерности протекания химических процессов. Основы химической термодинамики. (Лекция 2)
Закономерности протекания химических процессов. Основы химической термодинамики. (Лекция 2) Химические реакции в неорганической химии
Химические реакции в неорганической химии Производные пиридин-4-карбоновой кислоты
Производные пиридин-4-карбоновой кислоты Биологически важные химические элементы. Неорганические соединения
Биологически важные химические элементы. Неорганические соединения