Содержание
- 2. 1. Простые вещества, газы, оксиды, нерастворимые соединения не диссоциируют (в ионных уравнениях их записывают в молекулярном
- 3. 2. Малорастворимые вещества в левой части уравнения записывают в виде ионов, а в правой части –
- 4. 3. Общая сумма зарядов ионов в левой части уравнения должна быть равна общей сумме зарядов ионов
- 5. 4. Реакции ионного обмена идут до конца, если образуется: а) осадок (↓); б) газ (↑); в)
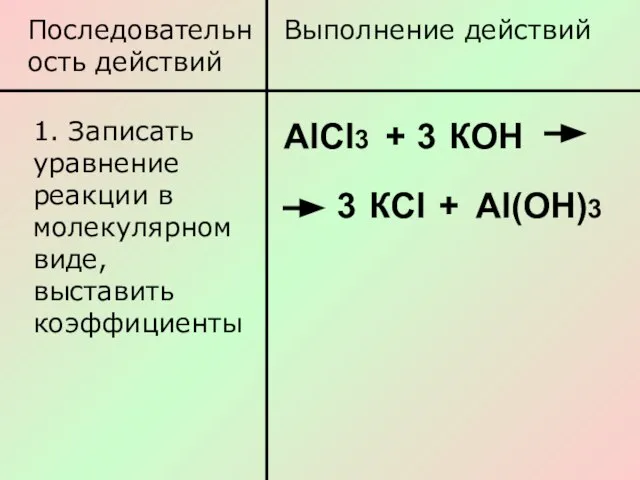
- 6. Последовательность действий Выполнение действий 1. Записать уравнение реакции в молекулярном виде, выставить коэффициенты АlСl3 + 3
- 7. Последовательность действий Выполнение действий 2. Используя таблицу растворимости определить растворимость каждого вещества АlСl3 – р. КСl
- 8. Последовательность действий Выполнение действий 3. Составить полное ионное уравнение, записав электролиты в виде ионов, неэлектролиты в
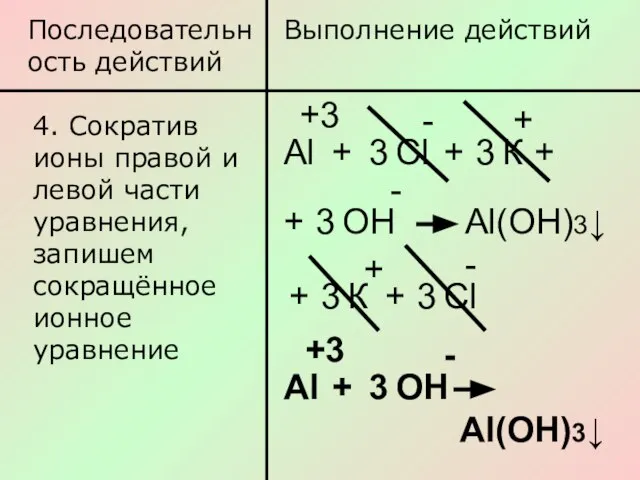
- 9. Последовательность действий Выполнение действий 4. Сократив ионы правой и левой части уравнения, запишем сокращённое ионное уравнение
- 10. Реакций, характеризующих общие химические свойства кислот. 1. Кислоты взаимодействуют с металлами, расположенных в ряду электрохимического ряда
- 11. Последовательность действий Выполнение действий 1. Молекулярное уравнение Zn + Н2SО4 ZnSО4 + Н2 2. Полное ионное
- 12. 2. Кислоты взаимодействуют с оксидами металлов. Молекулярное уравнение СuO + Н2О Н2SО4 CuSО4 + Полное ионное
- 13. Сокращённое ионное уравнение CuО + H Cu + H2O + +2 2 3. Кислоты взаимодействуют с
- 14. H2SO4 + KOH K2SO4 + 2 H2O 2 SO4 + K K + 2 H2O 2
- 15. SO4 H Cu(OH)2 + + + + -2 -2 +2 2 2 SO4 Cu + H2O
- 16. H2SO4 + BaCl2 + BaSO4 HCl ↓ 2 SO4 + Ba + BaSO4 Cl ↓ 2
- 17. H2SO4 + K2CO3 K2SO4 + H2CO3 CO2 + H2O + H + K K + CO2
- 18. Задания для самоконтроля 1. Напишите молекулярные, ионное и сокращенные ионные уравнения реакций между растворами: а) серной
- 19. в) карбоната натрия и нитрата свинца(II) г) нитрата меди(II) и гидроксида натрия д) карбоната калия и
- 21. Скачать презентацию










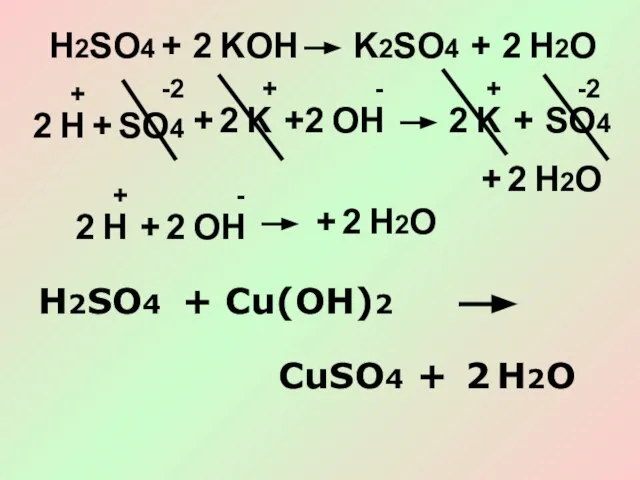

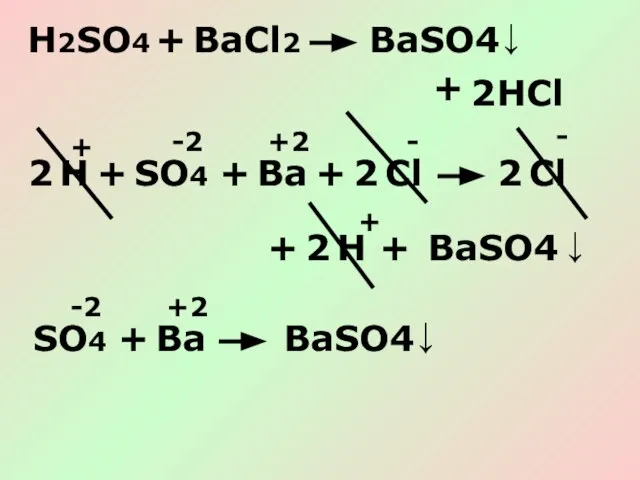
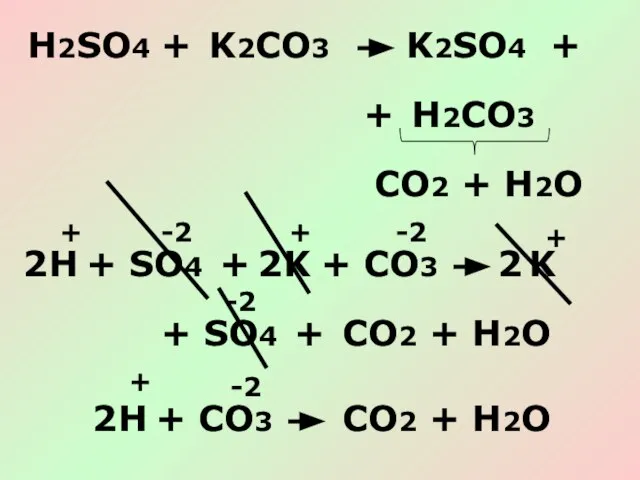


 Требования, особенности, оценка знаний по химии. ОГЭ - 2016
Требования, особенности, оценка знаний по химии. ОГЭ - 2016 Смазывающие вещества
Смазывающие вещества Водородная связь
Водородная связь Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены
Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований
Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі
Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі Практическая работа по химии. Строение пламени
Практическая работа по химии. Строение пламени Эндогенная серия. Вулканогенно-осадочная группа
Эндогенная серия. Вулканогенно-осадочная группа Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД) Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп
Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп “Проценты”, “Массовая доля” при решении задач. Интегрированный урок химии и математики
“Проценты”, “Массовая доля” при решении задач. Интегрированный урок химии и математики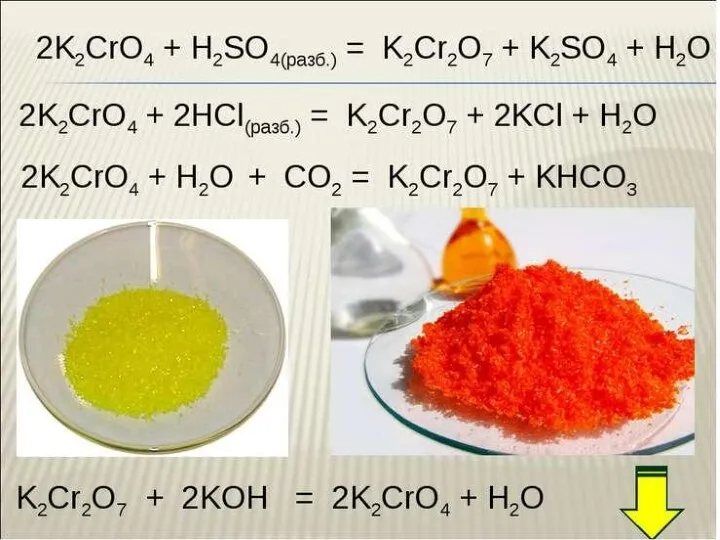 Хром. Соединения хрома
Хром. Соединения хрома История изучения структуры белка Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру
История изучения структуры белка Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен
Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен Алкалоиды, как лекарственные вещества. Источники получения. Методы установления строения. Классификация. (Тема 9)
Алкалоиды, как лекарственные вещества. Источники получения. Методы установления строения. Классификация. (Тема 9) Типы изомерии
Типы изомерии Синтетические моющие средства
Синтетические моющие средства Кадмий (Cadmium)
Кадмий (Cadmium) Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян
Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян Химия и физика полимеров. Курс лекций
Химия и физика полимеров. Курс лекций Строение вещества. Химические элементы
Строение вещества. Химические элементы Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны
Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны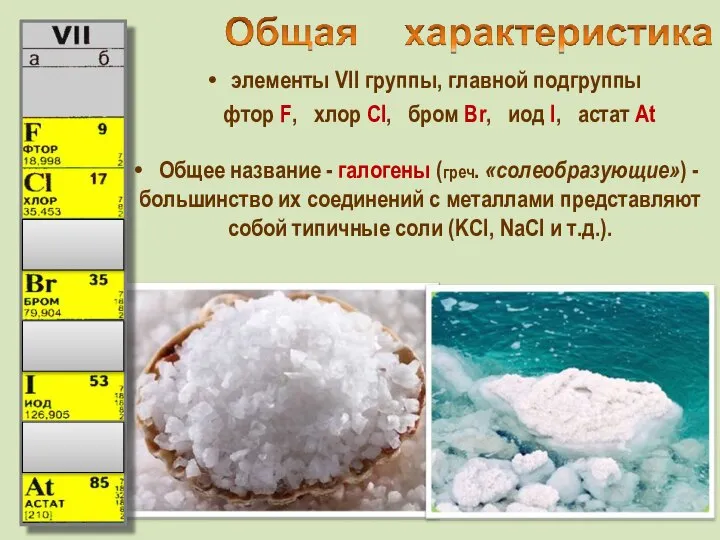 Элементы VII группы
Элементы VII группы Уроки зельеварения. Задача 6
Уроки зельеварения. Задача 6 Основные положения МКТ МКТ- молекулярно-кинетическая теория
Основные положения МКТ МКТ- молекулярно-кинетическая теория  Промышленное получение аминокислот и их применение в медицине и диетологии
Промышленное получение аминокислот и их применение в медицине и диетологии Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия
Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия Физическая и коллоидная химия
Физическая и коллоидная химия