Содержание
- 2. Произведение растворимости (ПР или Ks)
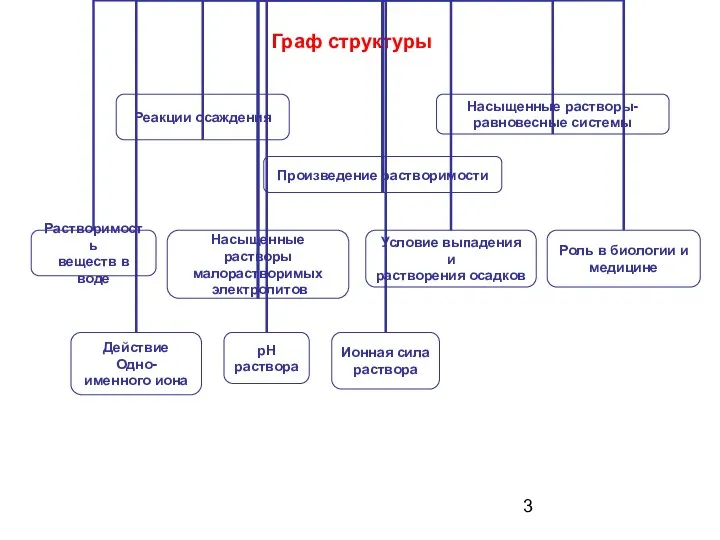
- 3. Граф структуры
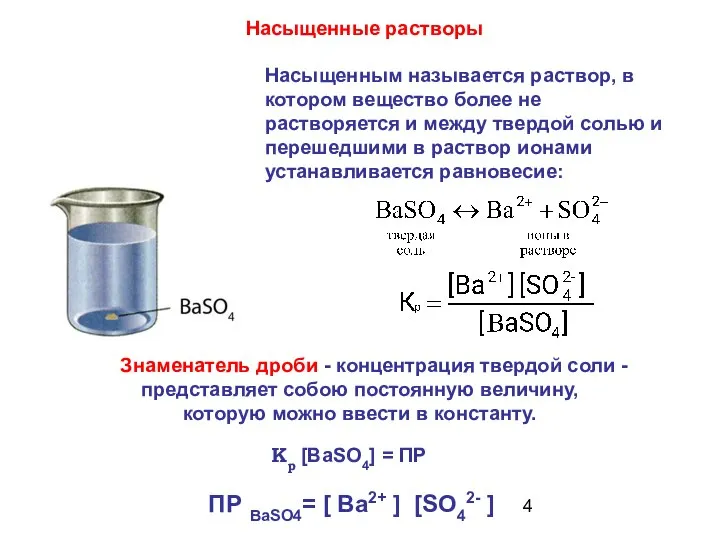
- 4. Знаменатель дроби - концентрация твердой соли - представляет собою постоянную величину, которую можно ввести в константу.
- 5. Если трудно растворимое вещество содержит два или несколько одинаковых ионов, концентрации этих ионов должны быть возведены
- 6. Чем меньше ПР, тем хуже растворимо вещество!
- 7. Использование произведения растворимости (ПР или Ks) 1. Для сравнения растворимости веществ (s) 2. Для прогнозирования выпадения
- 8. 3. Для установления последовательности выпадения осадка ( чем меньше ПР, тем раньше выпадает осадок!!!) ПР (AgCl)
- 9. 5. Для расчета растворимости солей. Рассчитать растворимость хлорида серебра, если ПР (AgCl) =1,8∙10-10 S S S
- 10. Рассчитать растворимость фосфата кальция, если S 3 S 2 S
- 11. NB! При добавлении к насыщенному раствору малорастворимого электролита раствора сильного электролита, не имеющего с ним общих
- 12. Значение ПР в медицине 1. Образование костной ткани: В поверхностных слоях кости образуется некоторое количество аморфного
- 13. При небольшом повышении содержания Н+ кость начинает растворяться, отдавая вначале катионы кальция: При большей кислотности среды
- 14. 2. Защита от кариеса: В полости рта в результате жизнедеятельности микробов образуются достаточно сильные кислоты: пировиноградная,
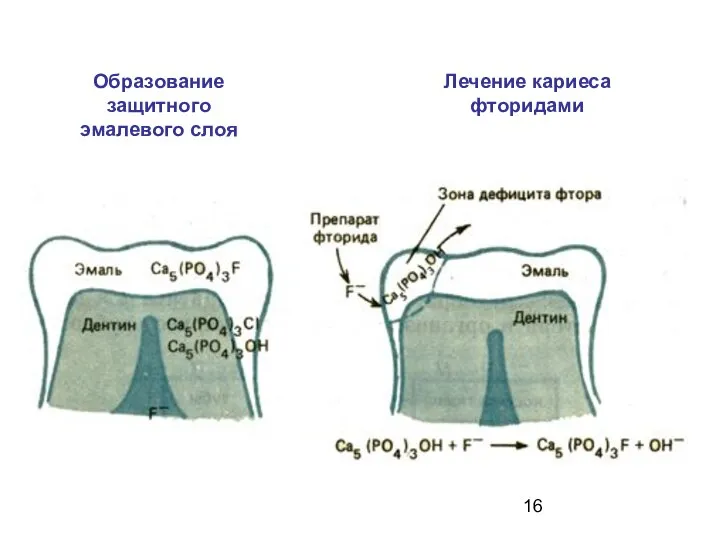
- 15. Замена гидроксид-аниона на фторид-анион значительно повышает твердость и устойчивость зубной эмали к растворению.
- 16. Образование защитного эмалевого слоя Лечение кариеса фторидами
- 17. 3. Рахиты различной этиологии: Бериллиевый рахит (бериллиоз) - вытеснение ионов Са2+ ионами Ве2+ из костей и
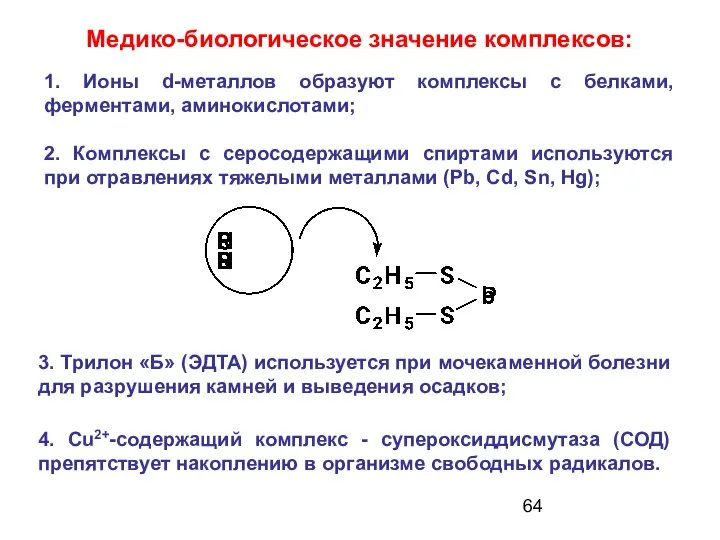
- 18. 4. Детоксикация при отравлениях: Отравление тяжелыми металлами (Pb, Hg, Cd) приводит к блокаде –SH-групп белковых фрагментов.
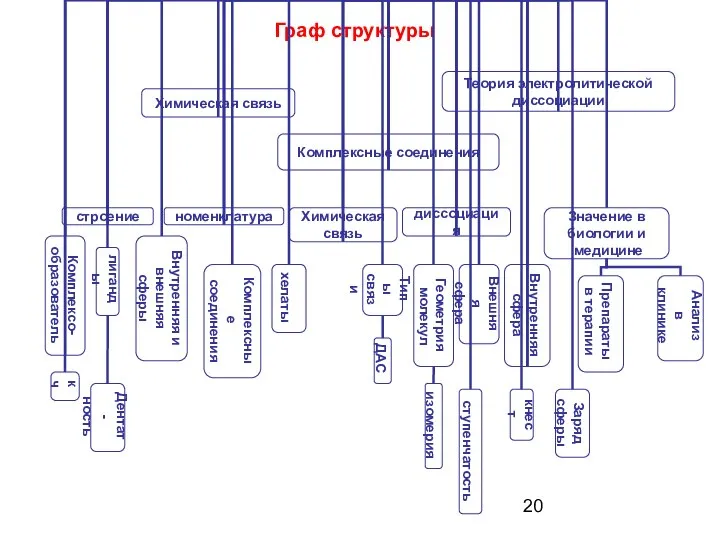
- 19. «Строение комплексных (координационных) соединений. Устойчивость в растворах»
- 20. Граф структуры
- 21. Комплексные соединения - устойчивые химические соединения сложного состава, в которых имеется хотя бы одна связь, образованная
- 22. K4[Fe(CN)6] Fe2+ – центральный ион–комплексообразователь – акцептор электронов ( кислота Льюиса) CN- – лиганды внутренней сферы
- 23. 3. По Льюису ЛЬЮИС Гилберт Ньютон (23.10 1875–23.03 1946) Во время первой мировой войны – полковник
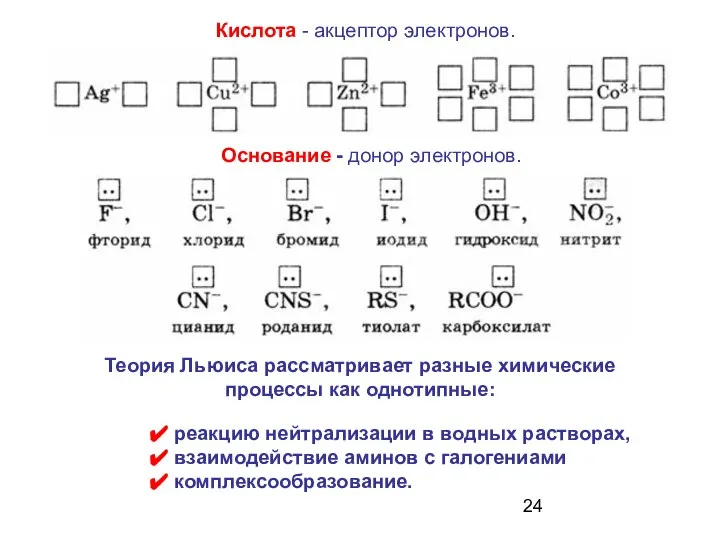
- 24. Кислота - акцептор электронов. реакцию нейтрализации в водных растворах, взаимодействие аминов с галогениами комплексообразование. Основание -
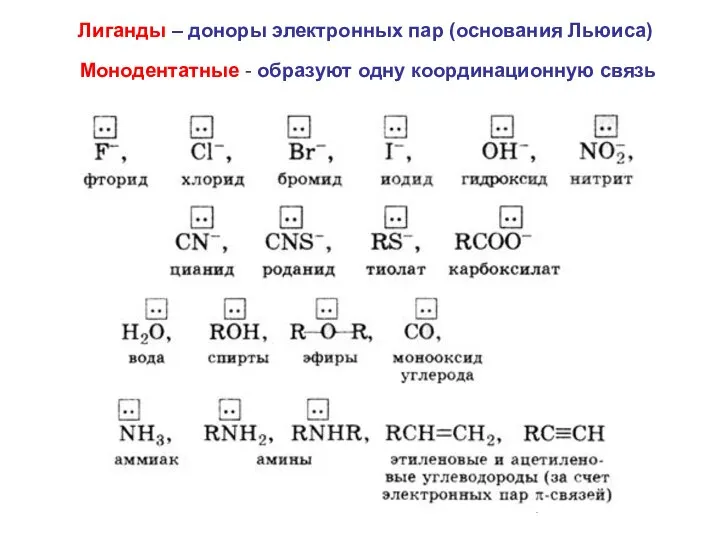
- 25. Лиганды – доноры электронных пар (основания Льюиса) Монодентатные - образуют одну координационную связь
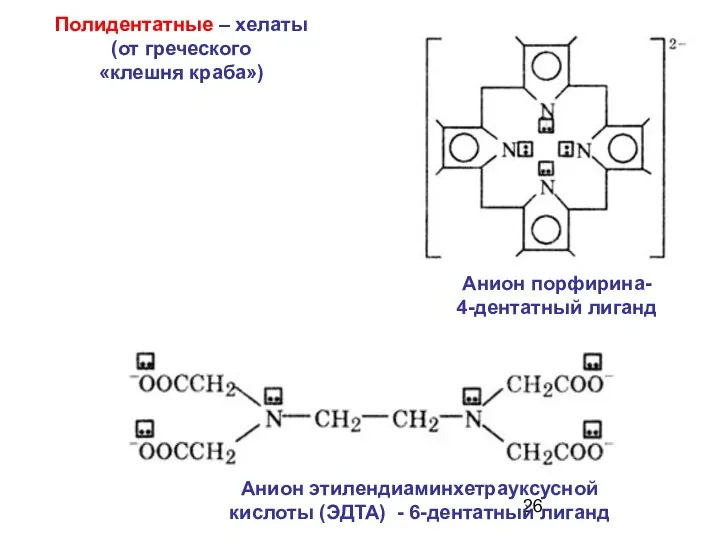
- 26. Анион порфирина- 4-дентатный лиганд Анион этилендиаминхетрауксусной кислоты (ЭДTA) - 6-дентатный лиганд Полидентатные – хелаты (от греческого
- 27. Большинство комплексных соединений, как и сами ионы металлов, имеют окраску
- 28. КЛАССИФИКАЦИЯ 1. По заряду внутренней сферы: - катионного типа: [Ag(NH3)2]Cl, [Cu(NH3)4]SO4 - анионного типа: K4[Fe(CN)6], K2[HgI4]
- 29. 4. По природе лигандов внутренней сферы: ацидокомплексы (анионы кислотных остатков): K3[Fe(CN)6], K2[HgI4] аквакомплексы: [Al(H2O)6]Cl3 аммиакаты: (разлагаются
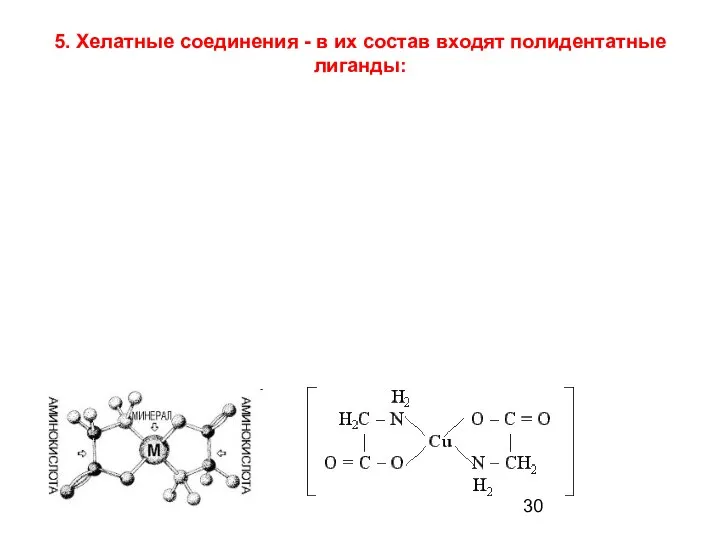
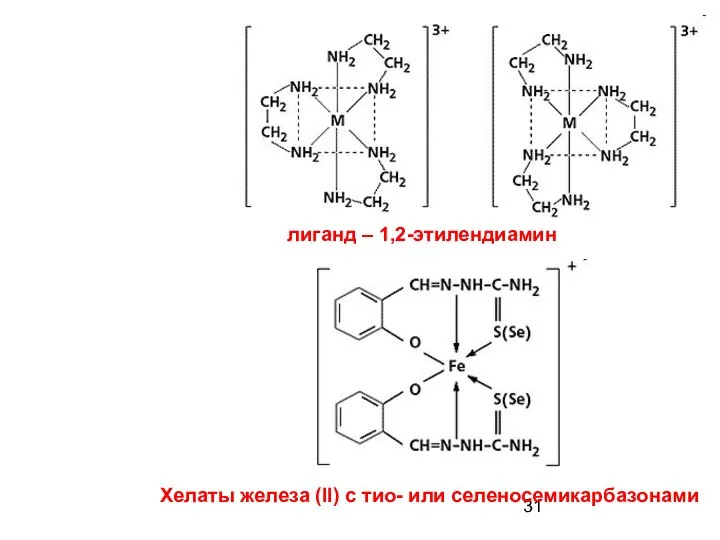
- 30. 5. Хелатные соединения - в их состав входят полидентатные лиганды:
- 31. Хелаты железа (ll) с тио- или селеносемикарбазонами лиганд – 1,2-этилендиамин
- 32. 2. Координационная изомерия - различное распределение комплексообразователей или лигандов между комплексными катионами и анионами: [Co(NH3)6][Cr(CN)6] [Cr(NH3)6][Co(CN)6]
- 33. [Сr(Н2О)6]Сl3 [Сr(Н2О)4Сl2]Сl·2Н2О сине-серая темно-зеленая 3. Гидратная изомерия определяется характером связей молекул воды, входящих в состав комплекса
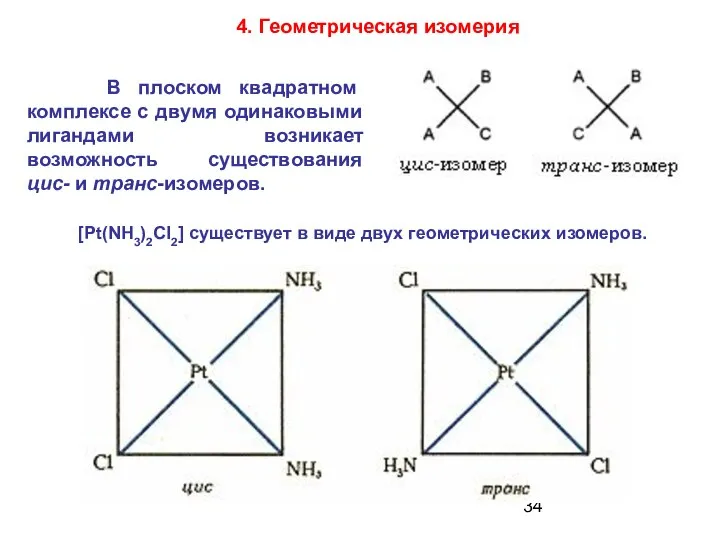
- 34. В плоском квадратном комплексе с двумя одинаковыми лигандами возникает возможность существования цис- и транс-изомеров. 4. Геометрическая
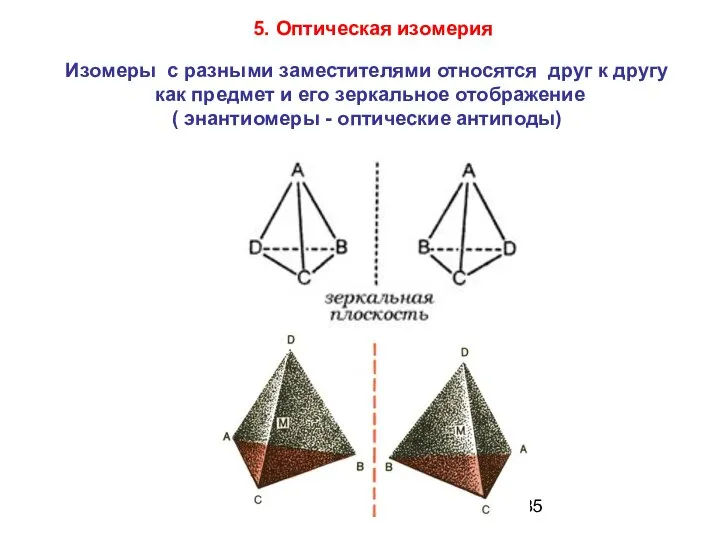
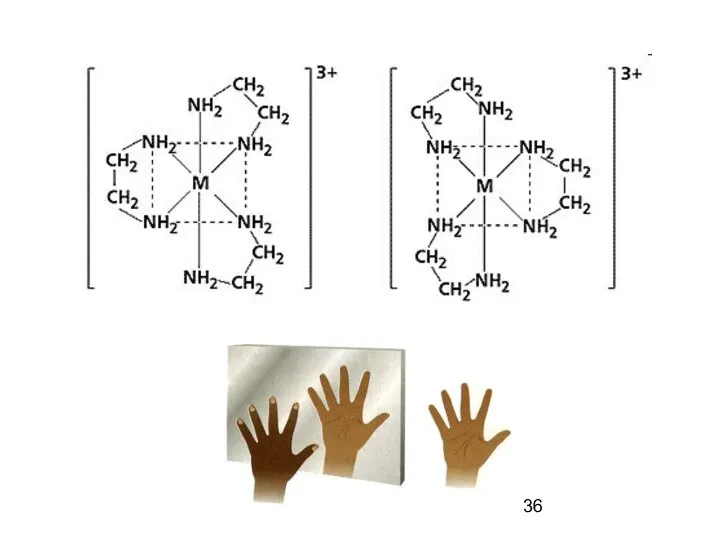
- 35. Изомеры с разными заместителями относятся друг к другу как предмет и его зеркальное отображение ( энантиомеры
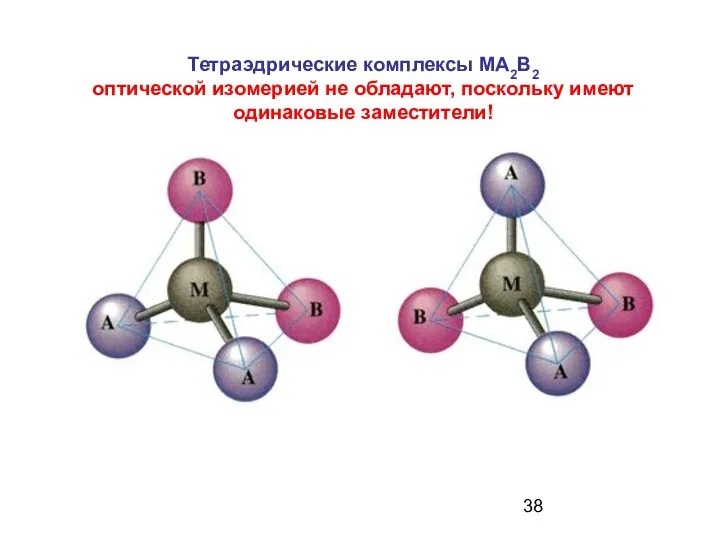
- 37. Характерная их особенность - способность вращать плоскость поляризации плоскополяризованного луча.
- 38. Тетраэдрические комплексы MA2B2 оптической изомерией не обладают, поскольку имеют одинаковые заместители!
- 39. Номенклатура [Ag(NH3)2]Cl – хлорид диамминсеребра [Cu(NH3)4]SO4 – сульфат тетраамминмеди (II) [Pt(NH3)2Cl2] – дихлориддиамминплатина (II)
- 40. Получение комплексных соединений:
- 41. Строение комплексных соединений: 1. [Ag(NH3)2]Cl Ag+ KLM 4s2 4p6 4d10 5s0 5p0
- 42. 1. [Ag(NH3)2]Cl (к.ч = 2) sp–гибридизация (прямая линия) Ag+ KLM 4s2 4p6 4d10 5s0 5p0
- 43. 2. K2[NiCl4] (к.ч. = 4) sp3 – гибридизация (тетраэдр) Ni+2 KL 3s2 3p6 3d8 4s0 4p0
- 44. При взаимодействии с жесткими лигандами происходит спаривание d-электронов. Образуется диамагнитный комплекс с плоским квадратным строением. Кристаллическое
- 45. 3. K2[Ni(CN)4] (к.ч. = 4) dsp2 – гибридизация (плоский квадрат) 28Ni2+ KL 3s2 3p6 3d8 4s0
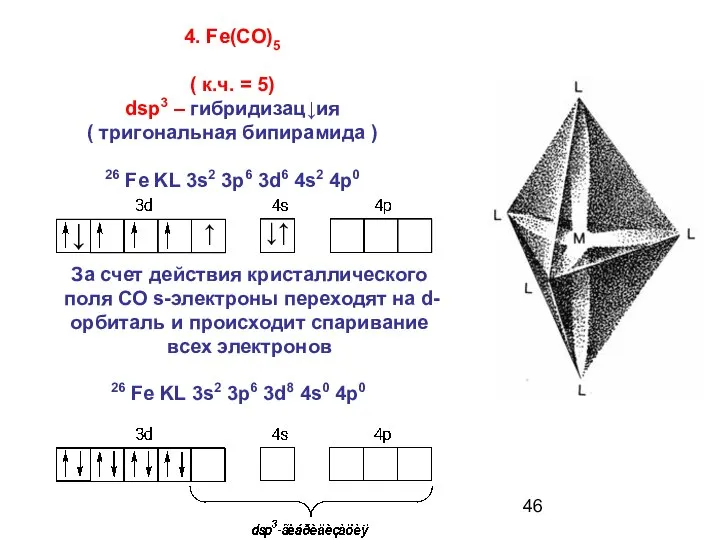
- 46. 4. Fe(CO)5 ( к.ч. = 5) dsp3 – гибридизац↓ия ( тригональная бипирамида ) 26 Fе KL
- 47. 5. K3[Fe(CN)6] (к.ч. = 6) d2sp3 – гибридизация (октаэдр) 26Fe3+ KL 3s2 3p6 3d5 4s0 4p0
- 48. Эффективность донорно-акцепторного взаимодействия лиганда и комплексообразователя, а, следовательно, и прочность связи между ними определяется их поляризуемостью
- 49. Жесткие и мягкие кислоты и основания ЖМКО Кислоты (по Льюису) – акцепторы электронов Al3+, Fe3+, Pb2+
- 50. Таким образом, прочность и устойчивость к диссоциации ковалентной связи между комплексообразователем и лигандами зависит от их
- 51. В соответствии с общим принципом «подобное в подобном» наиболее прочная и устойчивая к диссоциации ковалентная связь
- 52. Склонностью к комплексообразованию объясняется такжн токсичность цианидов, так как анион СN- ( очень мягкий лиганд) активно
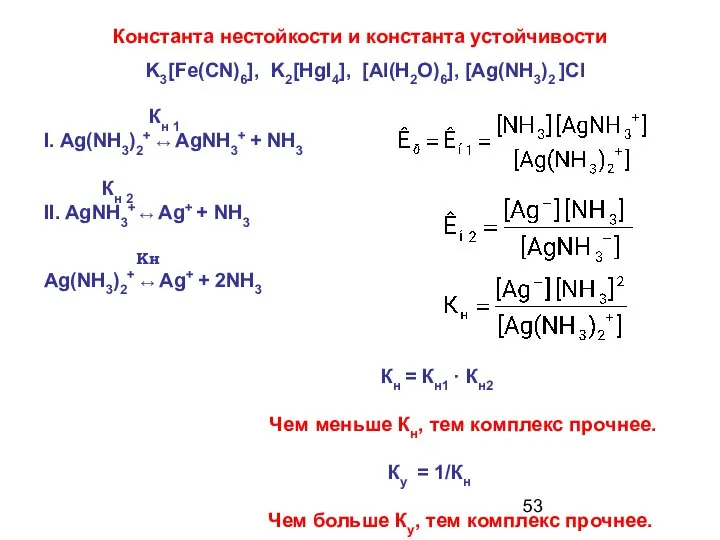
- 53. Константа нестойкости и константа устойчивости Кн 1 I. Ag(NH3)2+ ↔ AgNH3+ + NH3 Кн 2 II.
- 55. Смещение равновесия в растворах комплексных соединений
- 56. Если на систему, находящуюся в равновесии, оказывается внешнее воздействие, равновесие смещается в таком направлении, чтобы свести
- 57. Разрушение комплексов 1. Разрушение по металлу – введение лигандов, образующих с металлом более прочный комплекс
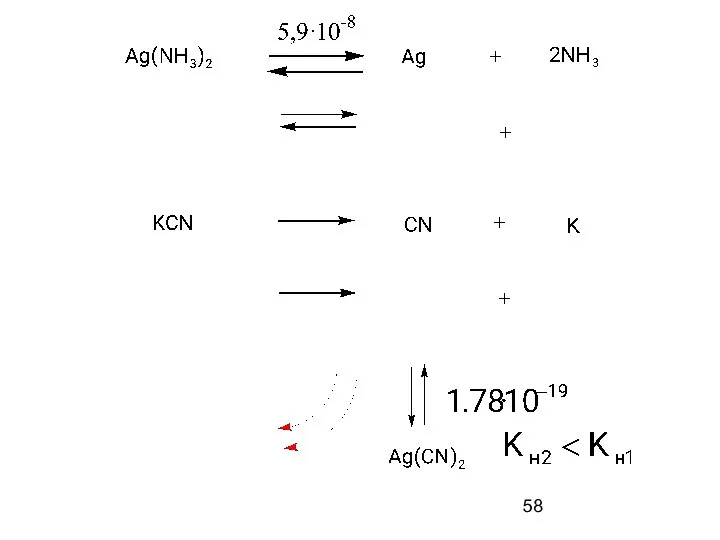
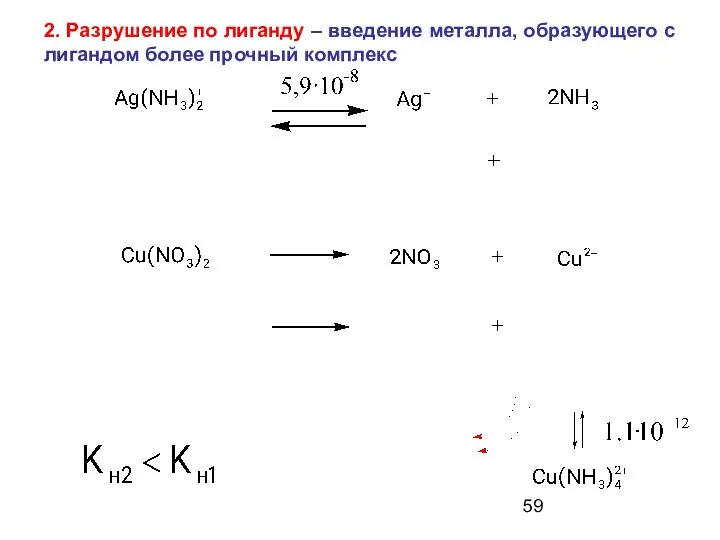
- 59. 2. Разрушение по лиганду – введение металла, образующего с лигандом более прочный комплекс
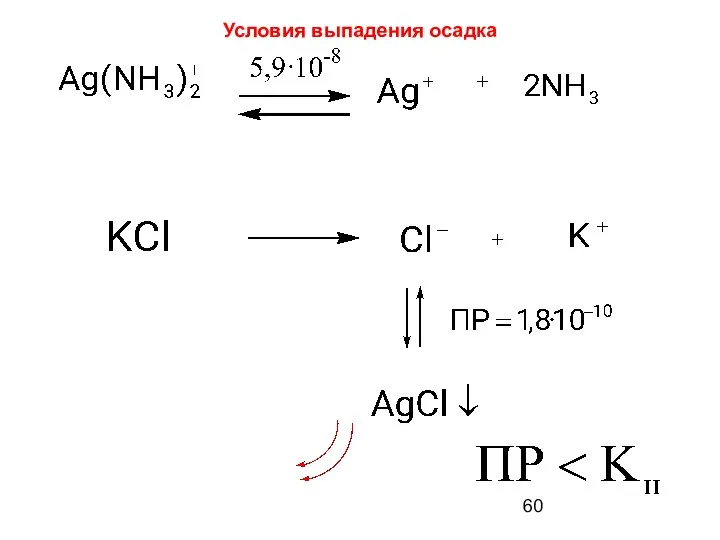
- 60. Условия выпадения осадка
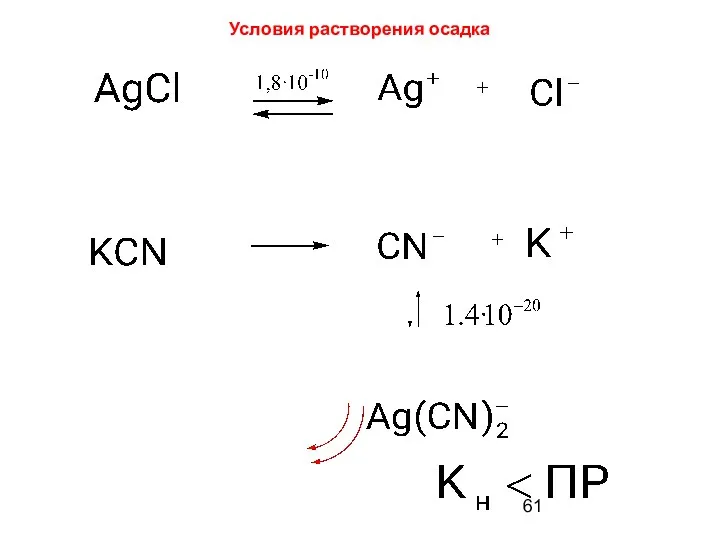
- 61. Условия растворения осадка
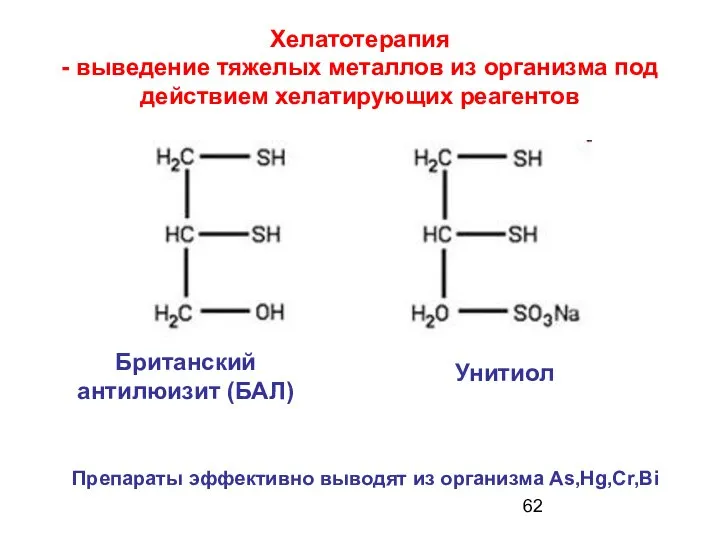
- 62. Хелатотерапия - выведение тяжелых металлов из организма под действием хелатирующих реагентов Британский антилюизит (БАЛ) Унитиол Препараты
- 63. Два основных принципа хелатотерапии Детоксикант (лиганд) должен эффективно связывать ионы-токсиканты то есть…!!!!!! - вновь образующиеся соединения
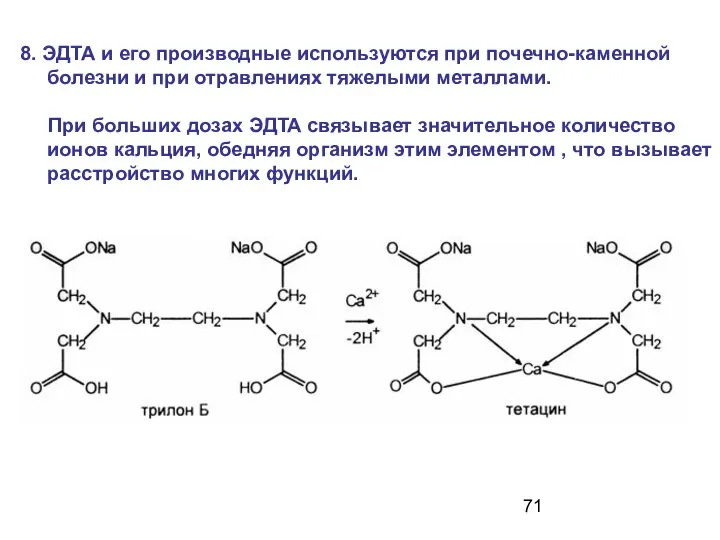
- 64. Медико-биологическое значение комплексов: 3. Трилон «Б» (ЭДТА) используется при мочекаменной болезни для разрушения камней и выведения
- 65. 5. Трилонометрия применяется для определения: содержания ионов кальция, цинка, магния, железа в фармпрепаратах, общего кальция в
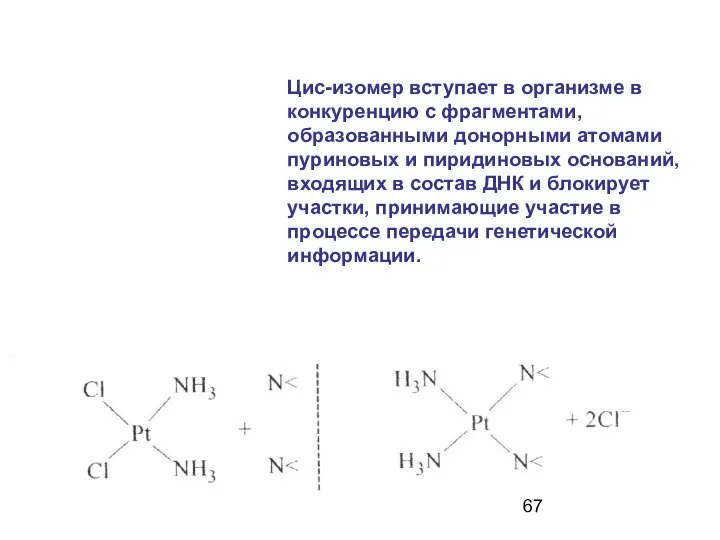
- 66. 6. Цис-изомер дихлордиамминплатины (II) обладает противоопухолевой активностью и применяется в качестве лекарственного средства при онкологических заболеваниях.
- 67. Цис-изомер вступает в организме в конкуренцию с фрагментами, образованными донорными атомами пуриновых и пиридиновых оснований, входящих
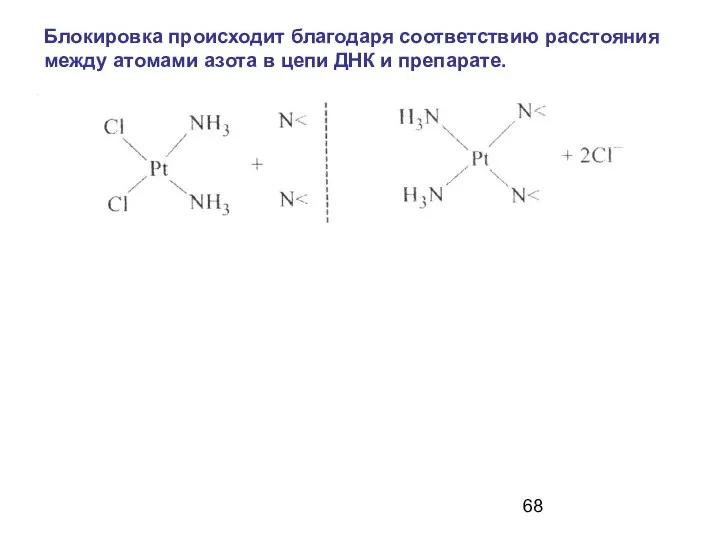
- 68. Блокировка происходит благодаря соответствию расстояния между атомами азота в цепи ДНК и препарате.
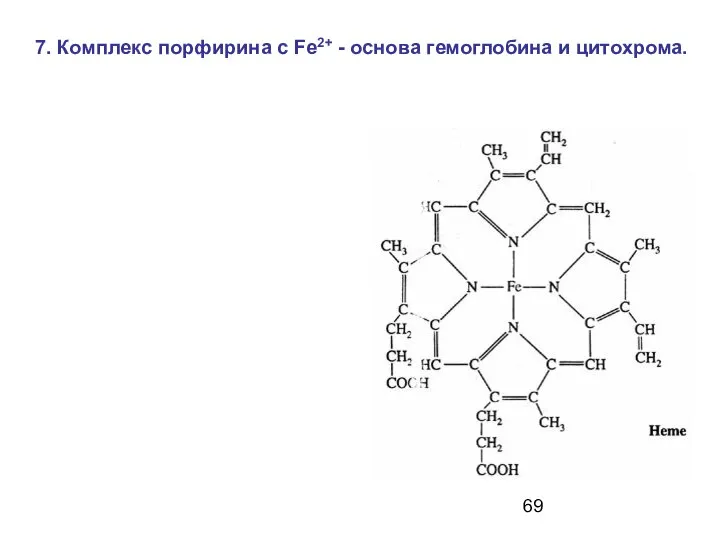
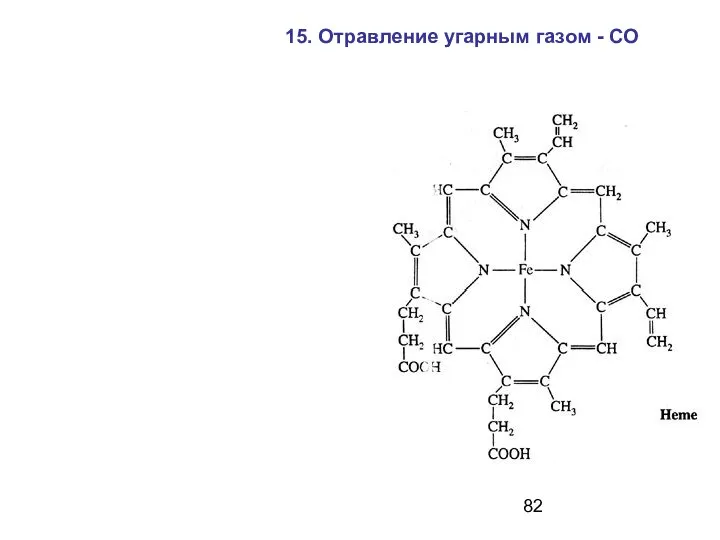
- 69. 7. Комплекс порфирина с Fe2+ - основа гемоглобина и цитохрома.
- 70. Среднее содержание гемоглобина в эритроцитах крови – 15 г / 100 мл. 1 г гемоглобина связывает
- 71. 8. ЭДТА и его производные используются при почечно-каменной болезни и при отравлениях тяжелыми металлами. При больших
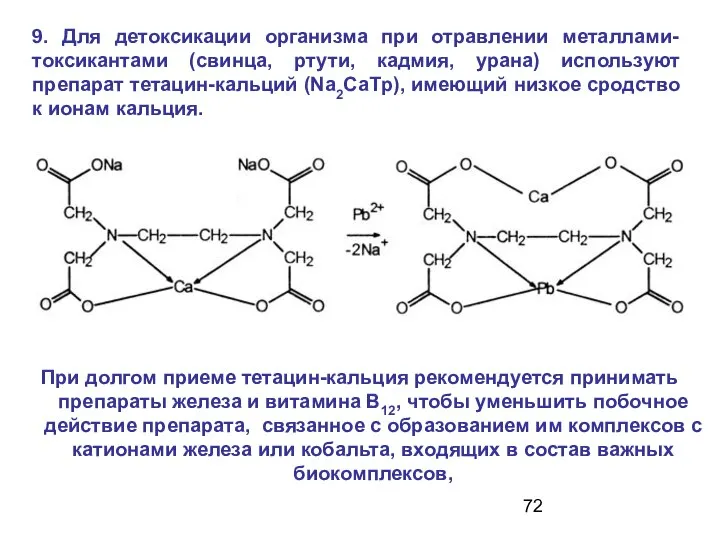
- 72. 9. Для детоксикации организма при отравлении металлами-токсикантами (свинца, ртути, кадмия, урана) используют препарат тетацин-кальций (Nа2СаТр), имеющий
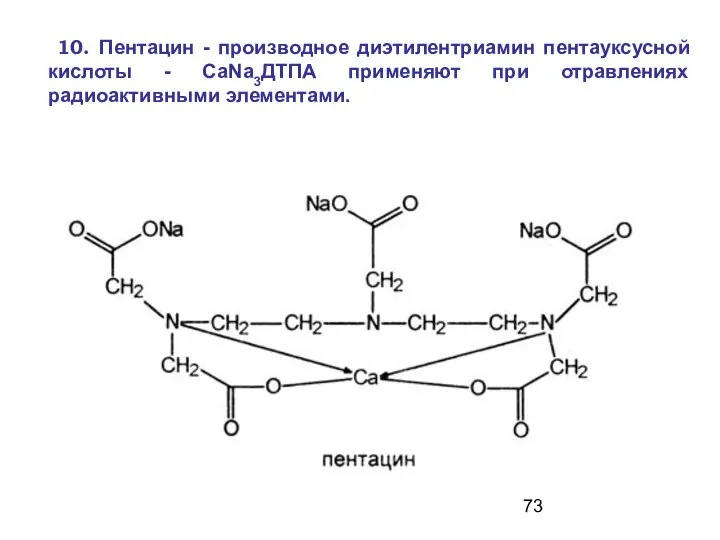
- 73. 10. Пентацин - производное диэтилентриамин пентауксусной кислоты - СаNа3ДТПА применяют при отравлениях радиоактивными элементами.
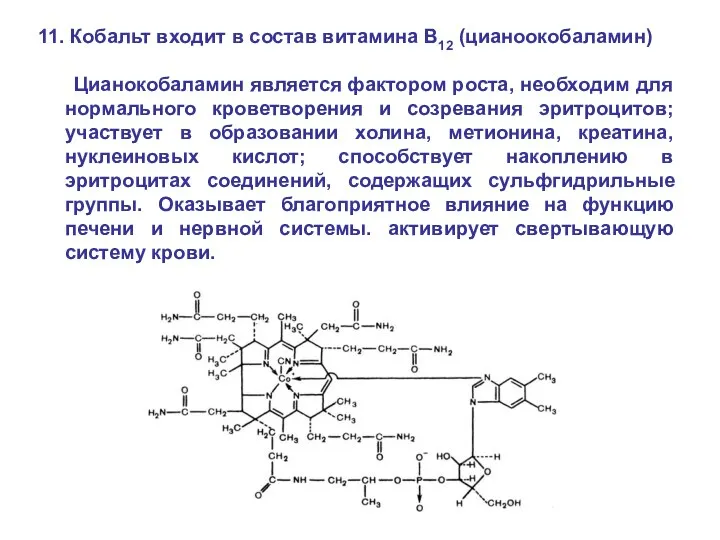
- 74. 11. Кобальт входит в состав витамина B12 (цианоокобаламин) Цианокобаламин является фактором роста, необходим для нормального кроветворения
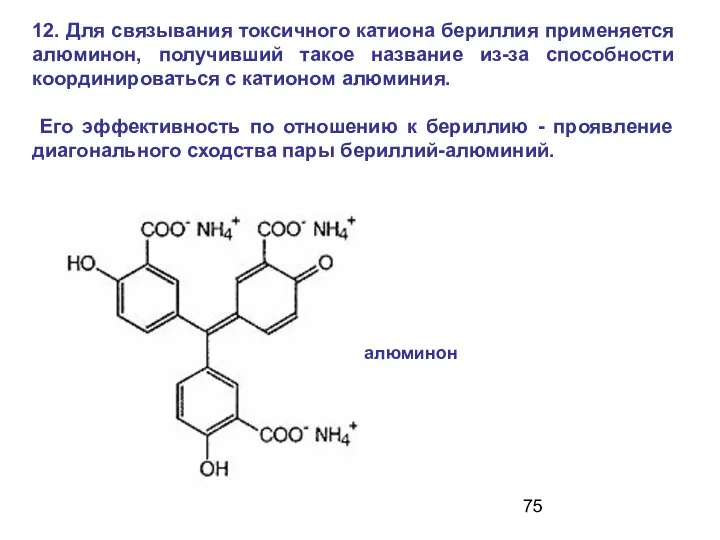
- 75. 12. Для связывания токсичного катиона бериллия применяется алюминон, получивший такое название из-за способности координироваться с катионом
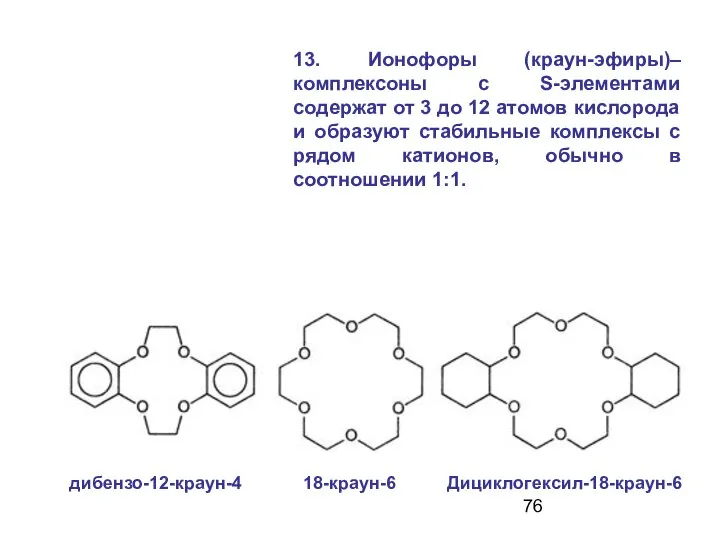
- 76. 13. Ионофоры (краун-эфиры)– комплексоны с S-элементами содержат от 3 до 12 атомов кислорода и образуют стабильные
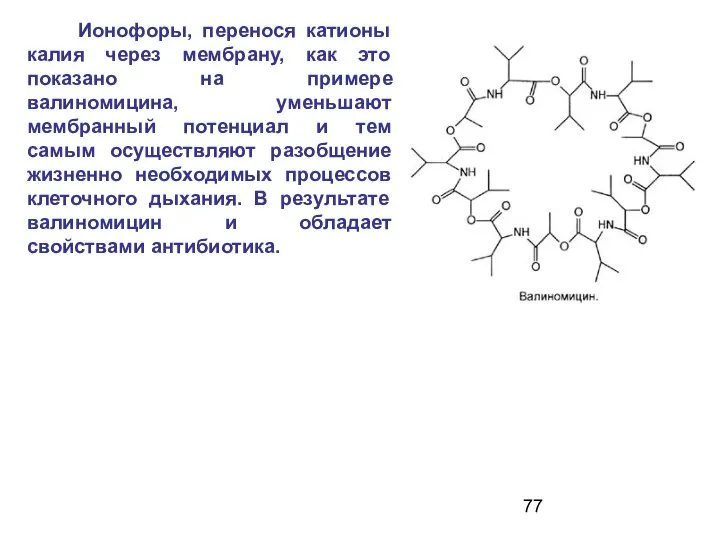
- 77. Ионофоры, перенося катионы калия через мембрану, как это показано на примере валиномицина, уменьшают мембранный потенциал и
- 78. Появление NO в организме связано с токсическим действием нитратов, которые при попадании в организм легко восстанавливаются
- 79. NO является лигандом, который, подобно кислороду, образует комплекс с гемоглобином, устойчивость которого в 60 раз больше,
- 80. б) Физиологическое значение: Вместе с тем, NO обязательно синтезируется в организме человека из аргинина. Время жизни
- 81. За открытие синтеза NO в организме и исследование его физиологической роли Р.Фурчготт, Л.Игнарро и Ф.Мурад были
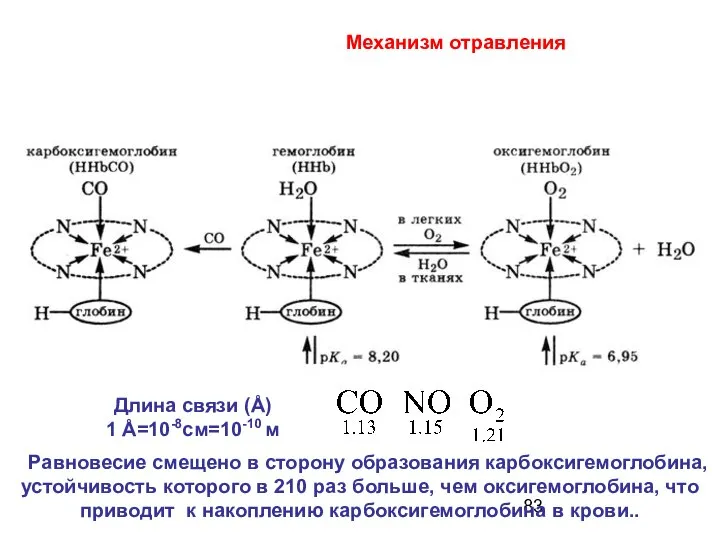
- 82. 15. Отравление угарным газом - СО
- 83. Равновесие смещено в сторону образования карбоксигемоглобина, устойчивость которого в 210 раз больше, чем оксигемоглобина, что приводит
- 84. Причины отравления 1. Курение
- 85. 2. Вдыхание выхлопных газов автомобиля.
- 86. 3. Преждевременное закрытие вытяжной заслонки протопленной печи.
- 87. Легкое отравление - содержание метгемоглобина 30% : наблюдается головная боль, слабость, тошнота. Отравление средней степени -
- 88. Пострадавшим необходимо тепло, сердечные средства и вдыхание чистого кислорода, так как содержание кислорода в воздухе недостаточно
- 90. Скачать презентацию
















![K4[Fe(CN)6] Fe2+ – центральный ион–комплексообразователь – акцептор электронов ( кислота Льюиса)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-21.jpg)


![КЛАССИФИКАЦИЯ 1. По заряду внутренней сферы: - катионного типа: [Ag(NH3)2]Cl, [Cu(NH3)4]SO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-27.jpg)
![4. По природе лигандов внутренней сферы: ацидокомплексы (анионы кислотных остатков): K3[Fe(CN)6],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-28.jpg)

![[Сr(Н2О)6]Сl3 [Сr(Н2О)4Сl2]Сl·2Н2О сине-серая темно-зеленая 3. Гидратная изомерия определяется характером связей молекул воды, входящих в состав комплекса](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-32.jpg)

![Номенклатура [Ag(NH3)2]Cl – хлорид диамминсеребра [Cu(NH3)4]SO4 – сульфат тетраамминмеди (II) [Pt(NH3)2Cl2] – дихлориддиамминплатина (II)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-38.jpg)

![Строение комплексных соединений: 1. [Ag(NH3)2]Cl Ag+ KLM 4s2 4p6 4d10 5s0 5p0](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-40.jpg)
![1. [Ag(NH3)2]Cl (к.ч = 2) sp–гибридизация (прямая линия) Ag+ KLM 4s2 4p6 4d10 5s0 5p0](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-41.jpg)
![2. K2[NiCl4] (к.ч. = 4) sp3 – гибридизация (тетраэдр) Ni+2 KL 3s2 3p6 3d8 4s0 4p0](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-42.jpg)

![3. K2[Ni(CN)4] (к.ч. = 4) dsp2 – гибридизация (плоский квадрат) 28Ni2+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-44.jpg)
![5. K3[Fe(CN)6] (к.ч. = 6) d2sp3 – гибридизация (октаэдр) 26Fe3+ KL](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408509/slide-46.jpg)





















 Выполнила: ученица 11 класса Э Бахарева Маргарита Руководитель: учитель химии Ефименко О.А.
Выполнила: ученица 11 класса Э Бахарева Маргарита Руководитель: учитель химии Ефименко О.А. Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат
Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат Ахрамович Наталья Михайловна учитель химии ГБОУ СОШ № 450 Курортного района Санкт – Петербурга
Ахрамович Наталья Михайловна учитель химии ГБОУ СОШ № 450 Курортного района Санкт – Петербурга Биохимия нервной ткани. Биологические мембраны
Биохимия нервной ткани. Биологические мембраны альдегиды и кетоны
альдегиды и кетоны Влияние фенолов на нас и окружающую среду
Влияние фенолов на нас и окружающую среду Жиры. История открытия жиров
Жиры. История открытия жиров Липиды. Классификация липидов
Липиды. Классификация липидов Калий. Общая информация
Калий. Общая информация Натрий
Натрий Решение задачи №10. Гидроксид рубидия. Команда «Карбораны»
Решение задачи №10. Гидроксид рубидия. Команда «Карбораны» Фосфор. Гипофосфатемия и гиперфосфатемия
Фосфор. Гипофосфатемия и гиперфосфатемия Лабораторное оборудование, посуда и средства защиты
Лабораторное оборудование, посуда и средства защиты Ароматические углеводороды
Ароматические углеводороды Энергетическое топливо
Энергетическое топливо Вода – основа жизни на Земле
Вода – основа жизни на Земле Презентация по Химии "Оцтова кислота" - скачать смотреть бесплатно
Презентация по Химии "Оцтова кислота" - скачать смотреть бесплатно Электрохимические технологии неорганических веществ
Электрохимические технологии неорганических веществ Химическая термодинамика. Термодинамические потенциалы
Химическая термодинамика. Термодинамические потенциалы Массовая доля компонентов
Массовая доля компонентов Бионеорганическая химия. Жидкие среды организма. (Лекция 2)
Бионеорганическая химия. Жидкие среды организма. (Лекция 2) Презентация по Химии "Презентация ОСНОВАНИЯ" - скачать смотреть
Презентация по Химии "Презентация ОСНОВАНИЯ" - скачать смотреть  Массовая доля элемента в веществе
Массовая доля элемента в веществе Спирты. Физические и химические свойства
Спирты. Физические и химические свойства Уравнения химических реакций
Уравнения химических реакций “Су. Ерітінділер” тарауын қорытындылау
“Су. Ерітінділер” тарауын қорытындылау Теоретическое описание полных сечений реакций при столкновениях 4,6He + 28Si и 6,7,9,11Li + 28Si
Теоретическое описание полных сечений реакций при столкновениях 4,6He + 28Si и 6,7,9,11Li + 28Si Теоретическая электрохимия, часть 1
Теоретическая электрохимия, часть 1