Содержание
- 3. Реакции обмена — это реакции, в результате которых, два сложных вещества обмениваются своими составными частями.
- 4. Реакции обмена, протекающие в растворах, идут до конца только в том случае, если в результате их
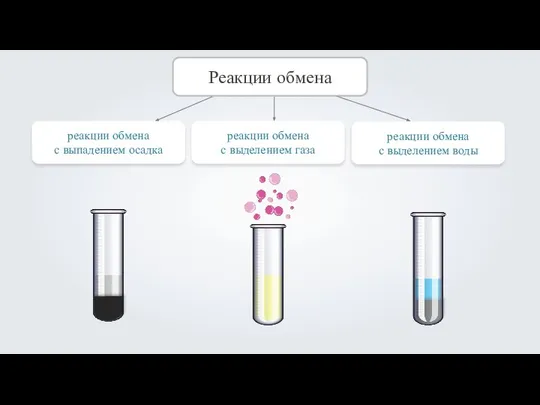
- 5. реакции обмена с выпадением осадка Реакции обмена реакции обмена с выделением газа реакции обмена с выделением
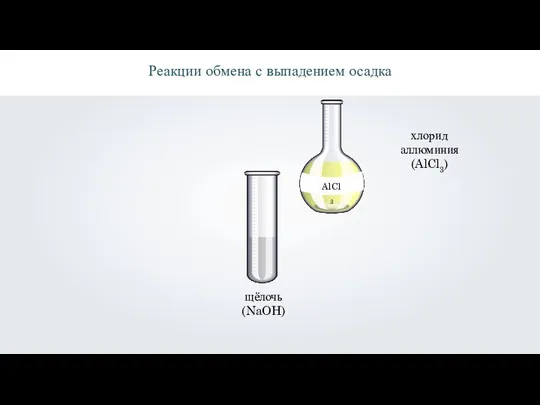
- 6. \ Реакции обмена с выпадением осадка щёлочь (NaOH) хлорид аллюминия (AlCl3)
- 7. \ Реакции обмена с выпадением осадка щёлочь (NaOH)
- 8. \ Реакции обмена с выпадением осадка
- 9. \ Реакции обмена с выпадением осадка
- 10. \ Реакции обмена с выпадением осадка AlCl3 + NaOН → Al(ОН)3↓ + NaCl ↓ AlCl3 +
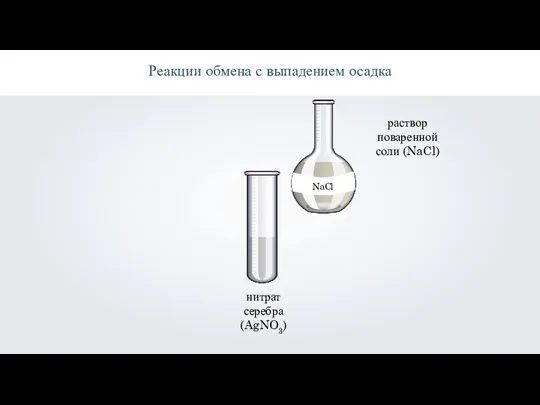
- 11. \ Реакции обмена с выпадением осадка нитрат серебра (AgNO3) раствор поваренной соли (NaCl)
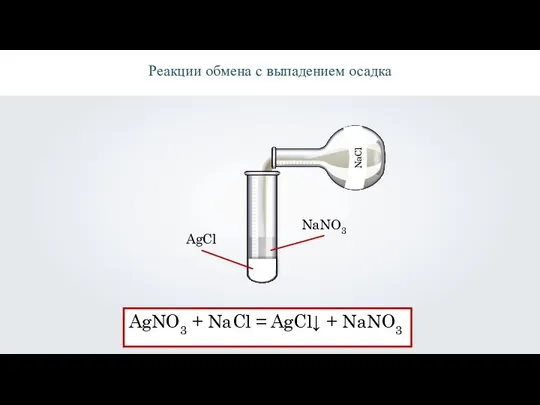
- 12. \ Реакции обмена с выпадением осадка AgNO3 + NaCl = AgCl↓ + NaNO3 AgCl NaNO3
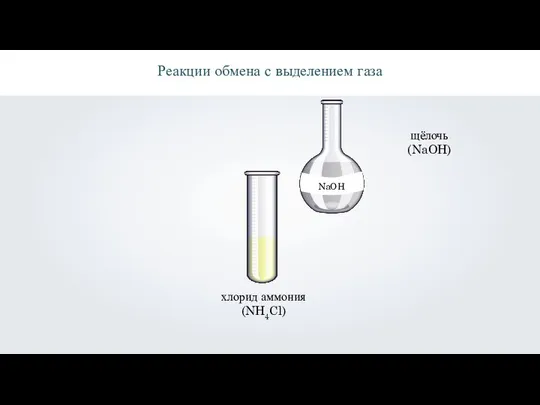
- 13. \ Реакции обмена с выделением газа хлорид аммония (NH4Cl) щёлочь (NaOH)
- 14. \ Реакции обмена с выделением газа
- 15. \ Реакции обмена с выделением газа
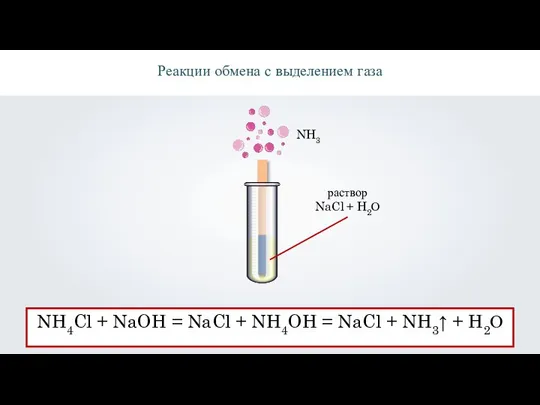
- 16. раствор NaCl + H2О \ Реакции обмена с выделением газа NH4Cl + NaOH = NaCl +
- 17. \ Реакции обмена с выделением воды Реакции нейтрализации — это реакции взаимодействия сильной кислоты со щёлочью,
- 18. \ Реакции обмена с выделением воды гидроксид калия (KOH)
- 19. \ Реакции обмена с выделением воды гидроксид калия (KOH) лакмус
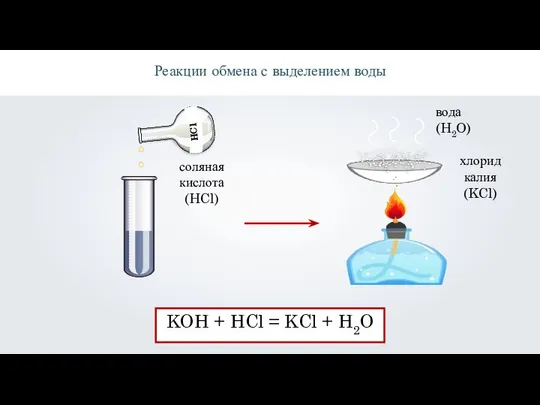
- 20. \ Реакции обмена с выделением воды соляная кислота (HCl) хлорид калия (KCl) KOH + HCl =
- 21. Основное правило протекания реакций обмена осадок газ вода
- 23. Скачать презентацию













 Современная химия Химия- это наука, изучающая свойства и превращения веществ, сопровождающееся изменением их состава и строе
Современная химия Химия- это наука, изучающая свойства и превращения веществ, сопровождающееся изменением их состава и строе Презентация по Химии "Химические элементы металлы и здоровье человека" - скачать смотреть бесплатно
Презентация по Химии "Химические элементы металлы и здоровье человека" - скачать смотреть бесплатно Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Теория растворов. Растворы электролитов
Теория растворов. Растворы электролитов Термодинамические характеристики многокомпонентных систем. Растворы. Основные понятия и определения
Термодинамические характеристики многокомпонентных систем. Растворы. Основные понятия и определения МИР ИНДИКАТОРОВ
МИР ИНДИКАТОРОВ Порох. Сера, халькогены
Порох. Сера, халькогены ОГЭ по химии. (Занятие 6)
ОГЭ по химии. (Занятие 6) Сульфиды. Лекция 8
Сульфиды. Лекция 8 Фосфор. Получение. Химические свойства
Фосфор. Получение. Химические свойства Положение тугоплавких металлов в Периодической системе элементов
Положение тугоплавких металлов в Периодической системе элементов Презентация по Химии "Царь - горох" - скачать смотреть
Презентация по Химии "Царь - горох" - скачать смотреть  К драгоценным металлам относятся золото, серебро, платина, палладий и др. Для изготовления ювелирных украшений в основном использу
К драгоценным металлам относятся золото, серебро, платина, палладий и др. Для изготовления ювелирных украшений в основном использу Взаимодействие атомов элементов-неметаллов между собой
Взаимодействие атомов элементов-неметаллов между собой Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс)
Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс) Низкомолекулярные компоненты сыворотки крови
Низкомолекулярные компоненты сыворотки крови Геологические структуры МПИ. Группа доминерализационных структур
Геологические структуры МПИ. Группа доминерализационных структур Выполнила: Здановская Карина 9 А класс
Выполнила: Здановская Карина 9 А класс  Эмульсии как лиофобные дисперсные системы
Эмульсии как лиофобные дисперсные системы Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии»
Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии» Основные законы химии
Основные законы химии Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ»
Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ» Алкены. Химические свойства этилена
Алкены. Химические свойства этилена Биологически важные вещества - белки
Биологически важные вещества - белки Gas hydrates
Gas hydrates Значення хімії в повсякденному житті
Значення хімії в повсякденному житті  Агрегатные состояния вещества. Плавление и отвердевание кристаллических тел
Агрегатные состояния вещества. Плавление и отвердевание кристаллических тел Осадительное титрование
Осадительное титрование