Содержание
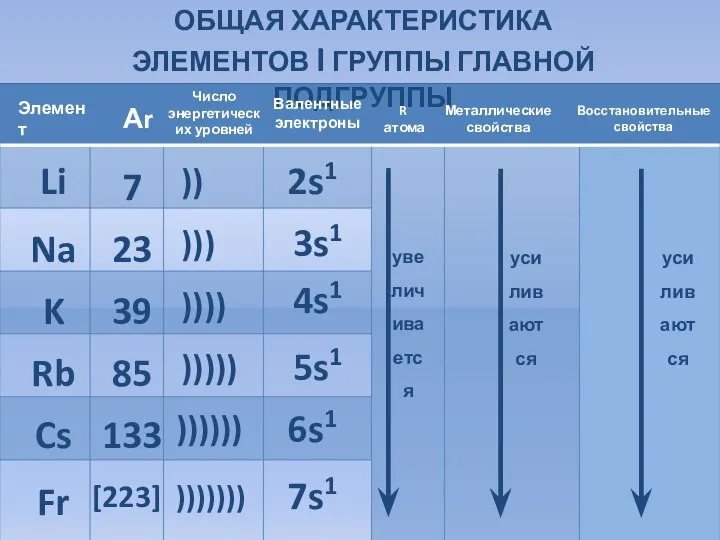
- 2. ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ I ГРУППЫ ГЛАВНОЙ ПОДГРУППЫ Li Na K Rb Cs Fr 7 23 39
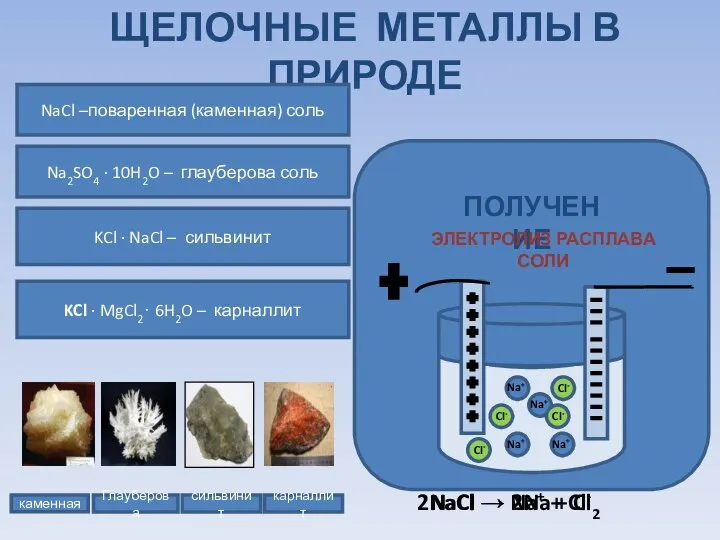
- 3. ЩЕЛОЧНЫЕ МЕТАЛЛЫ В ПРИРОДЕ каменная Глауберова сильвинит карналлит NaCl –поваренная (каменная) соль Na2SO4 ∙ 10H2O –
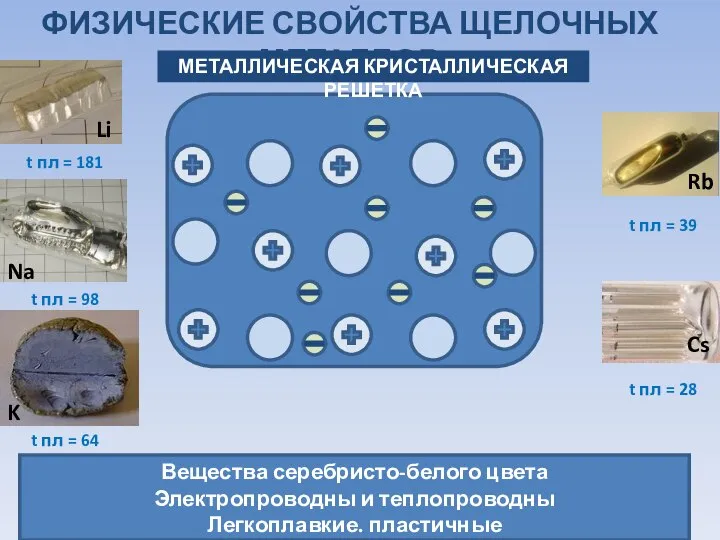
- 4. ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные t
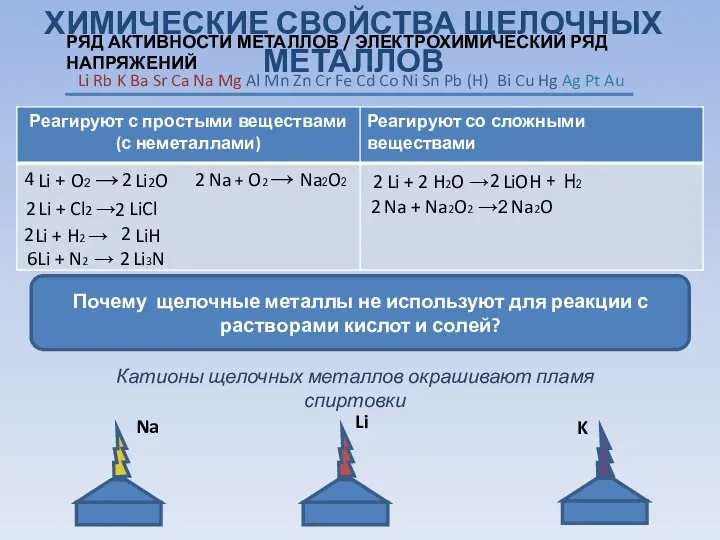
- 5. ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ Почему щелочные металлы не используют для реакции с растворами кислот и солей?
- 7. Скачать презентацию
 Вспомогательные устройства для высокоэффективной жидкостной хроматографии (ВЭЖХ)
Вспомогательные устройства для высокоэффективной жидкостной хроматографии (ВЭЖХ) Композиционные материалы, состав и классификация композиционных материалов
Композиционные материалы, состав и классификация композиционных материалов Степень окисления
Степень окисления Алканы. Гомологический ряд
Алканы. Гомологический ряд Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине Класса неорганических соединений.
Класса неорганических соединений. Тұздар гидролизі
Тұздар гидролизі Теоретические основы органической химии
Теоретические основы органической химии Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Комплексные соединения
Комплексные соединения Благородные металлы
Благородные металлы КАЛЬЦИЙ Ca 9 класс
КАЛЬЦИЙ Ca 9 класс Неметаллы IVA и IIIA групп Углерод, кремний , бор
Неметаллы IVA и IIIA групп Углерод, кремний , бор Гидролиз солей.
Гидролиз солей.  Спирт µндіру технологиясы
Спирт µндіру технологиясы Колообіг Карбону в природі Оленченко Катерина, 11-Б
Колообіг Карбону в природі Оленченко Катерина, 11-Б  Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Химия и экология
Химия и экология Дезактивація радіаційних речовин у зоні ядерного ураження
Дезактивація радіаційних речовин у зоні ядерного ураження Лабораторные, микробиологические и иммунологические исследования. Окраска препаратов по методу Грама
Лабораторные, микробиологические и иммунологические исследования. Окраска препаратов по методу Грама Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Диаграмма состояния Fe - FeC. Лекция 5 - 6
Диаграмма состояния Fe - FeC. Лекция 5 - 6 Адсорбционные явления. Общая характеристика адсорбции
Адсорбционные явления. Общая характеристика адсорбции Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций
Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Алканы. Бутан - С4Н10
Алканы. Бутан - С4Н10 Волокна
Волокна Соли Mg SO4 – сульфат магния
Соли Mg SO4 – сульфат магния