Содержание
- 2. Минеральные соли и их биологическая роль.
- 3. Минеральные соли и кислоты находятся в клетках или в виде растворов, или в виде твердых отложений.
- 4. Биологическая роль анионов и катионов Разность между количеством катионов и анионов на поверхности и внутри клетки
- 5. Водно-солевой обмен — совокупность процессов поступления воды и солей (электролитов) в организм, их всасывания, распределения во
- 6. Кислотно-щелочное равновесие— относительное постоянство концентрации водородных ионов во внутренних средах организма, обеспечивающее полноценность метаболических процессов, протекающих
- 7. буферная система крови 1. бикарбонатная система: Н2СО3 (угольная кислота) — NaHCO3 (бикарбонат натрия), общим ионом в
- 8. 2. К буферным системам крови относятся также белки, особенно гемоглобин, которые являются самой мощной буферной системой
- 9. Применение солей
- 10. Соли на кухне В приготовлении пищи поваренная соль употребляется как важная приправа. Соль имеет хорошо знакомый
- 11. NaHCO3 (гидрокарбонат натрия) — питьевая или пищевая сода, натрий двууглекислый, бикарбонат натрия В пищевой промышленности —
- 12. Соли в ванной Кальцинированная и кристаллическая сода. Na2CO3 (карбонат натрия) — кальцинированная сода Na2CO3·10H2O (декагидрат карбоната
- 13. Мыло В химическом отношении основным компонентом твёрдого мыла являются смесь растворимых солей высших жирных кислот. Обычно
- 14. Соли для ремонта Строительство — это один из основных потребителей карбоната кальция. Шпатлевки, различные герметики —
- 15. Соли в саду и огороде Селитры используются как азотные удобрения, при этом калиевая селитра является также
- 16. Соли в аптечке Ляпис Ляпис — Нитрат серебра (I) используется в медицине (ляписный карандаш) для прижигания
- 17. Перманганат калия Разбавленные растворы (около 0,1 %) перманганата калия нашли широчайшее применение в медицине как антисептическое
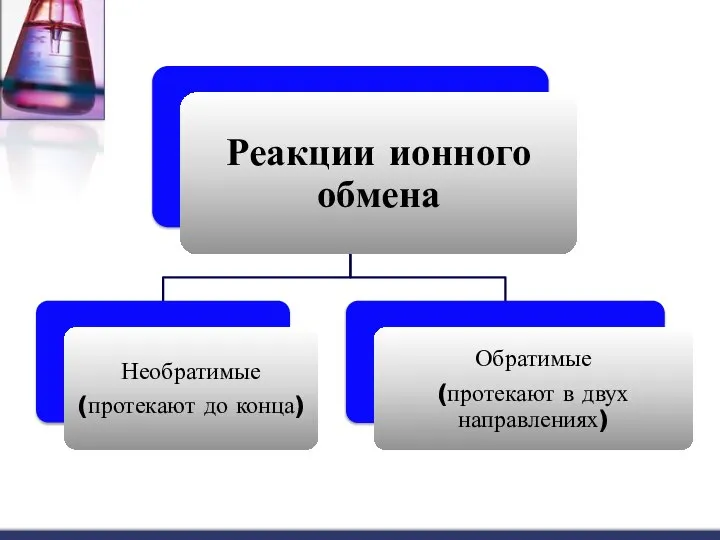
- 18. Реакции обмена протекают между ионами (положительно и отрицательно заряженными частицами) поэтому они называются реакциями ионного обмена
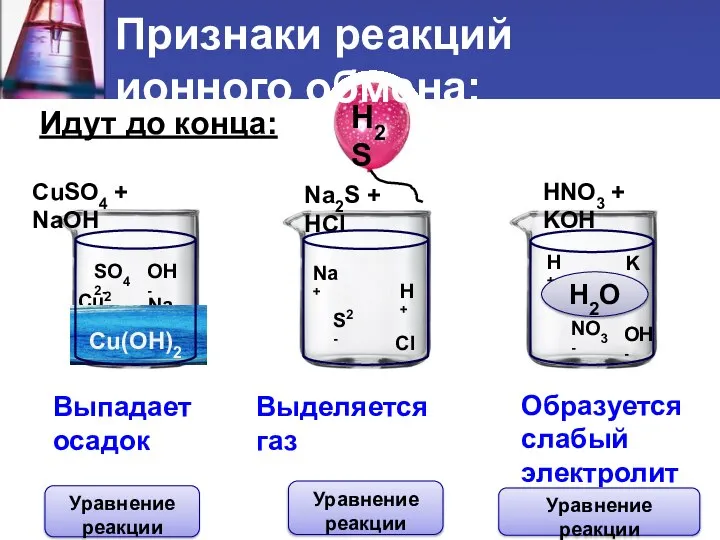
- 20. Идут до конца: CuSO4 + NaOH Na2S + HCl HNO3 + KOH Cu2+ SO42- Na+ OH-
- 21. Если образуется осадок: CuSO4 + 2NaOH Na2SO4 + Cu(OH)2 2AgNO3 + CaCl2 Ca(NO3)2 + 2AgCl Na2CO3
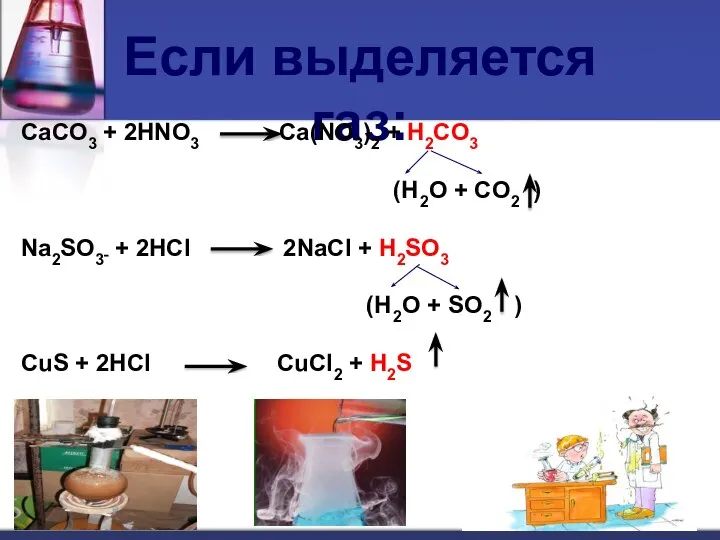
- 22. Если выделяется газ: CaCO3 + 2HNO3 Ca(NO3)2 + H2CO3 (H2O + CO2 ) Na2SO3 + 2HCl
- 23. Если образуется вода: CuO + H2SO4 CuSO4 + H2O Fe(OH)3 + 3HCl FeCl3 + 3H2O NaOH
- 24. 1) ЗАПИСАТЬ УРАВНЕНИЕ РЕАКЦИИИ В МОЛЕКУЛЯРНОЙ ФОРМЕ FeCI3 + 3NaOH = Fe(OH)3 + 3 NaCI 2)
- 25. Не расписываются на ионы: Вода H2O. Слабые кислоты (HNO2, H2CO3, H2SO3, CH3COOH и др.). Слабые основания
- 26. Обратимые реакции Na2SO4 + KNO3 Na+ SO42- K+ NO3- 1.Нет осадка 2.Не выделяется газ 3.Не образуется
- 27. Составление уравнений Молекулярное уравнение Na2SO4+2KNO3 2NaNO3 + K2SO4 Полное ионное уравнение 2Na + + SO4 2-
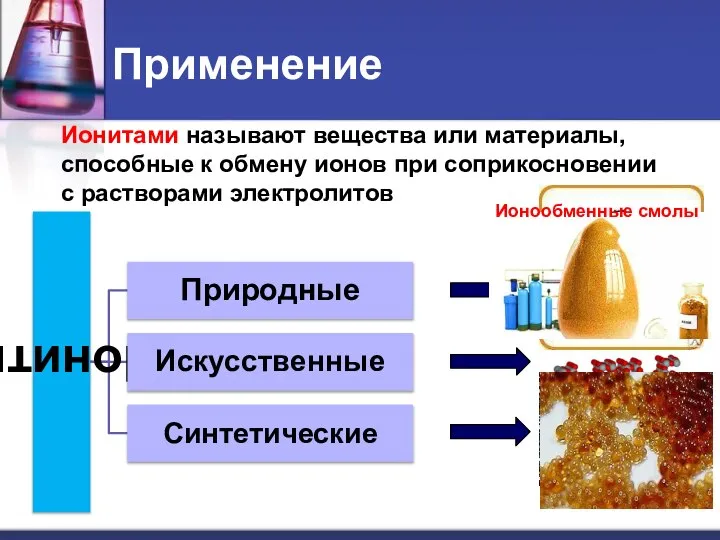
- 28. Применение Ионитами называют вещества или материалы, способные к обмену ионов при соприкосновении с растворами электролитов Цеолит
- 30. Скачать презентацию























 Метанол, етанол, гліцерин
Метанол, етанол, гліцерин Позднемеловая трубка взрыва щелочных базальтов Красноозерная
Позднемеловая трубка взрыва щелочных базальтов Красноозерная Эволюция антропогенных загрязнений в окружающей среде. Роль физико-химических явлений
Эволюция антропогенных загрязнений в окружающей среде. Роль физико-химических явлений Практическая работа по химии. Строение пламени
Практическая работа по химии. Строение пламени Кислоты
Кислоты Галогены VII группы. Биологическая роль и применение в медицине
Галогены VII группы. Биологическая роль и применение в медицине Занятие по познавательному развитию на тему: «Где спрятался воздух?» в средней группе.
Занятие по познавательному развитию на тему: «Где спрятался воздух?» в средней группе.  Молярный объём
Молярный объём Псевдогалогены и их соединения
Псевдогалогены и их соединения Органическая химия. Классификация и номенклатура органических соединений (ОС). Пространственное строение ОС
Органическая химия. Классификация и номенклатура органических соединений (ОС). Пространственное строение ОС Жиры Цели урока: Изучить жиры: состав, классификация,физические и химические свойства, переработка, применение, биологич
Жиры Цели урока: Изучить жиры: состав, классификация,физические и химические свойства, переработка, применение, биологич Теории кислот и оснований. Буферные системы крови
Теории кислот и оснований. Буферные системы крови План розміщення добрив у польовій сівозміні. (Лабораторна робота 22)
План розміщення добрив у польовій сівозміні. (Лабораторна робота 22) Нанохімія та нанотехнології
Нанохімія та нанотехнології Ультраосновные породы (гипербазиты)
Ультраосновные породы (гипербазиты) Применение интерактивной доски на уроках химии Учитель химии МОУ «СОШ п. Первомайский» Кириченко Е.Н.
Применение интерактивной доски на уроках химии Учитель химии МОУ «СОШ п. Первомайский» Кириченко Е.Н. МОЮЩИЕ СРЕДСТВА СВОЙСТВА МОЮЩИХ СРЕДСТВ КЛАССИФИКАЦИЯ МОЮЩИХ СРЕДСТВ
МОЮЩИЕ СРЕДСТВА СВОЙСТВА МОЮЩИХ СРЕДСТВ КЛАССИФИКАЦИЯ МОЮЩИХ СРЕДСТВ Ароматические системы
Ароматические системы Неорганические вещества
Неорганические вещества Буферные растворы
Буферные растворы Общая технология отрасли. Сахар и сахаристые вещества
Общая технология отрасли. Сахар и сахаристые вещества Химические и физические явления
Химические и физические явления Отдельные классы дисперсных систем
Отдельные классы дисперсных систем Ферменты. Значение ферментов
Ферменты. Значение ферментов Марганец. Роль марганца в организме
Марганец. Роль марганца в организме Элементы 7 группы побочной подгруппы
Элементы 7 группы побочной подгруппы Современная система контроля и обеспечения качества лекарственных средств в Украине
Современная система контроля и обеспечения качества лекарственных средств в Украине Сложные эфиры
Сложные эфиры