Содержание
- 2. Повторение первой лекции
- 3. Квант света Сколько квантов света потребуется для того, чтобы вскипятить 18 г воды инфракрасным излучением 10
- 4. Строение вещества Г. Пиментел , Р. Спратли Как квантовая механика объясняет химическую связь А.Ф. Уэллс Строение
- 5. Строение вещества Дж. Дальтон (1802 г.) высказал идею о том, что материя состоит из дискретных атомов.
- 6. Атомная модель Бора Центральное ядро атома несет положительный заряд, равный атомную номеру Z; Для сохранения электронейтральности
- 7. Атомная модель Бора
- 8. Квантово-механическая модель атома Уравнение Шредингера: В полярной системе координат:
- 9. Квантово-механическая модель атома Волновая функция: n – главное квантовое число; l – орбитальное квантовое число; ml
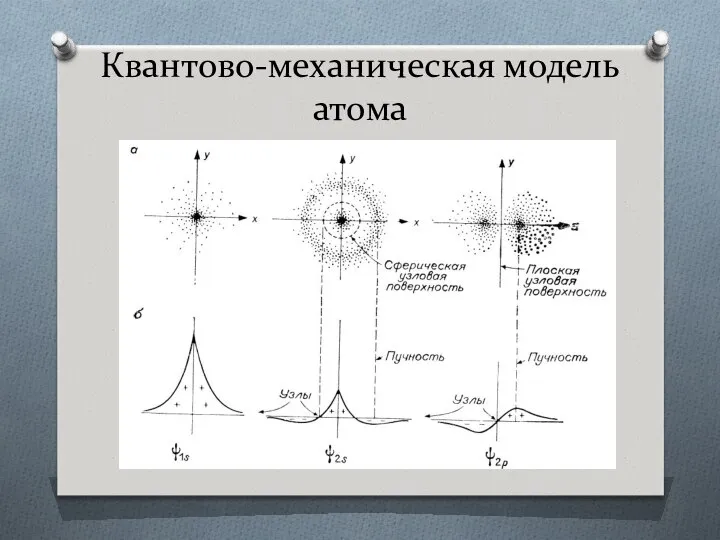
- 10. Квантово-механическая модель атома
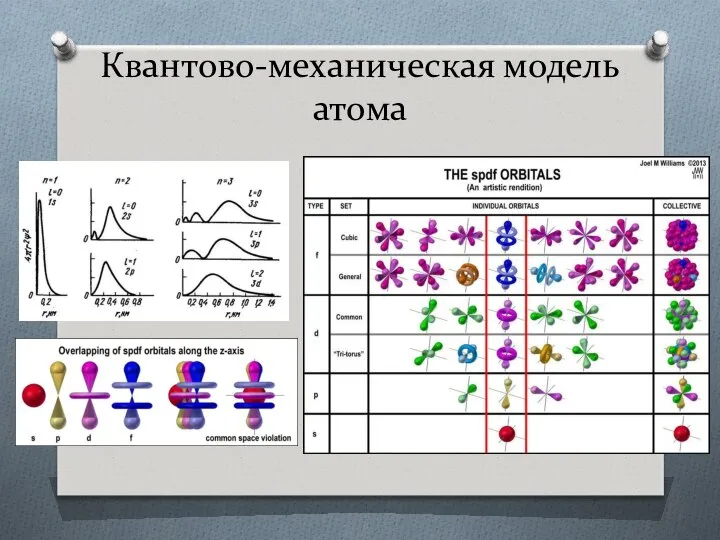
- 11. Квантово-механическая модель атома
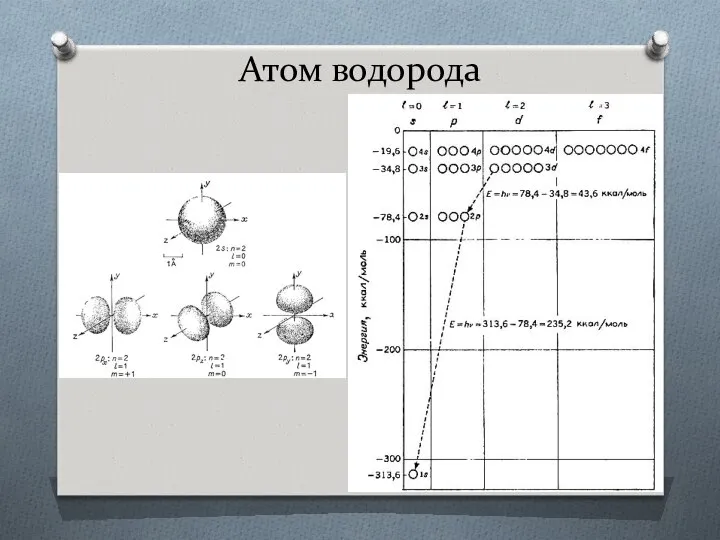
- 12. Атом водорода
- 13. Другие одноэлектронные атомы При увеличении заряда ядра электроны связываются в атоме сильнее и притягиваются ближе к
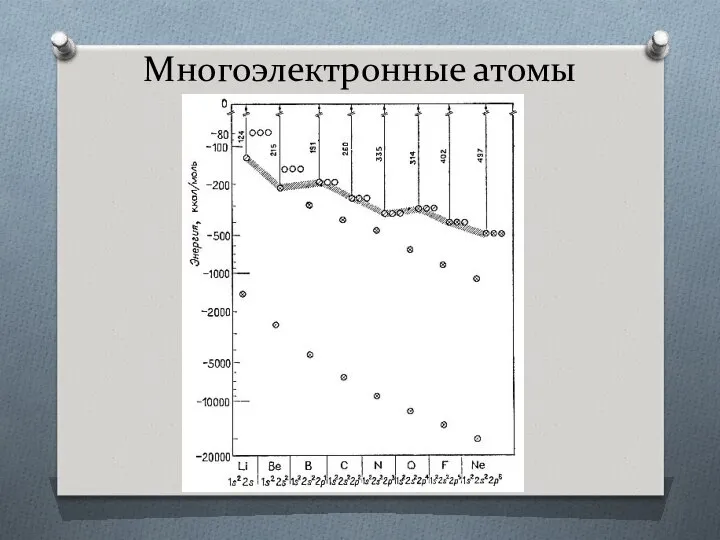
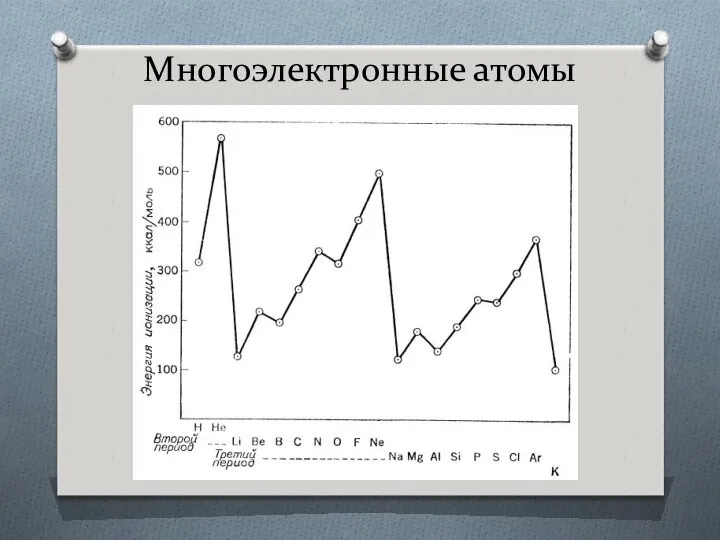
- 14. Многоэлектронные атомы Межэлектронное отталкивание расщепляет уровни энергии с одинаковым квантовым числом.
- 15. Многоэлектронные атомы
- 16. Многоэлектронные атомы
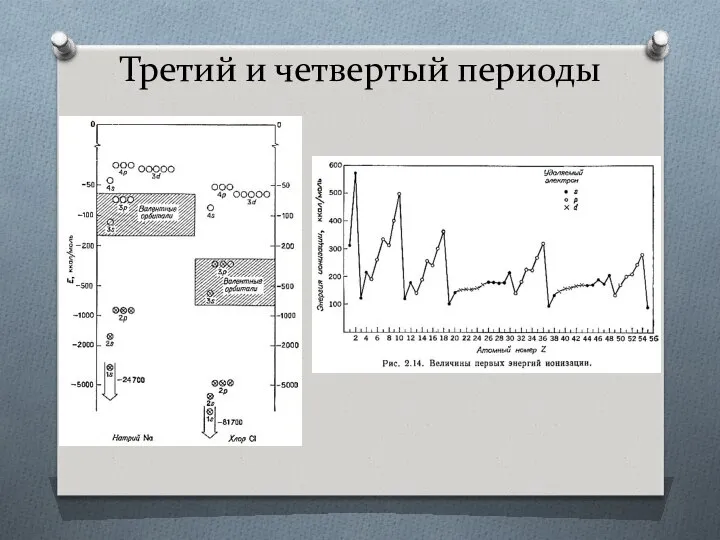
- 17. Третий и четвертый периоды
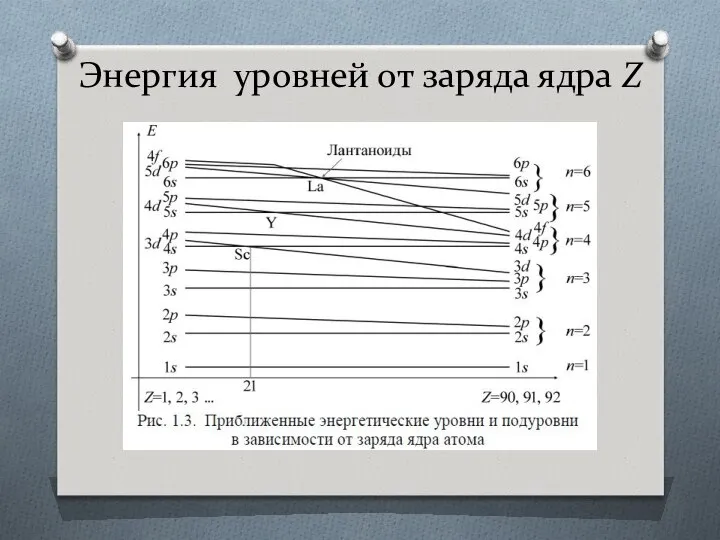
- 18. Энергия уровней от заряда ядра Z
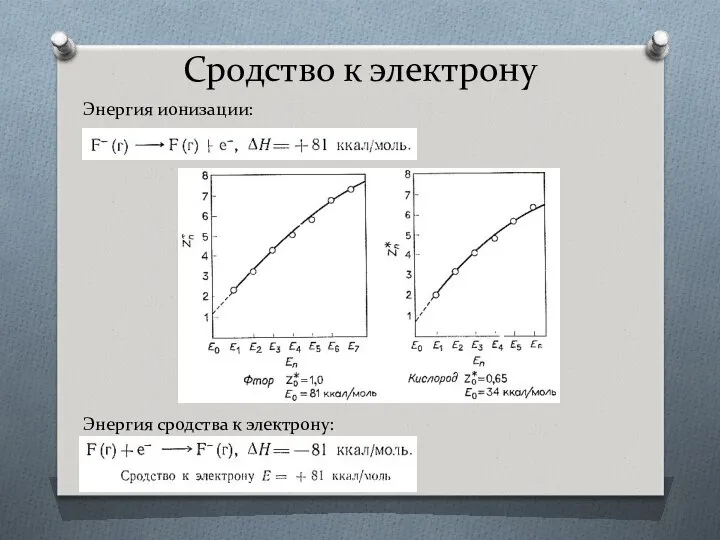
- 19. Сродство к электрону Энергия ионизации: Энергия сродства к электрону:
- 20. Химическая связь Описание химически связанных атомов: Метод валентных связей Метод молекулярных орбиталей (Так же как и
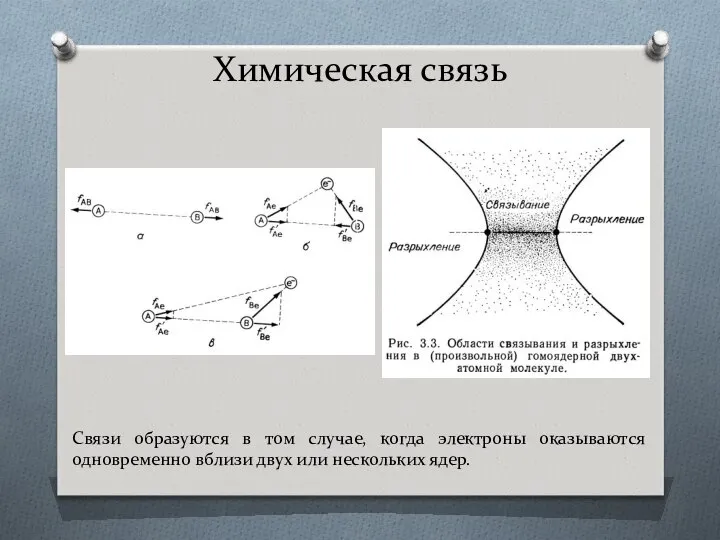
- 21. Химическая связь Связи образуются в том случае, когда электроны оказываются одновременно вблизи двух или нескольких ядер.
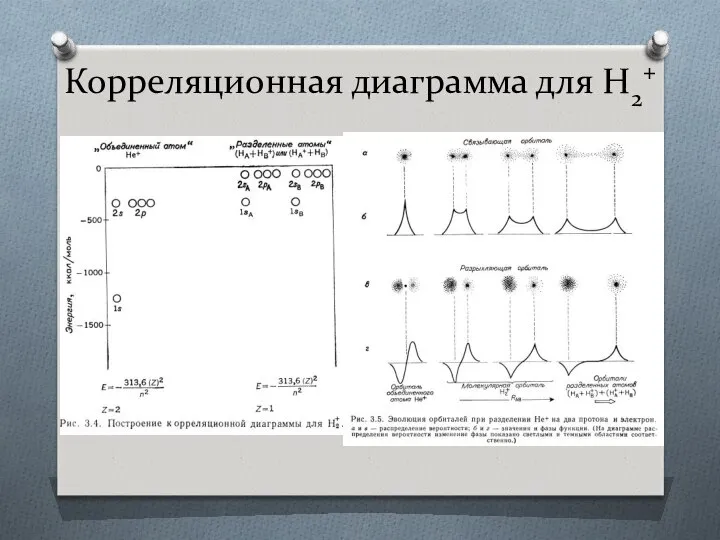
- 22. Корреляционная диаграмма для H2+
- 23. Корреляционная диаграмма для H2+ H2+ - устойчивая молекула. Энергия связи = 64,5 ккал/моль. Длина связи 1,06
- 24. Связывающие электроны и порядок связи
- 25. Многоэлектронные гомоатомные молекулы Орбитали, расположенные ниже валентных орбиталей не влияют на связь. Общее правило: по мере
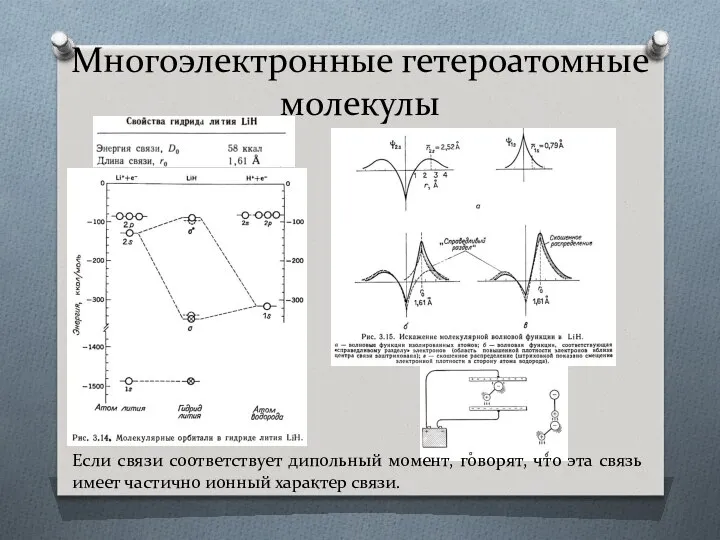
- 26. Многоэлектронные гетероатомные молекулы Если связи соответствует дипольный момент, говорят, что эта связь имеет частично ионный характер
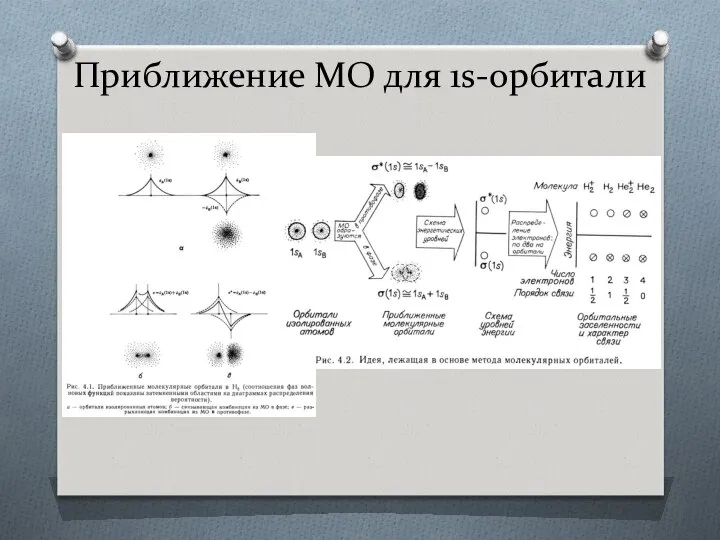
- 27. Приближение МО для 1s-орбитали
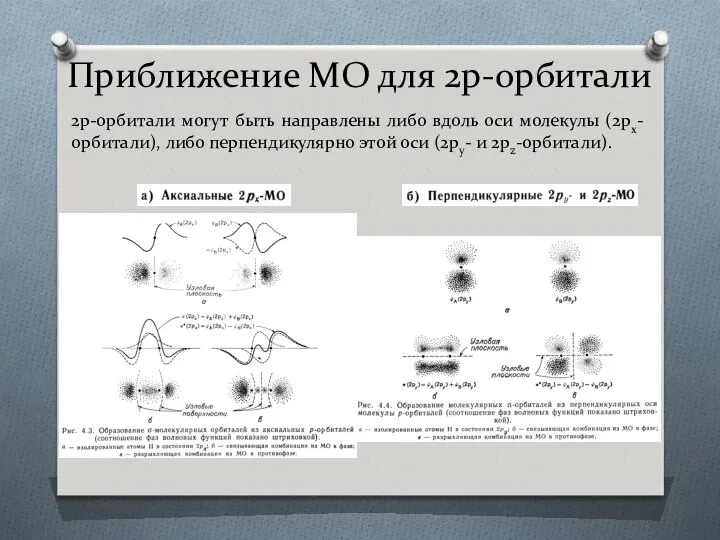
- 28. Приближение МО для 2p-орбитали 2p-орбитали могут быть направлены либо вдоль оси молекулы (2px-орбитали), либо перпендикулярно этой
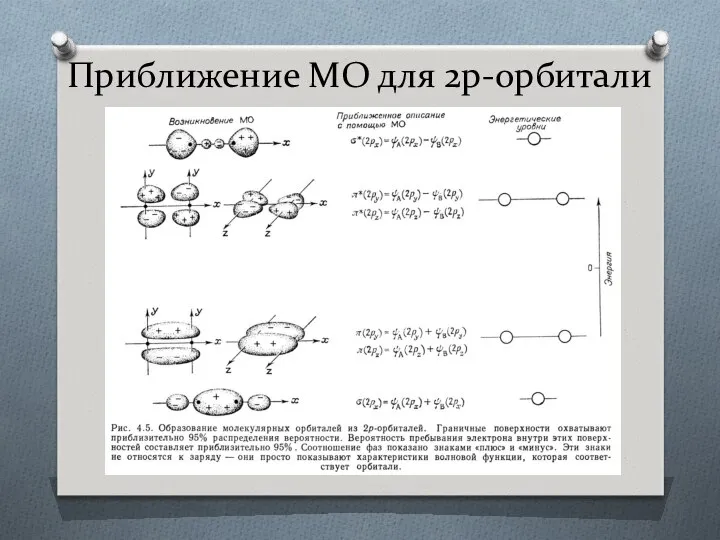
- 29. Приближение МО для 2p-орбитали
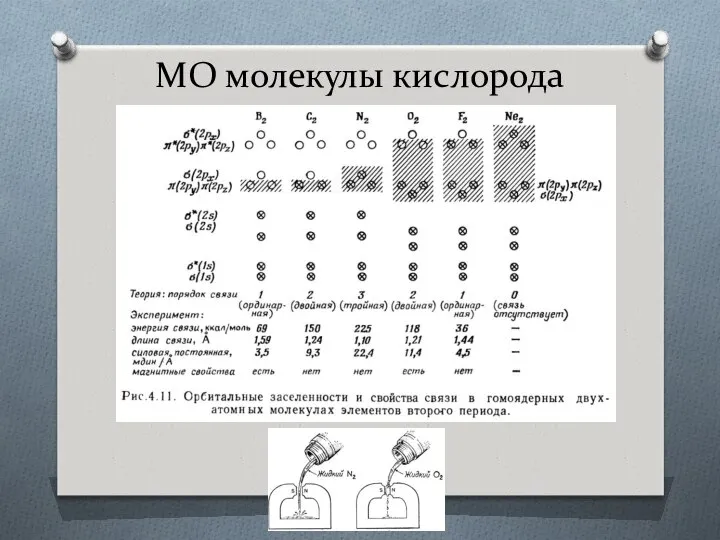
- 30. МО молекулы кислорода
- 31. МО молекулы кислорода
- 32. Типы химических связей Ковалентная связь Ионная связь Металлическая связь Водородная связь Ван-дер-ваальсову связь Ковалентная связь Наиболее
- 33. Типы химических связей Ковалентная связь Гомоядерные молекулы (неполярные связи) Гетероядерные молекулы (полярные связи)
- 34. Типы химических связей Ионная связь прочная химическая связь, образующаяся между атомами с большой разностью электроотрицательностей в
- 35. Типы химических связей Металлическая связь Отличительная черта металлов – число валентных электронов меньше числа валентных орбиталей.
- 36. Типы химических связей Водородная связь (Н-связь) Если водород образует молекулы с атомами, обладающими большой электроотрицательностью и
- 37. Химическая связь в твердых веществах Газообразное состояние Химическая связь в молекуле отражает свойства вещества только тогда,
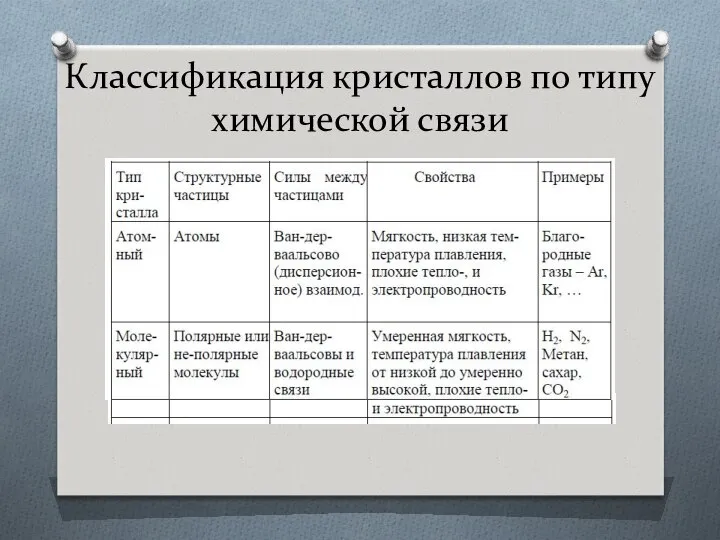
- 38. Классификация кристаллов по типу химической связи
- 39. Классификация кристаллов по типу химической связи
- 40. Классификация кристаллов по типу химической связи
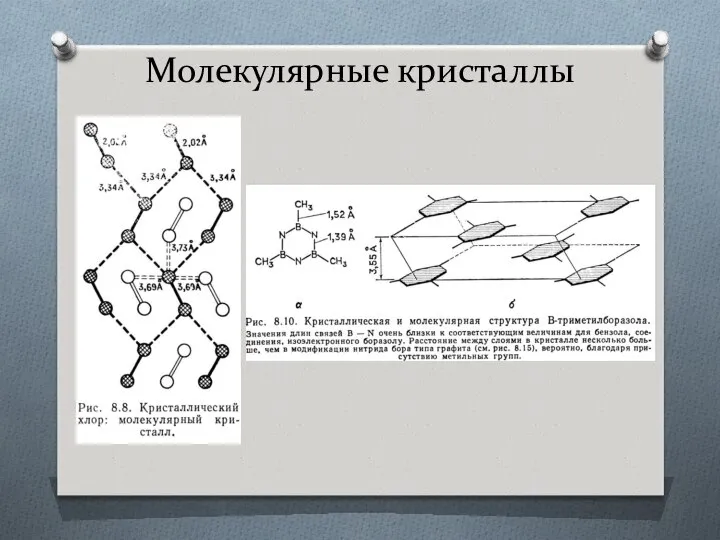
- 41. Молекулярные кристаллы
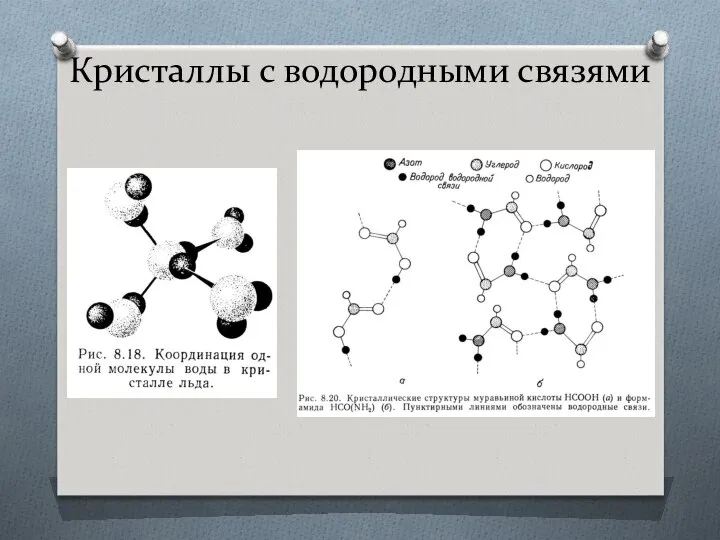
- 42. Кристаллы с водородными связями
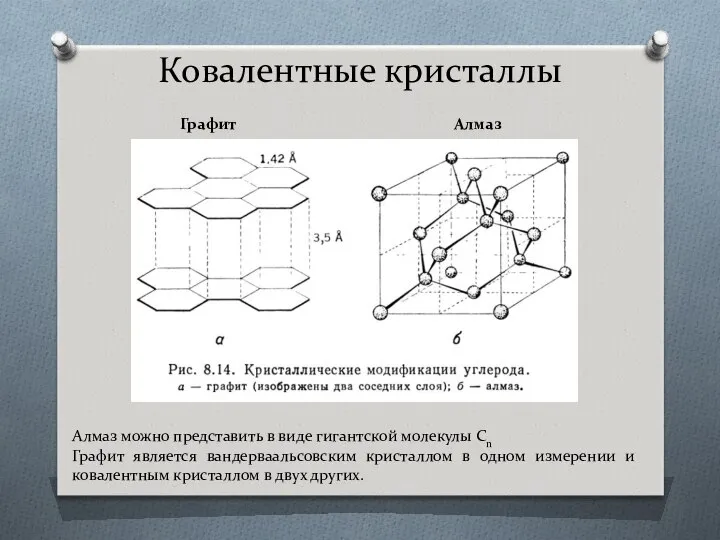
- 43. Ковалентные кристаллы Графит Алмаз Алмаз можно представить в виде гигантской молекулы Cn Графит является вандерваальсовским кристаллом
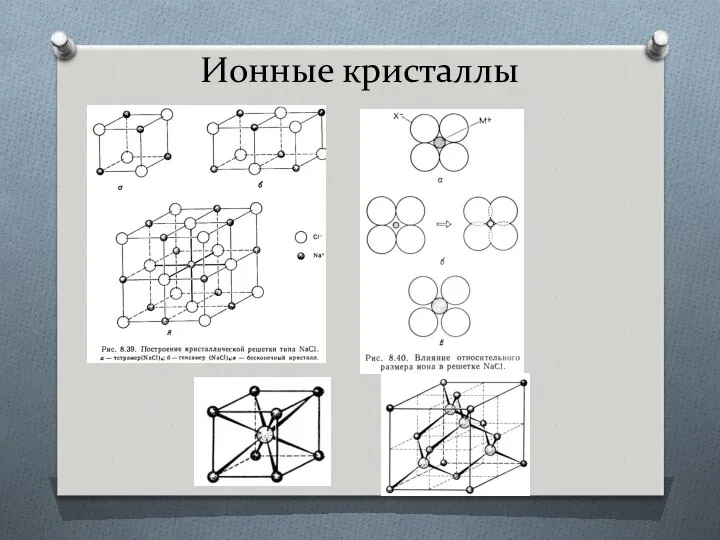
- 44. Ионные кристаллы
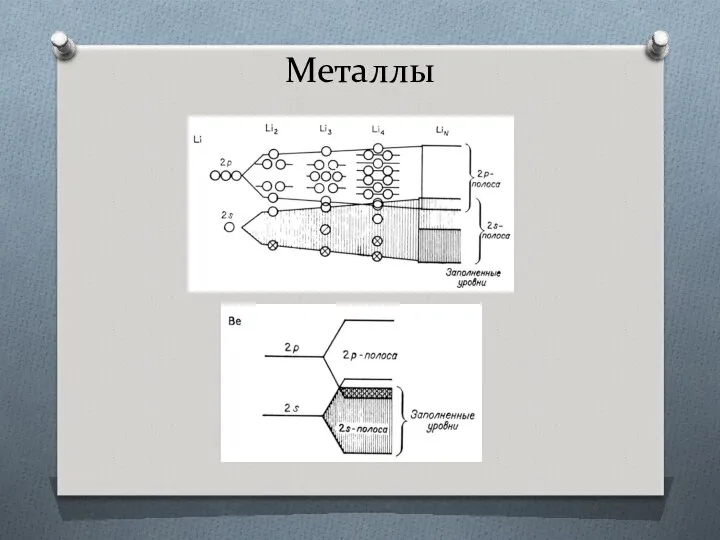
- 45. Металлы Каждая МО охватывает всю цепь атомов лития, а в трех измерениях – весь кристалл. Это
- 46. Металлы
- 47. Формирование зон Образование зонного энергетического спектра в кристалле является квантово-механическим эффектом и вытекает из соотношения неопределенностей.
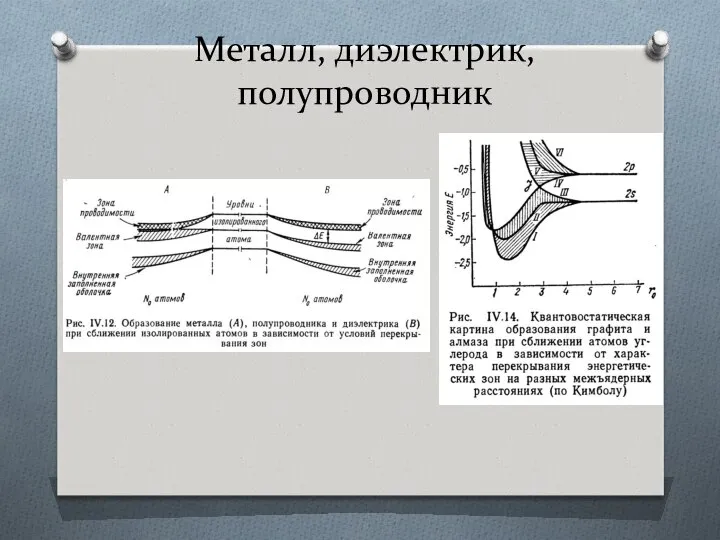
- 48. Металл, диэлектрик, полупроводник
- 49. Активированный кристалл
- 50. Внутрикристаллические поля Различные внутрикристаллические поля: слабое (Vee >> Vso>>Vкр) среднее (Vee >> Vкр>>Vso) сильное (Vкр >>
- 51. Штарковское расщепление
- 52. Внутрикристаллические поля Различные внутрикристаллические поля: слабое (Vee >> Vso>>Vкр) среднее (Vee >> Vкр>>Vso) сильное (Vкр >>
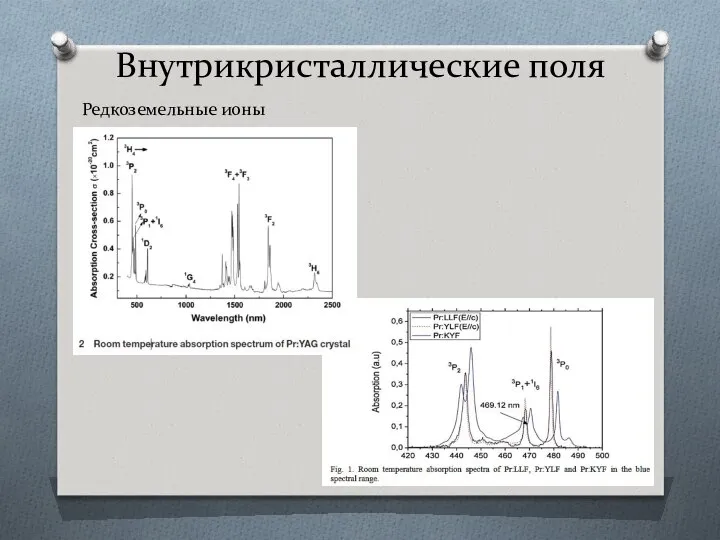
- 53. Внутрикристаллические поля Редкоземельные ионы
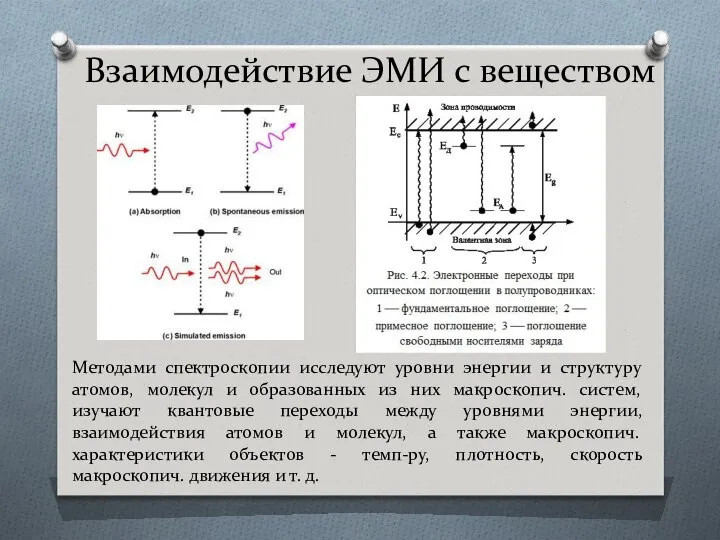
- 54. Взаимодействие ЭМИ с веществом Методами спектроскопии исследуют уровни энергии и структуру атомов, молекул и образованных из
- 55. Электронная конфигурация Определение электронной конфигурации элемента: Принцип заполнения. Согласно принципу заполнения, электроны в основном состоянии атома
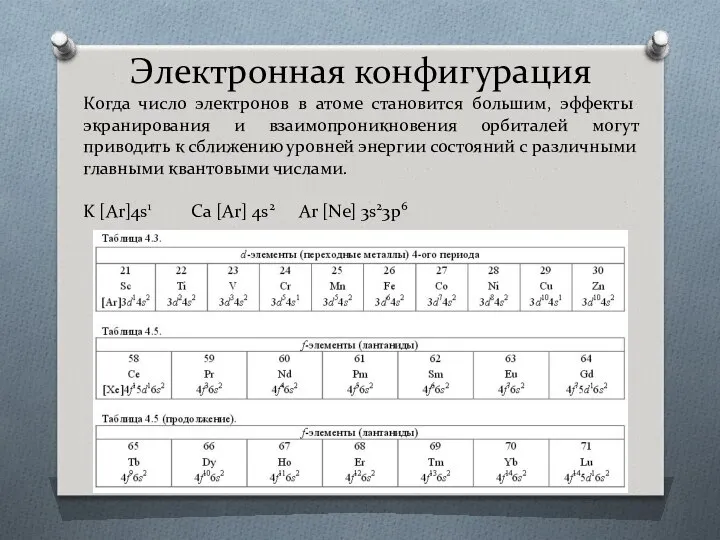
- 56. Электронная конфигурация Когда число электронов в атоме становится большим, эффекты экранирования и взаимопроникновения орбиталей могут приводить
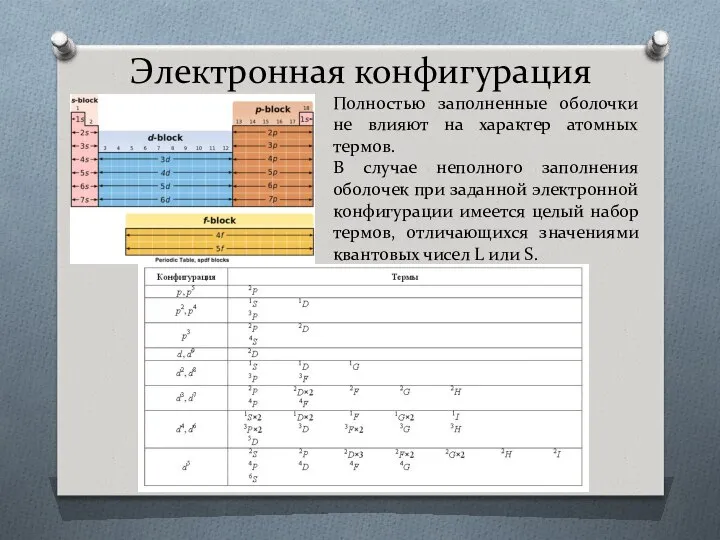
- 57. Электронная конфигурация Полностью заполненные оболочки не влияют на характер атомных термов. В случае неполного заполнения оболочек
- 58. Расщепление уровней Кулоновское взаимодействие между электронами и ядерным зарядом и электростатическое отталкивание электронов друг от друга.
- 60. Скачать презентацию































 Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян
Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян Оксиды азота
Оксиды азота Аэробное окисление углеводов
Аэробное окисление углеводов Простые и сложные вещества. Химический элемент
Простые и сложные вещества. Химический элемент Иммунохимические методы детекции
Иммунохимические методы детекции Кремний. Нахождение в природе. Свойства
Кремний. Нахождение в природе. Свойства Способы разделения смесей
Способы разделения смесей Презентация по Химии "Органічні розчинники" - скачать смотреть бесплатно
Презентация по Химии "Органічні розчинники" - скачать смотреть бесплатно Химия атмосферы
Химия атмосферы ЧИСТЫЕ ВЕЩЕСТВА СМЕСИ
ЧИСТЫЕ ВЕЩЕСТВА СМЕСИ Значение органической химии Кондрашов Алексей | 9 А класс
Значение органической химии Кондрашов Алексей | 9 А класс  Классы неорганических соединений
Классы неорганических соединений Спирты. Классификация спиртов
Спирты. Классификация спиртов Углеводы. Моносахариды
Углеводы. Моносахариды Распределение электронов в атомах. Энергетические уровни
Распределение электронов в атомах. Энергетические уровни Липидтердің метаболизмі
Липидтердің метаболизмі Электроизоляционные материалы. Лаки и класки
Электроизоляционные материалы. Лаки и класки Неорганические соединения. Тест
Неорганические соединения. Тест Презентация по Химии "Вода найпоширеніша речовина на планеті. розчини у природі та побуті. Приготування розчинів. Практична роб
Презентация по Химии "Вода найпоширеніша речовина на планеті. розчини у природі та побуті. Приготування розчинів. Практична роб Презентация по Химии "Йод и здоровье человека" - скачать смотреть
Презентация по Химии "Йод и здоровье человека" - скачать смотреть  История получения алюминия. Применение
История получения алюминия. Применение Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Моносахариды
Моносахариды Методичне об'єднання учителів біології та хімії Христинівської спеціалізованої школи І – ІІІ ступенів ім. О.Є.Корнійчука
Методичне об'єднання учителів біології та хімії Христинівської спеціалізованої школи І – ІІІ ступенів ім. О.Є.Корнійчука Коррозия железа в различных средах Проект по химии: Авторы: ученица 10б класса
Коррозия железа в различных средах Проект по химии: Авторы: ученица 10б класса  Гибридизация атома углерода
Гибридизация атома углерода Дисперсные системы
Дисперсные системы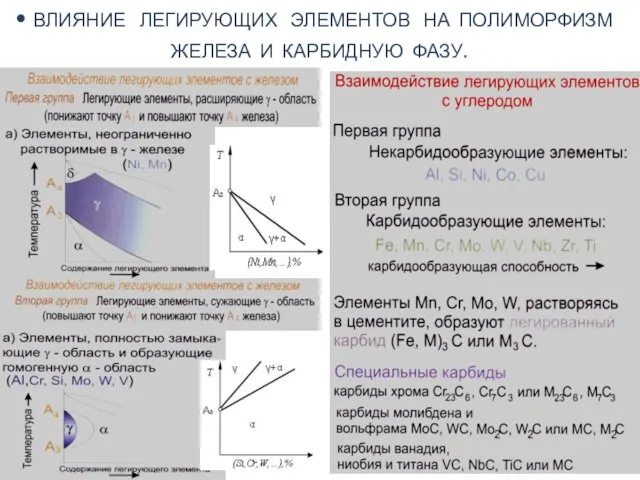 Влияние легирующих элементов на полиморфизм железа и карбидную фазу
Влияние легирующих элементов на полиморфизм железа и карбидную фазу