Содержание
- 6. Образующиеся в результате реакции агрегаты AgI адсорбируют на своей поверхности те ионы, которые способны достраивать кристаллическую
- 7. Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра за счет электростатических и адсорбционных
- 8. В качестве еще одного примера рассмотрим строение коллоидных частиц (мицелл) сульфата бария, полученного в реакции обмена
- 10. Скачать презентацию
Слайд 2
Слайд 3
Слайд 4
Слайд 5
Слайд 6
Образующиеся в результате реакции агрегаты AgI адсорбируют на своей поверхности те
Образующиеся в результате реакции агрегаты AgI адсорбируют на своей поверхности те
ионы, которые способны достраивать кристаллическую решетку AgI (правило Панета – Фаянса).
В данном случае ионы I- взяты в недостатке, поэтому агрегат AgI адсорбирует ионы Ag+. Ионы Ag+, сообщившие поверхности этот заряд называются потенциалопределяющими ионами (ПОИ), так как эти ионы определяют знак заряда коллоидной частицы.
К положительно заряженной поверхности образовавшегося ядра мицеллы притягиваются ионы противоположного знака – противоионы (ионы NO3-).
В данном случае ионы I- взяты в недостатке, поэтому агрегат AgI адсорбирует ионы Ag+. Ионы Ag+, сообщившие поверхности этот заряд называются потенциалопределяющими ионами (ПОИ), так как эти ионы определяют знак заряда коллоидной частицы.
К положительно заряженной поверхности образовавшегося ядра мицеллы притягиваются ионы противоположного знака – противоионы (ионы NO3-).
Слайд 7
Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра
Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра
за счет электростатических и адсорбционных сил. Ядро вместе с адсорбционным слоем составляет коллоидную частицу. В данном примере она заряжена положительно (так же, как ПОИ).
Слайд 8
В качестве еще одного примера рассмотрим строение коллоидных частиц (мицелл)
В качестве еще одного примера рассмотрим строение коллоидных частиц (мицелл)
сульфата бария, полученного в реакции обмена между сульфатом калия и хлоридом бария:
Na2SO4 + BaCl2 = BaSO4 + 2 NaCl
Для получения устойчивого золя необходимо, чтобы один из электролитов (Na2SO4 или BaCl2) присутствовал в избытке в качестве стабилизатора.
В этих условиях нерастворимое вещество не выпадает в осадок, а переходит в коллоидное состояние – образуется золь. Нерастворимое вещество, образовавшееся в результате реакции, называют зародышем или агрегатом и обозначают
BaSO4 . Коэффициент m указывает число частиц вещества.
Na2SO4 + BaCl2 = BaSO4 + 2 NaCl
Для получения устойчивого золя необходимо, чтобы один из электролитов (Na2SO4 или BaCl2) присутствовал в избытке в качестве стабилизатора.
В этих условиях нерастворимое вещество не выпадает в осадок, а переходит в коллоидное состояние – образуется золь. Нерастворимое вещество, образовавшееся в результате реакции, называют зародышем или агрегатом и обозначают
BaSO4 . Коэффициент m указывает число частиц вещества.
- Предыдущая
Молекулярные массы и гибкость полимеровСледующая -
Организация физической защиты ДРМ






 Поширення солей у природі
Поширення солей у природі Органические соединения амины
Органические соединения амины Chemophobia
Chemophobia Тема урока «Важнейшие соединения серы». Цель: рассмотреть свойства важнейших соединений серы-сероводорода, оксидов серы (IV) и (V
Тема урока «Важнейшие соединения серы». Цель: рассмотреть свойства важнейших соединений серы-сероводорода, оксидов серы (IV) и (V Харчові добавки і їх вплив на організм людини
Харчові добавки і їх вплив на організм людини  Связующие для полимерных композиционных материалов. (Тема 2)
Связующие для полимерных композиционных материалов. (Тема 2) Аттестационная работа. Методическая разработка занятия клуба Я – исследователь по теме Волшебное вещество ‒ соль
Аттестационная работа. Методическая разработка занятия клуба Я – исследователь по теме Волшебное вещество ‒ соль Презентация Принципы гормональной и нейромедиаторной регуляции
Презентация Принципы гормональной и нейромедиаторной регуляции 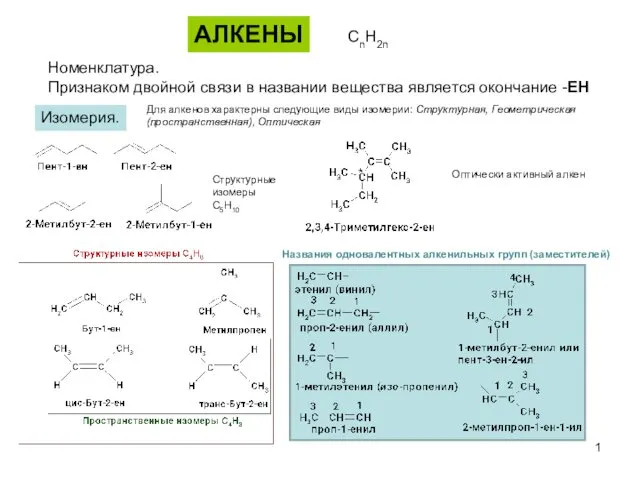 Алкены
Алкены Современные сплавы на основе циркония
Современные сплавы на основе циркония Опал
Опал Химия Кислотные дожди.
Химия Кислотные дожди.  Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Амилаза. Строение амилазы
Амилаза. Строение амилазы Яблочная кладовая Автор работы: Быстрова Анастасия, ученица 9«А» класса Руководитель: Баранова Алевтина Владимировна 2010
Яблочная кладовая Автор работы: Быстрова Анастасия, ученица 9«А» класса Руководитель: Баранова Алевтина Владимировна 2010 Технологічні і біохімічні властивості м‘яса та м‘ясопродуктів. Будова тканин живих організмів
Технологічні і біохімічні властивості м‘яса та м‘ясопродуктів. Будова тканин живих організмів Презентация по Химии "Діопсид силікати" - скачать смотреть
Презентация по Химии "Діопсид силікати" - скачать смотреть  Физические свойства минералов
Физические свойства минералов Органическая химия. Скорость химических реакций
Органическая химия. Скорость химических реакций Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия
Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия  Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Название работы: «Выращивание кристаллов из водного раствора методом охлаждения »
Название работы: «Выращивание кристаллов из водного раствора методом охлаждения » Мұнай
Мұнай Презентація на тему: “Мінеральні добрива” Підготував: Учень 10-А класу Матвійчук Роман
Презентація на тему: “Мінеральні добрива” Підготував: Учень 10-А класу Матвійчук Роман  Моносахариды, глюкоза
Моносахариды, глюкоза Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготував
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготував Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции