Содержание
- 2. В KFeF4 , т.е. K[FeF2/1F4/2] это уже неочевидно, т.к. октаэдры связаны вершинами или рёбрами, катионы сближены,
- 3. Между атомами р-элементов максимальный порядок связи равен 3 (одна ϭ- и две π-связи, а с участием
- 4. Смешанновалентные соединения d-эементов (правильнее было бы говорить «соединения с дробной степенью окисления) Это соединения, где один
- 5. Оксидные бронзы переходных металлов (не путать со сплавами металлов на основе меди!) – это нестехиометрические проводящие
- 6. Основные идеи теории кристаллического поля (ТКП) 1) Пять d-орбиталей имеют одинаковую энергию только в отсутствие внеш-него
- 7. 4) Заселение расщеплённого d-подуровня подчиняется общим принципам: запрету Паули, стремлению к минимуму орбитальной энергии и к
- 8. Надо учитывать энергию спаривания Р – энергию, которую нужно затратить на преодоление межэлек-тронного отталкивания при переносе
- 9. Энергия стабилизации кристаллическим полем (ЭСКП) Это дополнительный вклад в энергию связи сверх кулоновского притяже-ния, обусловленный тем,
- 10. Отклонения от монотонности на графике ΔН от Z (см. предыдущий слайд) соответствуют ЭСКП в слабом октаэдрическом
- 11. При восьми d-электронах в октаэдрическом окружении – максимально возможная ЭСКП . Как видно из рисунка, тетрагональное
- 12. Теорема Яна-Теллера. В упрощённой формулировке она гласит: всякая нели-нейная структура, где орбитали одного подуровня заселены неравномерно,
- 13. Кроме немонотонного изменения термохимических характеристик, ТКП также объясняет немонотонности в изменении ионных радиусов и харак-терных степеней
- 14. Ковалентные эффекты в химии катионов d-элементов Если мы приписываем металлу положительную степень окисления, значит, имеем в
- 15. Ковалентные эффекты в химии катионов d-элементов Если мы приписываем металлу положительную степень окисления, значит, имеем в
- 16. Из приведённой выше схемы, что с лигандами - π-акцепторами наиболее прочно связываются катионы π-доноры – имеющие
- 17. Первый вариант благоприятствует появлению сегнетоэлектричества в каркасных структурах, второй – пониженной связности структур: на концевом анионе
- 18. Классификация d0- и d1-катионов по их склонности к асимметрии π-связывания в кислородных октаэдрах (чётко коррелирует с
- 19. Так называемый “цирконилхлорид ZrOCl2*8H2O”, а фактически – [Zr4(OH)8(OH2)16]Cl8*12H2O: никаких связей Zr-Cl и никакого цирконила ZrO2+: КЧ
- 20. Координационные предпочтения катионов d-элементов У мелких катионов (V5+, Mo6+. W6+) есть тенденция к тетраэдрической коорди-нации, у
- 22. Скачать презентацию
В KFeF4 , т.е. K[FeF2/1F4/2] это уже неочевидно, т.к. октаэдры связаны
В KFeF4 , т.е. K[FeF2/1F4/2] это уже неочевидно, т.к. октаэдры связаны
– при переходе от вершинного соединения к рёберному и гранному расстоя-ния металл-металл уменьшаются и вероятность взаимодействия растёт;
– по периоду слева направо с ростом заряда ядра d-орбитали сжимаются и возможности для взаимодействия металл-металл уменьшаются. Пример: оксиды MO типа NaCl
M расстояние М-М, Å Вывод о связях M-M в оксиде МО
в металле в оксиде
Ca 3,94 3,39
Ti 2,96 3,00
Ni 2,49 2,96
нет, т.к. нет электронов для этого; диэлектрик
есть: есть электроны, расстояние позволяет; металл
нет, т.к. расстояние большое; диэлектрик
– 3d-орбитали кайносимметричные (имеют один максимум в радиальном распределении электронной плотности), а 4d- и 5d-орбитали некайносимме-тричные, более протяжённые в пространстве, легче вовлекаются в связи, поэтому у тяжёлых d-элементов – в 5-м и 6-м периодах – взаимодействие металл-металл более вероятно.
Между атомами р-элементов максимальный порядок связи равен 3 (одна ϭ-
Между атомами р-элементов максимальный порядок связи равен 3 (одна ϭ-
В низших оксидах и галогенидах 4d- и 5d-элементов (NbO, MoO2, W6Br14, ReCl3 и т.п.) при большом содер-жании М неизбежны короткие расстояния М-М и связи М-М. Один пример – октаэдрический кластер – показан на рисунке. Заметьте, что, в отличие от ранее рассмотренных октаэдрических групп МХ6, вершины октаэдра связаны не с центральным атомом (его нет!), а друг с другом. 6 концевых Br присоединены к шести вершинам, а 8 мостиковых Br – к восьми граням октаэдра, т.е имеют КЧ 3.
Четверная связь Cr-Cr в молекуле ацетата Cr(2+): Cr2(CH3COO)4*2H2O
Смешанновалентные соединения d-эементов
(правильнее было бы говорить «соединения с дробной степенью
Смешанновалентные соединения d-эементов
(правильнее было бы говорить «соединения с дробной степенью
Это соединения, где один и тот же d-элемент формально находится в двух разных степенях окисления. При этом ионные радиусы мало отличаются, т.к. главное квантовое число n одинаковое, в отличие от катионов р-элементов, таких, как Pb2+ (n=6) и Pb4+ (n=5). Если позиции таких катионов эквивалент-ны или хотя бы сходны, то они могут легко обмениваться электроном, что ведёт, в зависимости от обстоятельств, к полупроводниковым, металличес-ким или даже сверхпроводниковым свойствам. Примеры.
Стехиометрический NiO типа NaCl – диэлектрик, а с акцепторной примесью лития – дырочный полупроводник Li+xNi3+xNi2+1-2xO.
La2CuO4 (его слоистая структура уже рассмотрена в задаче по модели элементарной ячейки) – полупроводник, а с акцепторной примесью строн-ция (La2-xSrxCuO4) или донорной примесью тория (La2-xThxCuO4) – металл, а ниже ~35 К– сверхпроводник, родоначальник большого семейства ВТСП: Ba2YCu3O7, Ba2HgCuO4±x…
Тип взаимодействия может зависеть и от температуры. В тетрагональном VO2 типа рутила выше ~90°C два расстояния V-V одинаковые: по 2,85 Å, а ниже этой Т фаза моноклинно искажается, и в ней чередуются короткие и длинные расстояния V-V: 2,60 и 3,19 Å. Какая из фаз – диамагнитный полупроводник, а какая – парамагнитный металл?
Оксидные бронзы переходных металлов (не путать со сплавами металлов на основе
Оксидные бронзы переходных металлов (не путать со сплавами металлов на основе
A = K – 2/5 пятиугольных (КЧ 15), 1/5 квадратных (КЧ 12) и 2/5 треугольных (КЧ 9), пригодных лишь для мелких катионов вроде Li+. Следовательно, предельное содержание калия х=3/5: 0,4≤x≤0,6, тип ТВБ. A = K, Rb, Cs – 1/3 шестиугольных и 2/3 треугольных каналов, х≤0,33, тип ГВБ. Везде – метал-
лическая проводимость на уровне меди, интенсивная окраска, блеск. Но по механическим свойствам это типичные ионно-ковалентные кристаллы.
Не бронзы, а диэлектрики и даже сегнетоэлектрики типа ТВБ: Ba2NaNb5O15, PbNb2O6, K3Li2Nb5O15…
Основные идеи теории кристаллического поля (ТКП)
1) Пять d-орбиталей имеют одинаковую энергию
Основные идеи теории кристаллического поля (ТКП)
1) Пять d-орбиталей имеют одинаковую энергию
2) В любом случае сохраняется центр тяжести подуровня на шкале энергии.
3) Лиганды (анионы или полярные молекулы) – считаются точечными отрицательными зарядами, без учёта их электронной структуры.
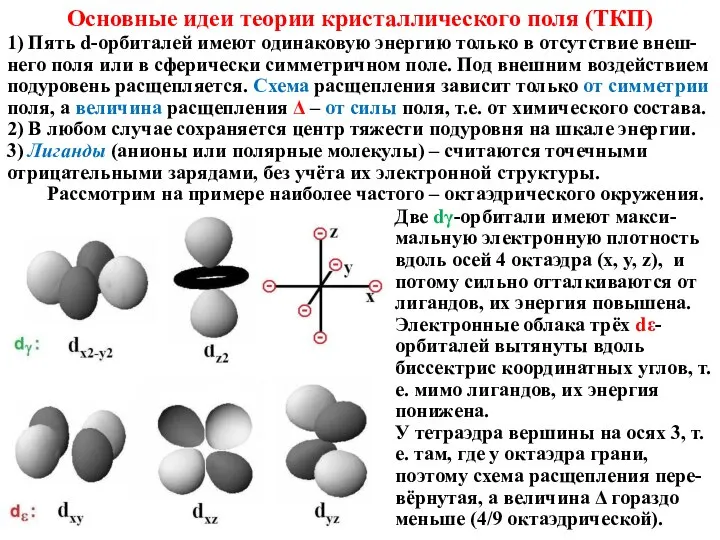
Рассмотрим на примере наиболее частого – октаэдрического окружения.
Две dγ-орбитали имеют макси-мальную электронную плотность вдоль осей 4 октаэдра (x, y, z), и потому сильно отталкиваются от лигандов, их энергия повышена. Электронные облака трёх dε-орбиталей вытянуты вдоль биссектрис координатных углов, т.е. мимо лигандов, их энергия понижена.
У тетраэдра вершины на осях 3, т.е. там, где у октаэдра грани, поэтому схема расщепления пере-вёрнутая, а величина Δ гораздо меньше (4/9 октаэдрической).
4) Заселение расщеплённого d-подуровня подчиняется общим принципам: запрету Паули, стремлению к
4) Заселение расщеплённого d-подуровня подчиняется общим принципам: запрету Паули, стремлению к
Надо учитывать энергию спаривания Р – энергию, которую нужно затратить на
Надо учитывать энергию спаривания Р – энергию, которую нужно затратить на
Δ
Δ>P – сильное поле, низкоспиновое состояние (НС). 2) Номер периода: как уже сказано, 4d- и 5d-орбитали – более протяжённые в пространстве , чем 3d-АО, поэтому сильнее взаимодействуют с лигандами, а два электрона на одной АО слабее отталкиваются → почти всегда Δ>P . 3d 4d, 5d
Эти два состояния объективно различимы по магнитным измерениям, а также по длинам и прочности связей.
Факторы, влияющие на величину расщепления.
1) Форма окружения. Как уже сказано, при прочих равных условиях Δ(тетр.) ≈ 4Δ(окт.)/9
3) Природа лиганда. В рамках ТКП она не
рассматривается, но на основе положения мак-
симума в спектрах поглощения света можно
сравнить величины Δ и расположить лиганды по возрастанию Δ в спектро-химический ряд: Cl– < F– < OH– < H2O < NH3 < NO2– < CN–
4) Степень окисления. С её повышением уменьшается радиус, усиливается влияние лигандов, растёт Δ. Например, в октаэдрическом окружении из молекул NH3 катион Со2+ – высокоспиновый, а Со3+ – низкоспиновый.
тетраэдр ВС ???
октаэдр НС или ВС НС
Энергия стабилизации кристаллическим полем (ЭСКП)
Это дополнительный вклад в энергию связи сверх
Энергия стабилизации кристаллическим полем (ЭСКП)
Это дополнительный вклад в энергию связи сверх
б) ЭСКП (НС) = 6*2Δ/5 – 2Р = 12Δ/5 – 2Р. ЭСКП (НС) – ЭСКП (ВС) = 2(Δ – Р).
Отклонения от монотонности на графике ΔН от Z (см. предыдущий слайд)
Отклонения от монотонности на графике ΔН от Z (см. предыдущий слайд)
При восьми d-электронах в октаэдрическом окружении – максимально возможная ЭСКП .
При восьми d-электронах в октаэдрическом окружении – максимально возможная ЭСКП .
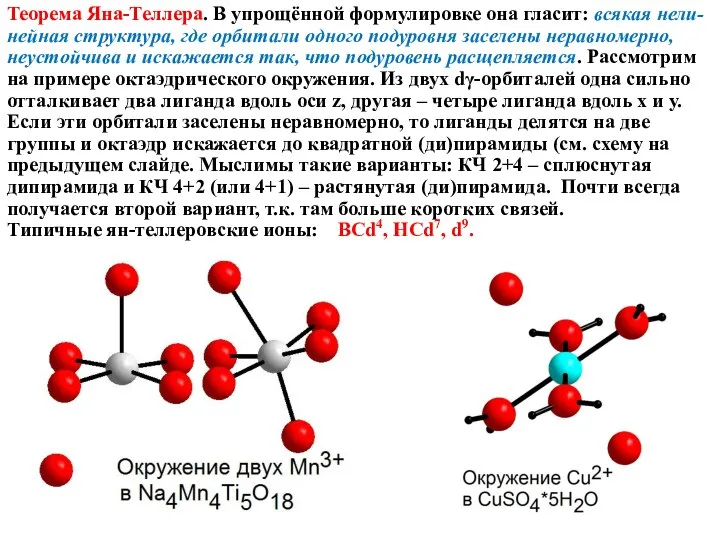
Теорема Яна-Теллера. В упрощённой формулировке она гласит: всякая нели-нейная структура, где
Теорема Яна-Теллера. В упрощённой формулировке она гласит: всякая нели-нейная структура, где
Типичные ян-теллеровские ионы:
ВСd4, НСd7, d9.
Кроме немонотонного изменения термохимических характеристик, ТКП также объясняет немонотонности в изменении
Кроме немонотонного изменения термохимических характеристик, ТКП также объясняет немонотонности в изменении
Почему у Cr и Fe наиболее типичная степень окисления 3, а у Mn, который стоит между ними, не 3, а 2 и 4?
Наиболее устойчивы наполовину и пол-ностью заполненные конфигурации.
В октаэдрическом окружении это:
d3: Cr3+, Mn4+
ВС d5: Mn2+, Fe3+
НС d6: Fe2+, Co3+, Pd4+, Pt4+
d8: Ni2+
Почему Cr5+, Mn5+, Mn6+ менее устойчивы, чем Cr6+, Mn7+? Для октаэдра они малы, а в тетраэдрическом поле ЭСКП мала. Поэ-тому выгодно диспропорционирование на d0 в тетраэдрической координации и d3 в октаэдрической с большой ЭСКП: на
Cr6+ + Cr3+ и Mn7+ + Mn4+
Ковалентные эффекты в химии катионов d-элементов
Если мы приписываем металлу положительную степень
Ковалентные эффекты в химии катионов d-элементов
Если мы приписываем металлу положительную степень
пригодны для ϭ-связи с лигандами, а оставшиеся три dε-АО по симметрии пригодны для π-связи. И тут возможны три варианта:
1) Лиганды – π-доноры (О2- и т.п), dε-подуровень – π-разрыхляющий, параметр расщепления Δ мал.
2) Лиганды не имеют π-орбиталей (NH3), dε – несвязывающие МО.
3) Лиганды – π-акцепторы (CN–), dε-подуровень – π-связывающий, параметр расщепления Δ велик. Синие – π-орбитали лигандов.
Ковалентные эффекты в химии катионов d-элементов
Если мы приписываем металлу положительную степень
Ковалентные эффекты в химии катионов d-элементов
Если мы приписываем металлу положительную степень
и образуется 6 связывающих ϭ-МО, которые заняты электронами лигандов, и 6 разрыхляющих ϭ-МО. Иэ этих 12 на рис. показаны только две dγ-орбитали, а прочие гораздо ниже (связывающие) или выше. Далее возможны три варианта:
1) Лиганды – π-доноры (О2– и т.п.), dε-подуровень – π-разрыхляющий, параметр расщепления Δ мал.
2) Лиганды не имеют π-орбиталей (NH3), dε – несвязывающие МО.
3) Лиганды – π-акцепторы (CN–), dε-подуровень – π-связывающий, параметр расщепления Δ велик. Синие – π-орбитали лигандов.
Из приведённой выше схемы, что с лигандами - π-акцепторами наиболее прочно
Из приведённой выше схемы, что с лигандами - π-акцепторами наиболее прочно
Асимметрия π-связывания в октаэдрических комплексах
d0- и d1-катионов
Если катион с (почти) пустым d-подуровнем
октаэдрически окружён шестью лигандами π-донорами – например, анионами кислорода, гидроксила, фтора, то на три его π-орбитали претендуют 6 или 12 электронных пар лигандов. По принципу Паули прочная связь с обоими соседями (левым и правым) невозмож-на, приходится выбирать. И чем прочнее связь с левым соседом, тем слабее связь с правым.
Катион смещается из центра октаэдра к одной, двум или трём вершинам:
КЧ 1+4(+1), 2+2+2 или 3+3, так что в транс-положении к самым прочным связям находятся самые слабые. Локальный баланс валентности может обеспечиваться принципиально разными способами: либо у каждого аниона есть одна прочная и одна слабая связь, т.е. существует цепочка с чередованием коротких и длинных связей, либо один из анионов является концевым (КЧ 1), а у транс-партнёра тогда большее КЧ (от 2 до 6!).
Первый вариант благоприятствует появлению сегнетоэлектричества в каркасных структурах, второй – пониженной
Первый вариант благоприятствует появлению сегнетоэлектричества в каркасных структурах, второй – пониженной
КЧ кислорода
V2O5: 1, 2, 3
[Ta6O19]8-: 1, 2, 6
[PMo12O40]3-: 1, 2, 4
Для возникновения такой асимметрии π-связывания нужны следующие условия:
– катион – π-акцептор (d0 или d1);
– лиганды – π-доноры: отрицательно поляризованные атомы кислорода, фтора или азота;
– не слишком большая разница электроотрицательностей, т.е. небольшая степень ионности связи; поэтому эффект сильнее выражен в кислородных соединениях, чем во фторидах, а с титаном – сильнее, чем с цирконием;
– октаэдрическое или близкое к нему окружение.
Если КЧ катиона 4, то девяти его атомных орбиталей хватает для ϭ- и π-связывания со всеми соседями, и асимметрия не возникает. Если катион – π-донор, а все лиганды – одинаковые π-акцепторы, то π-связывание сразу со всеми лигандами не противоречит принципу Паули, и асимметрии тоже нет.
Классификация d0- и d1-катионов по их склонности к асимметрии π-связывания в
Классификация d0- и d1-катионов по их склонности к асимметрии π-связывания в
4 5 6 7 8
Sc3+ Ti4+ V5+,4+ Cr6+ Mn7+ Fe8+ Практически нет;
Y3+ Zr4+ Nb5+ Mo6+.5+ Tc7+ Ru8+ Очень слабо выражена – наиболее
La3+ Hf4+ Ta5+ W6+ Re7+ Os8+ интересно для сегнетоэлектричества; сильно выражена – переполяризация обычно невозможна; мелкие – вряд ли вообще возможно КЧ 6 с О2-
Ванадил VO2+ – реальность, титанил TiO2+ можно усмотреть только очень условно, а «цирконил» ZrO2+ – полная бессмыс-лица (см. следующий слайд). Справа – TcO2F3 – редкий пример Tc(7+) в октаэдре, но искажение типичное: двухвалентные атомы кислорода – концевые (s=2), а в транс-положениях к ним – мостиковые одновалентные F (s=0,5)
Так называемый “цирконилхлорид ZrOCl2*8H2O”, а фактически – [Zr4(OH)8(OH2)16]Cl8*12H2O: никаких связей Zr-Cl
Так называемый “цирконилхлорид ZrOCl2*8H2O”, а фактически – [Zr4(OH)8(OH2)16]Cl8*12H2O: никаких связей Zr-Cl
На предыдущем слайде показано по одному варианту искажения BaTiO3 и KNbO3, но на самом деле у каждого из них при понижении температуры наблюдаются все варианты октаэдров. КЧ: 6 → 1+4+1 → 2+2+2 → 3+3.
Рисунок справа иллюстрирует влия-ние ионности связи на поляризацию и сегнетоэлектрическую температуру Кюри: Nb и Ta – электронные аналоги, их ионные радиусы – одинаковые, и главное различие – в большей ЭО ниобия и, соответственно, более ковалентном характере связи Nb-O.
Координационные предпочтения катионов d-элементов
У мелких катионов (V5+, Mo6+. W6+) есть тенденция
Координационные предпочтения катионов d-элементов
У мелких катионов (V5+, Mo6+. W6+) есть тенденция
![В KFeF4 , т.е. K[FeF2/1F4/2] это уже неочевидно, т.к. октаэдры связаны](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397126/slide-1.jpg)














![Так называемый “цирконилхлорид ZrOCl2*8H2O”, а фактически – [Zr4(OH)8(OH2)16]Cl8*12H2O: никаких связей Zr-Cl](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397126/slide-18.jpg)

 Понятие о качественных реакциях. 9 класс
Понятие о качественных реакциях. 9 класс Металлы. Общая характеристика
Металлы. Общая характеристика Полимеры. Пластмассы
Полимеры. Пластмассы Реакции щелочных металлов (Группа 1) – Li, Na, K
Реакции щелочных металлов (Группа 1) – Li, Na, K Строение атома. (8 класс)
Строение атома. (8 класс) Альдегидная функциональная группа
Альдегидная функциональная группа Кальцит
Кальцит Озон. Аллотропия кислорода
Озон. Аллотропия кислорода Инновационный проект производства фуллеренов
Инновационный проект производства фуллеренов Cromatografia de gaze
Cromatografia de gaze Державна система забезпечення якості лікарських засобів в Україні
Державна система забезпечення якості лікарських засобів в Україні Обмен липидов
Обмен липидов Химический элементы в нашей жизни
Химический элементы в нашей жизни Алканы. Задания
Алканы. Задания Миф о холоде. Задача 7
Миф о холоде. Задача 7 Термореактивные пластмассы (реактопласты)
Термореактивные пластмассы (реактопласты) Структурно-механiчнi (реологiчнi) властивостi харчових мас
Структурно-механiчнi (реологiчнi) властивостi харчових мас Повторительное обобщение по неорганической химии, подготовка к ГИА
Повторительное обобщение по неорганической химии, подготовка к ГИА Химия – наука о веществах, их свойствах и превращениях Урок №1
Химия – наука о веществах, их свойствах и превращениях Урок №1 Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготувал
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготувал Презентация Белки и аминокислоты
Презентация Белки и аминокислоты  Виртуальный урок по химии тема: Химические реакции Практическое занятие Подготовил: Учитель химии МОУ «МЛ №1
Виртуальный урок по химии тема: Химические реакции Практическое занятие Подготовил: Учитель химии МОУ «МЛ №1 Аргентум (Срібло)
Аргентум (Срібло) Комплексные соединения
Комплексные соединения Технология промышленных газов
Технология промышленных газов Презентация по химии «Соли. Названия и классификация солей»
Презентация по химии «Соли. Названия и классификация солей»  Количество вещества
Количество вещества Растворы. Общие свойства растворов
Растворы. Общие свойства растворов