Т 2. Элементы группы VIIA ФТОР Фтор «F» в невозбужденном состоянии имеет электронную конфигурацию: 1s22s22p5. Наличием одног
Содержание
- 2. Фтор – довольно распространенный элемент. Из минералов фтора наибольшее значение имеют СаF2 — плавиковый шпат (флюорит),
- 3. Простое вещество. Подобно водороду фтор образует двухатомные молекулы F2, что соответствует следующей электронной конфигурации: ( σsсв)2
- 4. Молекула фтора F2 имеет относительно небольшую массу и достаточно подвижна, поэтому фтор в обычных условиях —
- 5. Вследствие высокой химической активности фтор вызывает коррозию почти всех материалов. В качестве материала аппаратуры для получения
- 6. Широкое применение фтора началось в связи с работами по разделению изотопов урана (в виде 235UF6 и
- 7. Фтор исключительно активен химически, он — сильнейший окислитель. Высокая химическая активность фтора объясняется тем, что его
- 8. По образному выражению акад. А. Е. Ферсмана, фтор «всесъедающий». В атмосфере фтора горят такие стойкие вещества,
- 9. Исключительно активно протекает взаимодействие фтора с большинством простых веществ. С серой и фосфором он взаимодействует даже
- 10. Фтор окисляет некоторые так называемые инертные газы: (при нормальном Р) Хе + 2F2 = ХеF4(к), ΔНo298
- 11. Е АОF MOXeF AOXe σразр σ 5p 2р σсв В линейной молекуле ХеF2 за счет одной
- 12. В соответствии с закономерным изменением характера элементов по периодам и группам периодической системы закономерно изменяются и
- 13. Ионные фториды кристаллические вещества с высокой температурой плавления. Координационное число иона фтора 6 (NаF) или 4
- 14. Многие фториды металлов в низких степенях окисления получают действием раствора HF на оксиды, гидроксиды, карбонаты и
- 15. По химической природе ионные фториды являются основными соединениями, а ковалентные фториды — кислотными. Так в реакции
- 16. Основные фториды при гидролизе создают щелочную среду, а кислотные фториды — кислотную NaF + H2O =
- 17. В неводных растворах PF5 взаимодействует с основными фторидами KF + PF5 = KPF6 С жидким HF
- 18. Комплексные фториды весьма разнообразны. Координационное число по фтору для элементов 2-го периода равно 4, для элементов
- 19. Фтор со взрывом взаимодействует с водородом даже при низких температурах и (в отличие от хлора) в
- 20. Молекула фторида водорода НF сильно полярна и имеет большую склонность к ассоциации за счет водородных связей
- 21. Собственная ионизация жидкого НF незначительна (К = 2,07⋅10-11). Она происходит путем перехода протона (или соответственно иона
- 22. Жидкий фторид водорода - сильный ионизирующий растворитель. В нем хорошо растворяются вода, фториды, сульфаты и нитраты
- 23. Даже НNО3 в этих условиях ведет себя как основание: НNО3 + 2НF ↔ NО3Н2+ + HF2-
- 24. В жидком НF ведут себя как кислоты вещества — акцепторы фторид-ионов, например BF3, SbF5: BF3 +
- 25. Амфотерными соединениями в жидком НF являются, например, фториды алюминия и хрома (III): 3NаF + АIF3 =
- 26. HF неограниченно растворяется в воде. HF ионизируется с образованием ионов OH3+ и F-. Последние взаимодействуя с
- 27. При нейтрализации HF образуются фторогидрогенаты 2HF + KOH = K[HF2] + H2O КНF2, КH2F3, КH3F4, КH4F5
- 28. Термическое разложение фторогидрогенатов используется для получения чистого НF и фторида металла: KHF2 = KF + HF
- 29. Характерная особенность плавиковой кислоты (фтористоводородной = фтороводородной) ее способность взаимодействовать с диоксидом кремния: SiO2 (к) +
- 30. В соединениях со фтором у кислорода проявляется электроположительная поляризация атомов. Простейший представитель такого рода соединений —
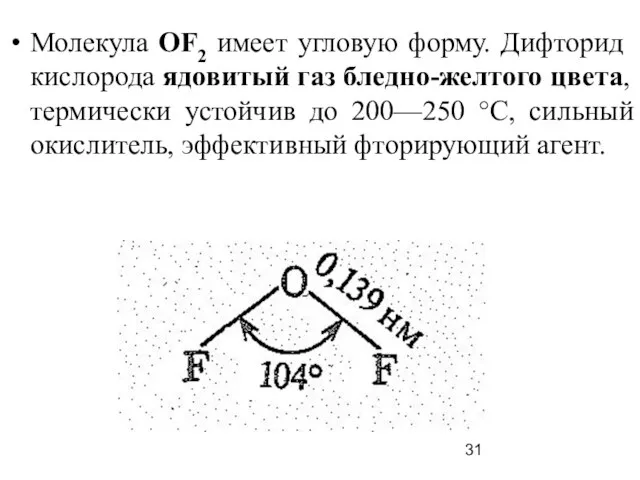
- 31. Молекула ОF2 имеет угловую форму. Дифторид кислорода ядовитый газ бледно-желтого цвета, термически устойчив до 200—250 °С,
- 32. ОF2 довольно легко гидролизуется основаниями, водой – гораздо медленнее: OF2 + 2NaOH = 2NaF + O2
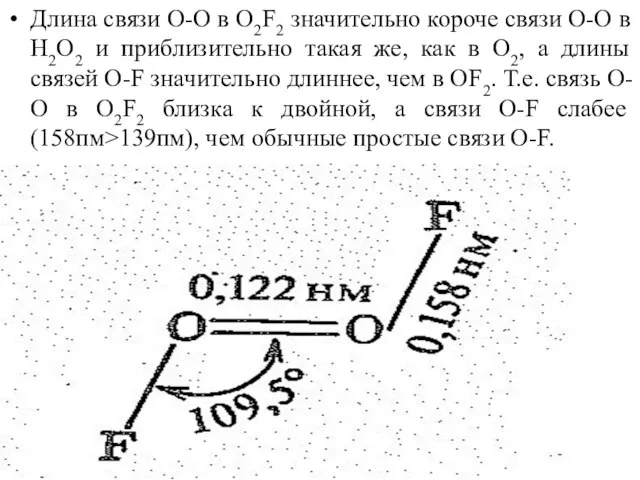
- 33. Длина связи О-О в О2F2 значительно короче связи О-О в Н2О2 и приблизительно такая же, как
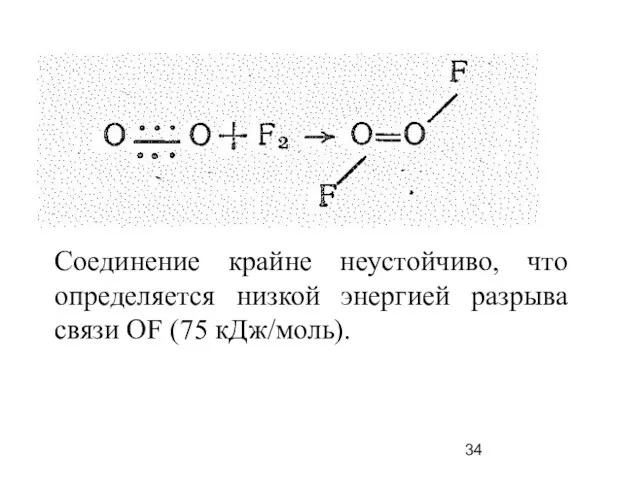
- 34. Соединение крайне неустойчиво, что определяется низкой энергией разрыва связи ОF (75 кДж/моль).
- 36. Скачать презентацию

























![При нейтрализации HF образуются фторогидрогенаты 2HF + KOH = K[HF2] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1198770/slide-26.jpg)




 Каталитический крекинг
Каталитический крекинг Валетные состояния атома углерода
Валетные состояния атома углерода Типы метаморфизма
Типы метаморфизма Рідкісні кристали і полімери. Їх властивості та застосування
Рідкісні кристали і полімери. Їх властивості та застосування Понятие о композиционных материалах. Лекция 2
Понятие о композиционных материалах. Лекция 2 Электрофильные реакции
Электрофильные реакции Губна помада та ії призначення
Губна помада та ії призначення Презентация по Химии "Комплексные соединения: строение, изомерия, использование в онкологии" - скачать смотреть
Презентация по Химии "Комплексные соединения: строение, изомерия, использование в онкологии" - скачать смотреть  Углерод, аллотропные модификации
Углерод, аллотропные модификации Ацетилен и его гомологи
Ацетилен и его гомологи Уксусная кислота
Уксусная кислота Характеристика ядов, изолируемых минерализацией в клинической фармации
Характеристика ядов, изолируемых минерализацией в клинической фармации Многоатомные спирты
Многоатомные спирты Растворы. Классификация
Растворы. Классификация Химическая промышленность
Химическая промышленность Основные методы получения моно- и поликристаллического SiC. Диаграмма состояния
Основные методы получения моно- и поликристаллического SiC. Диаграмма состояния Кадмий
Кадмий Степень диссоциации. 9 класс
Степень диссоциации. 9 класс Обмен триацилглицеролов и жирных кислот
Обмен триацилглицеролов и жирных кислот Насыщенные углеводороды
Насыщенные углеводороды Хімія в житті суспульства
Хімія в житті суспульства Мұнай. Мұнайдың химиялық құрамы
Мұнай. Мұнайдың химиялық құрамы Минерал гранат
Минерал гранат Растворы. Определения и понятия
Растворы. Определения и понятия Геохимические классификации элементов
Геохимические классификации элементов Углеводный обмен
Углеводный обмен Прості й складні речовини. Хімічні формули
Прості й складні речовини. Хімічні формули  Физико-химиеские методы анализа (ФХМА)
Физико-химиеские методы анализа (ФХМА)