Содержание
- 2. Раствор состоит из растворенного вещества и растворителя. Растворителем считают тот компонент, агрегатное состояние которого не изменяется
- 3. В зависимости от агрегатного состояния растворителя растворы бывают: газовые (воздух –растворенные друг в друге азот, кислород,
- 4. Вода – бесцветная, прозрачна жидкость, может существовать в 3 агрегатных состояниях – жидком, твердом (лед) и
- 5. Кристаллизация воды сопровождается увеличением объема. Кристаллы воды образуют решетку молекулярного типа. Слабый электролит. Сравнительно высокая температура
- 6. Молекула воды - равнобедренный треугольник, образованный ядрами атомов водорода и кислорода.
- 7. Связь ковалентная полярная, что приводит к асимметрии распределения зарядов и полярности молекулы – молекула диполь. У
- 8. Химическая теория растворов Д.И. Менделеева Растворение – физико-химический процесс, который в зависимости от природы веществ –
- 9. Растворение сопровождается увеличением энтропии системы (ΔS > 0), с этим связана самопроизвольность процесса растворения, даже, если
- 10. Химическая теория растворов Д.И. Менделеева: вещества растворяясь в воде образуют с ней химические соединения – гидраты,
- 11. сольваты и гидраты образованы либо силами электростатического притяжения (диполь - дипольное взаимодействие), либо донорно-акцепторным взаимодействием; гидраты
- 12. гидраты, у которых вода входит в состав кристаллов растворенного вещества называются кристаллогидратами, а содержащаяся в них
- 13. Растворимость веществ Растворимость (коэффициент растворимости β [г/100г H2O]) – это масса вещества, которая может раствориться при
- 14. По растворимости в воде вещества делятся на: растворимые (Р) – β >1 [г/100г H2O]; малорастворимые (М)
- 15. Растворимость зависит от: природы растворенного вещества; природы растворителя; температуры; давления.
- 16. 1 и 2. Сходство химической природы веществ усиливает их взаимную растворимость: вещества, состоящие из полярных молекул
- 17. 3 и 4. Влияние Т и Р на растворимость регулируется принципом Ле Шателье: при увеличении температуры
- 18. В зависимости от количества вещества, растворенного в растворителе различают: насыщенные растворы – содержащие максимальное количество растворенного
- 19. Ненасыщенные растворы с содержанием растворенного вещества менее 1 моль на 1 литр раствора называются разбавленными, более
- 20. Способы выражения количественного состава растворов 1) Массовая доля Показывает сколько граммов растворенного вещества содержится в 100
- 21. 2) Мольная доля Отношение числа молей растворенного вещества (или растворителя) к сумме молей растворенного вещества и
- 22. 3) Молярная концентрация (молярность) Отношение количества вещества к объему раствору, показывает число молей растворенного вещества в
- 23. 4) Эквивалентная или нормальная концентрация (нормальность) Отношение количества эквивалентов вещества к объему раствору, показывает число эквивалентов
- 24. 5) Моляльная концентрация (моляльность) Отношение количества растворенного вещества к массе растворителя, показывает сколько молей растворенного вещества
- 26. Скачать презентацию











![Растворимость веществ Растворимость (коэффициент растворимости β [г/100г H2O]) – это масса](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1394598/slide-12.jpg)











 Гидролиз. Сущность процесса гидролиза
Гидролиз. Сущность процесса гидролиза Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения Кругообіг Нітрогену
Кругообіг Нітрогену  Химические реактивы
Химические реактивы Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М
Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М Сложные эфиры. 10 класс
Сложные эфиры. 10 класс Алканы. Алкены. Алкины. Задачи урока:
Алканы. Алкены. Алкины. Задачи урока:  Теория резонанса в неорганической химии
Теория резонанса в неорганической химии Пищевые красители
Пищевые красители Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_
Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_ «Уксусная кислота»
«Уксусная кислота»  Физико-химическая и механическая миграция
Физико-химическая и механическая миграция Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс)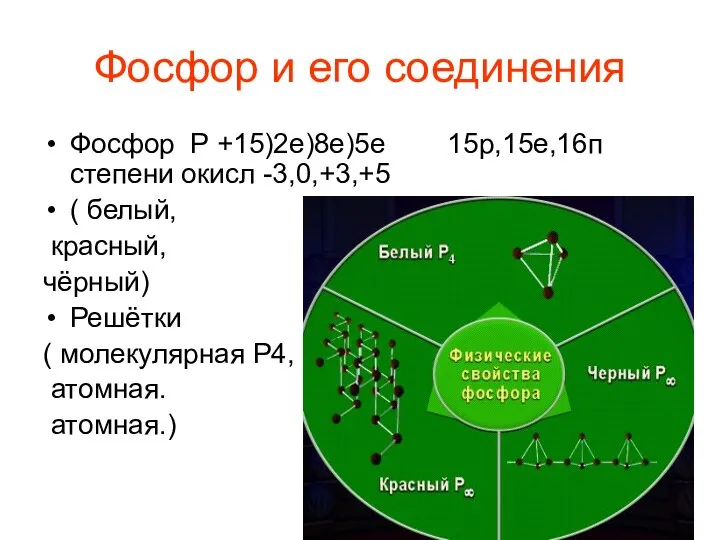 Фосфор и его соединения
Фосфор и его соединения Исследование процесса диффузии на примере движения частиц в жидкостях и газах
Исследование процесса диффузии на примере движения частиц в жидкостях и газах Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Электрометрические методы анализа ЛВ. Термографические методы
Электрометрические методы анализа ЛВ. Термографические методы Янтарь – солнечный камень. Рассказ об удивительном минерале
Янтарь – солнечный камень. Рассказ об удивительном минерале Фармацевтические суспензии и эмульсии
Фармацевтические суспензии и эмульсии Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Галогены: Хлор, бром, иод
Галогены: Хлор, бром, иод Классификация и номенклатура органических соединений
Классификация и номенклатура органических соединений Введение в обмен веществ. Метаболические пути
Введение в обмен веществ. Метаболические пути Залежність фізичних властивостей речовин від типу кристалічних ґраток
Залежність фізичних властивостей речовин від типу кристалічних ґраток Тема урока "Круговорот углерода в природе и последствия его нарушения« Учитель биологии Рабаданова Светлана Ивановна МОУ Лиц
Тема урока "Круговорот углерода в природе и последствия его нарушения« Учитель биологии Рабаданова Светлана Ивановна МОУ Лиц Қызықты химия
Қызықты химия Основы химической кинетики
Основы химической кинетики Трансформация энергии в процессе оксигенного фотосинтеза
Трансформация энергии в процессе оксигенного фотосинтеза