Т 3 Л 7 Подгруппа Селена Селен Sе, теллур Те и полоний Ро р-элементы с конфигурацией валентных электронов s2р4. В образование связей
Содержание
- 2. В подгруппе селена, как и в других подгруппах р-элементов, с увеличением размеров атомов наблюдается общая тенденция
- 3. Собственные минералы селена и теллура встречаются редко. Чаще всего Sе и Те сопутствуют самородной сере и
- 4. Простые вещества. В ряду O—S—Sе—Te—Po тип устойчивых молекул изменяется: от двухатомных кислорода О2, затем циклических S8
- 5. Серый селен — полупроводник (ΔЕ = 1,8 эВ). Его электрическая проводимость резко (примерно в 1000 раз)
- 6. Устойчивые модификации теллура образованы зигзагообразными молекулами Te∞. Гексагональная модификация теллура — серебристо-белое металлоподобное кристаллическое вещество. Однако
- 7. Будучи изоморфными, гексагональные селен и теллур образуют между собой непрерывный ряд твердых растворов. При высоких температурах
- 8. П о л о н и й - мягкий металл серебристо-белого цвета, по физическим свойствам напоминающий
- 9. В ряду O—S—Sе—Te—Po уменьшается окислительная и возрастает восстановительная активность, о чем, в частности, свидетельствует сопоставление их
- 10. S, Se, Te с кислотами-неокислителями не реагируют. При нагревании Se, Te и Po довольно легко окисляются
- 11. Селен и теллур извлекают из отходов производства серной кислоты, накапливающихся в пылеуловителях, и из анодного шлама,
- 12. Соединения со степенью окисления селена, теллура и полония -2. У селена, теллура и полония степень окисления
- 13. По методам получения, кристаллической структуре, растворимости и химическим свойствам селениды и теллуриды аналогичны сульфидам. Среди них
- 14. В соответствии с усилением металлических признаков простых веществ в ряду O—S—Sе—Te—Po возрастает склонность к образованию соединений
- 15. Селенид водорода H2Sе и теллурид водорода H2Те в обычных условиях — газы с очень неприятным запахом,
- 16. В воде Н2Sе и Н2Те растворяются лучше, чем Н2S. Их растворы — слабые кислоты. В ряду
- 17. Соединении селена (II), теллура(II) и полония (II). Из производных Sе(II), Те(II) и Ро(II) лучше других изучены
- 18. Для химии Sе (II) и Те(II) очень характерны реакции диспропорцио-нирования, протекающие при нагревании и гидролизе галогенидов:
- 19. Соединения селена (IV), теллура (IV) и полония (IV). Степень окисления +4 селена, теллура и полония проявляется
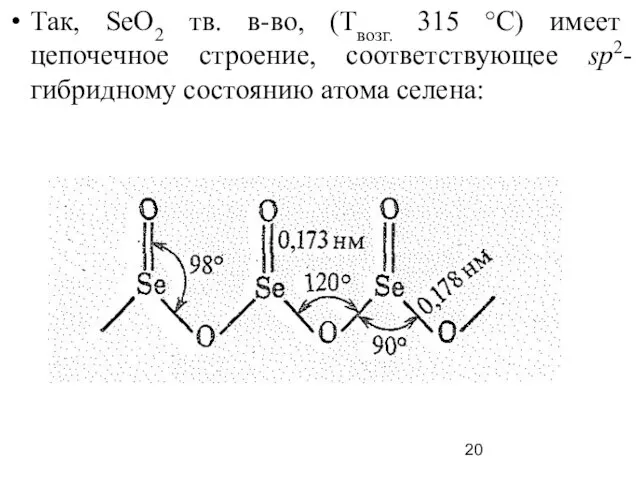
- 20. Так, SеO2 тв. в-во, (Твозг. 315 °С) имеет цепочечное строение, соответствующее sp2-гибридному состоянию атома селена:
- 21. В ряду SеO2—ТеO2—РоO2 отчетливо наблюдается ослабление кислотных свойств. Так, SеO2 легко растворяется в воде, образуя селенистую
- 22. ТеО2 в воде не растворяется, но взаимодействует с растворами щелочей: ТеО2 + 2КОН + 2Н2О =
- 23. В отличие от Н2SО3 триоксоселенат (IV) водорода Н2SеО3 выделен в свободном состоянии. Это — твердое вещество,
- 24. Оксид SеO2 (а также SеО32-) по сравнению с SO2 (в SО32-) проявляют в большей степени окислительные
- 25. Соединения селена (VI), теллура (VI) и полония (VI). Для селена (VI) и теллура (VI) известны бинарные
- 26. Триоксид селена SеO3 (Тпл. 118,5 °С, Tразл. > 185 °С) белого цвета, известен в виде стекловидной
- 27. Триоксид селена SеО3 получают кипячением К2SеO4 с жидким SО3, а ТеО3 — обезвоживанием гексаоксотеллурата (VI) водорода:
- 28. Тетраоксоселенат (VI) водорода H2SеO4 белое кристаллическое вещество (Тпл. 62,4 °С). Как и Н2SO4, он жадно поглощает
- 29. Гексаоксотеллурат (VI) водорода H6TeO6 белое кристаллическое вещество, хорошо растворимое в горячей воде. Теллуровая кислота очень слабая
- 30. Соединения селена (VI) менее устойчивы, чем соответствующие соединения серы (VI). Так, при нагревании SеO3 и Н2SеO4
- 31. Также, Н2SеO4 окисляет концентрированную соляную кислоту: +6 -1 +4 0 Н2SеO4 + 2HCl = Н2SеO3 +
- 32. Помимо полупроводниковой техники соединения селена и теллура используются в органическом синтезе, в частности для получения разнообразных
- 33. Ст. ок. +4 SO2 SeO2 TeO2 PoO2 газ тв. в-во. тв. в-во. крист. бесцв. белый белый
- 34. Ст. ок. +4 Н2SO3 Н2SеO3 Н2ТеO3 неустойч. тв. в-во в раств. в раств. белое полимеризуется сернистая
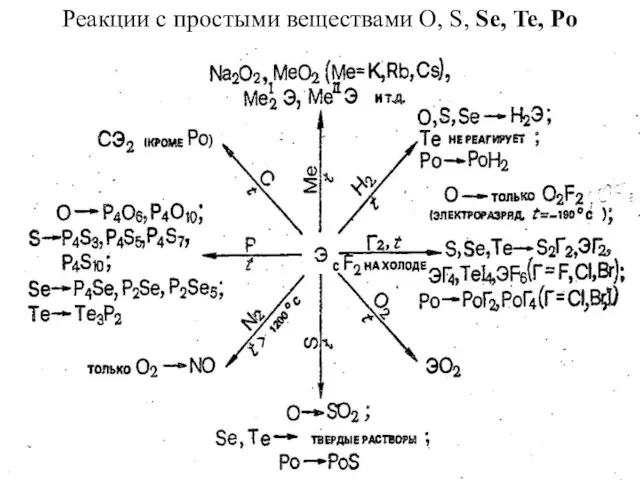
- 35. Реакции с простыми веществами O, S, Se, Te, Po
- 37. Скачать презентацию
































 Биохимия. Лекция 7. Углеводы
Биохимия. Лекция 7. Углеводы Ізогіпсичні перетворення функціональних груп. Реакції заміщення та елімінування
Ізогіпсичні перетворення функціональних груп. Реакції заміщення та елімінування Сера
Сера Азотосодержащие органические соединения
Азотосодержащие органические соединения Век медный, бронзовый, железный Тужилкина Полина 9 Б класс МОУ «СОШ №92»
Век медный, бронзовый, железный Тужилкина Полина 9 Б класс МОУ «СОШ №92» Элементарный состав живых организмов
Элементарный состав живых организмов Геохимия стабильных изотопов, Радиоуглеродный метод
Геохимия стабильных изотопов, Радиоуглеродный метод Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства
Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства Неметаллические материалы
Неметаллические материалы «Строительные материалы»
«Строительные материалы»  Химия и организм человека
Химия и организм человека Подготовлено ученицей 9 "А" класса Михневской СОШ Темновой Яной.
Подготовлено ученицей 9 "А" класса Михневской СОШ Темновой Яной. Некоторые примеры использования Ферментов в промышленности
Некоторые примеры использования Ферментов в промышленности Учение о растворах. Буферные растворы
Учение о растворах. Буферные растворы Презентация по Химии "Белирий, магний и щелочноземельные металлы" - скачать смотреть
Презентация по Химии "Белирий, магний и щелочноземельные металлы" - скачать смотреть  Аттестационная работа. Образовательная программа кружка «Химия и жизнь»
Аттестационная работа. Образовательная программа кружка «Химия и жизнь» Органическая химия
Органическая химия Оксиди Неметалічних Елементів Підготував : Учень 10 Класу Кійко Едуард
Оксиди Неметалічних Елементів Підготував : Учень 10 Класу Кійко Едуард  Биосинтез кортикостероидов из ацетил КоА и ХС
Биосинтез кортикостероидов из ацетил КоА и ХС Крахмал (C6H10O5)n
Крахмал (C6H10O5)n  Аттестационная работа. Задачи на смеси и сплавы
Аттестационная работа. Задачи на смеси и сплавы Характеристика элементов VI-В группы. Хром
Характеристика элементов VI-В группы. Хром Тест по теме «Альдегиды и кетоны»
Тест по теме «Альдегиды и кетоны» Аттестационная работа. Методическая разработка по выполнению проекта Анализ содержания ионов железа (III) в пищевых продуктах
Аттестационная работа. Методическая разработка по выполнению проекта Анализ содержания ионов железа (III) в пищевых продуктах VI A-ХАЛЬКОГЕНЫ О-кислород S-сера Se-селен Te-теллур Ро-полоний VI B Cr-хром Мо-молибден W-вольфрам Rf-резерфордий
VI A-ХАЛЬКОГЕНЫ О-кислород S-сера Se-селен Te-теллур Ро-полоний VI B Cr-хром Мо-молибден W-вольфрам Rf-резерфордий Презентация по Химии "Монооксид углерода: угарный газ" - скачать смотреть
Презентация по Химии "Монооксид углерода: угарный газ" - скачать смотреть  Растворы. Классификация растворов. (Лекция 5)
Растворы. Классификация растворов. (Лекция 5) Ионные равновесия в растворах электролитов
Ионные равновесия в растворах электролитов