Содержание
- 2. Важным видом классификации является классификация по механизму осуществления реакции. Различают простые (одностадийные) и сложные (многостадийные) реакции,
- 3. Для выбора конструкции химического реактора и способов управления проведением процесса существенное значение имеет фазовый состав реакционной
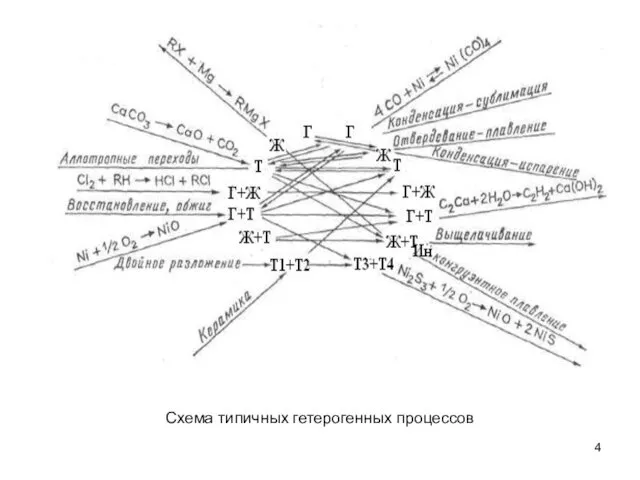
- 4. Схема типичных гетерогенных процессов
- 5. Гетерогенные реакции, несмотря на их многообразие, обладают некоторыми общими фундаментальными закономерностями. Химическое превращение в гетерогенных системах
- 6. Технологические показатели промышленных процессов В качестве таких показателей принято, прежде всего, использовать степень превращения исходного реагента,
- 7. Большинство химических реакций обратимы. Для обратимых реакций при заданных условиях их осуществления предельным является состояние химического
- 8. Величина в уравнении зависит от типа осуществляемой химической реакции: (I) Необратимая химическая реакция Максимально возможное количество
- 9. (III) Параллельные и последовательные реакции Рассмотрим две параллельно протекающие реакции, в которых наряду с целевым продуктом
- 10. Селективность Полная, или интегральная, селективность φ — это отношение количества исходного реагента, расходуемого на целевую реакцию,
- 11. Константа равновесия Известно, что стандартная энергия Гиббса образования вещества связывают с константой равновесия: Для гетерогенные реакций
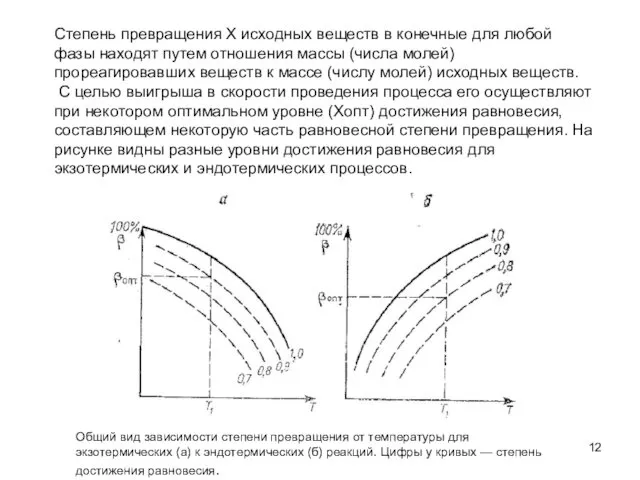
- 12. Степень превращения Х исходных веществ в конечные для любой фазы находят путем отношения массы (числа молей)
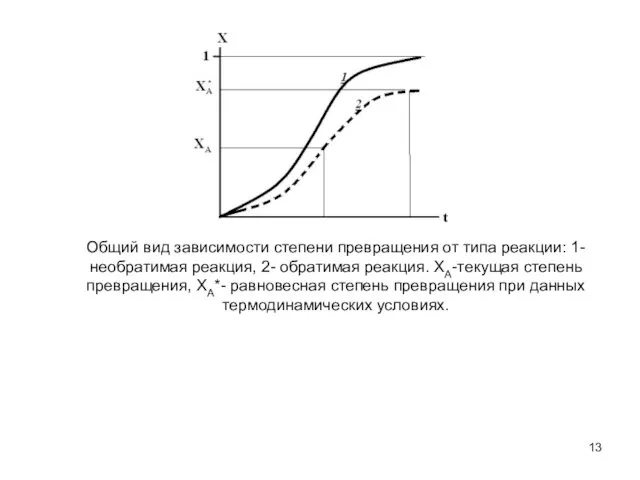
- 13. Общий вид зависимости степени превращения от типа реакции: 1- необратимая реакция, 2- обратимая реакция. ХА-текущая степень
- 14. Константу равновесия химической реакции можно представить через скорости протекания процесса в прямом и обратном направлении. Поскольку
- 15. Лимитирующая стадия гетерогенного процесса Скорость химической реакции r это число актов взаимодействия в единицу времени в
- 16. Скорость химической реакции образования нового продукта С на поверхности контролирует так называемую кинетическую стадию процесса. Если
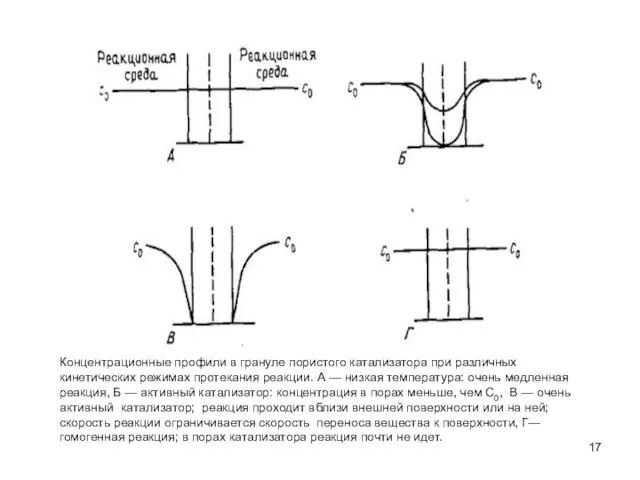
- 17. Концентрационные профили в грануле пористого катализатора при различных кинетических режимах протекания реакции. А — низкая температура:
- 18. Теория активированного (переходного) комплекса (переходного состояния) Скорость простой бимолекулярной газофазной реакции (т. е. реакции, происходящей в
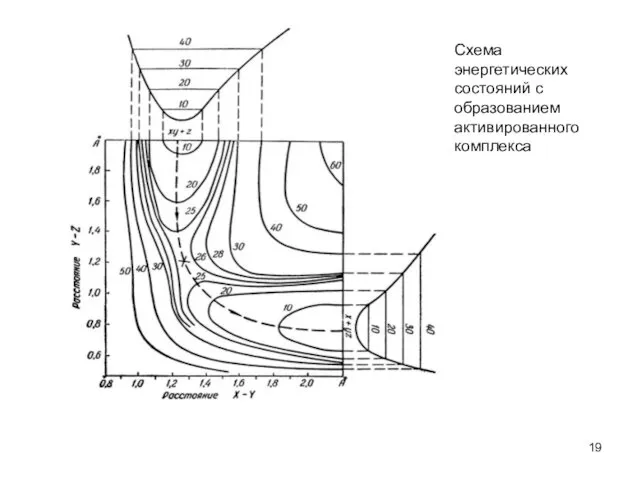
- 19. Схема энергетических состояний с образованием активированного комплекса
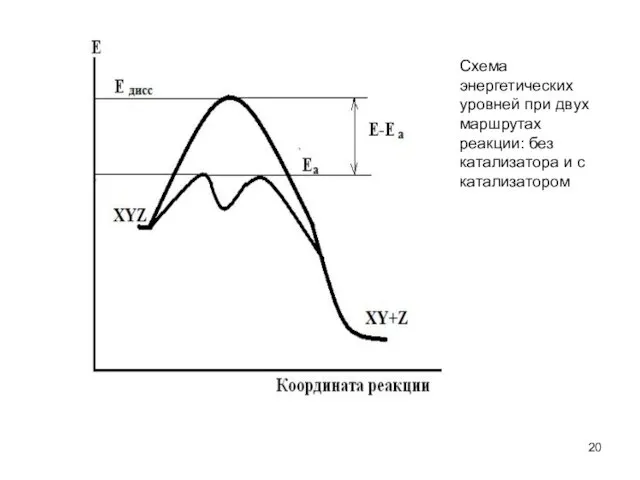
- 20. Схема энергетических уровней при двух маршрутах реакции: без катализатора и с катализатором
- 21. Для скорости гетерогенной каталитической реакции между A и В: Для описания данных по скоростям каталитических реакций
- 22. Внешендиффузионная область протекания гетерогенного процесса Внешнедиффузионной областью называют режим протекания реакции, при котором скорость диффузии исходных
- 23. В гетерогенном химическом процессе исходные вещества и (в общем случае) продукты находятся в разных фазах. По
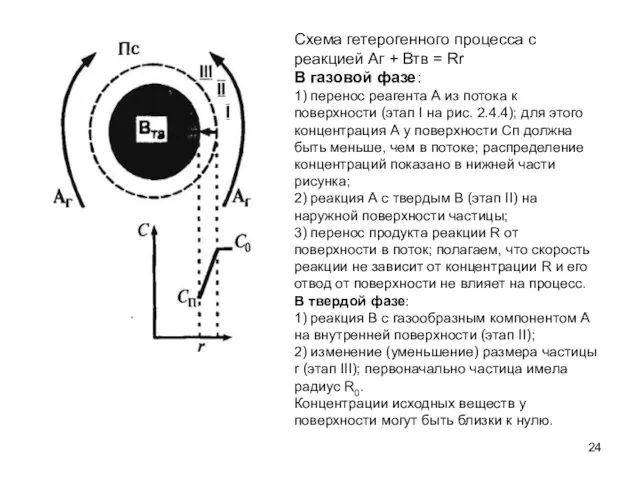
- 24. Схема гетерогенного процесса с реакцией Аг + Втв = Rr В газовой фазе: 1) перенос реагента
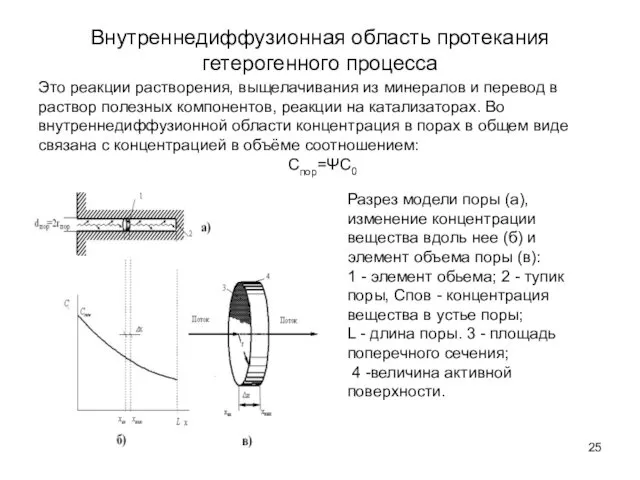
- 25. Внутреннедиффузионная область протекания гетерогенного процесса Это реакции растворения, выщелачивания из минералов и перевод в раствор полезных
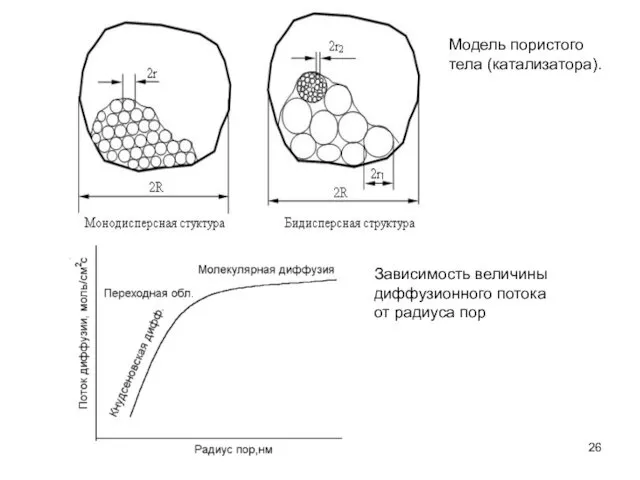
- 26. Модель пористого тела (катализатора). Зависимость величины диффузионного потока от радиуса пор
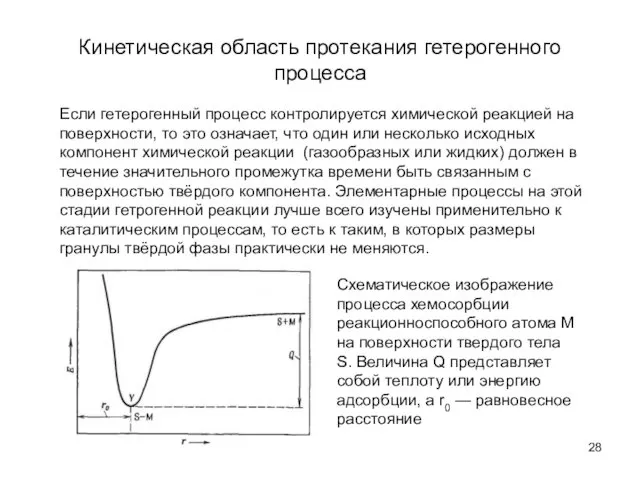
- 28. Кинетическая область протекания гетерогенного процесса Если гетерогенный процесс контролируется химической реакцией на поверхности, то это означает,
- 29. Во многих случаях общая скорость реакции лимитируется не адсорбцией или десорбцией, а скоростью химической реакции: -механизм
- 30. Разложение с адсорбцией продуктов: А→ В + С Предполагается, что: 1) все вещества (А, В и
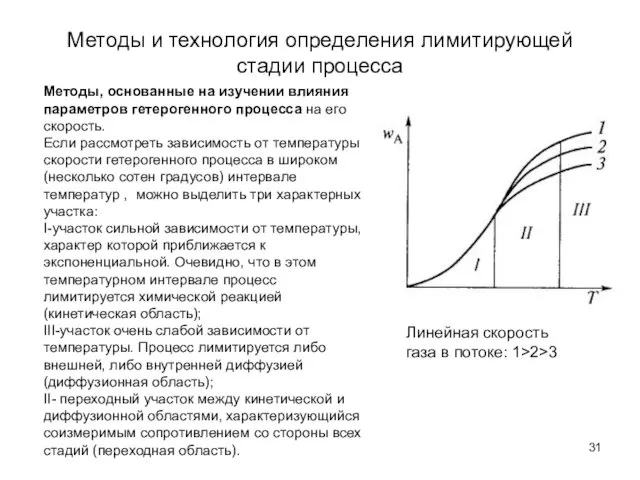
- 31. Методы и технология определения лимитирующей стадии процесса Методы, основанные на изучении влияния параметров гетерогенного процесса на
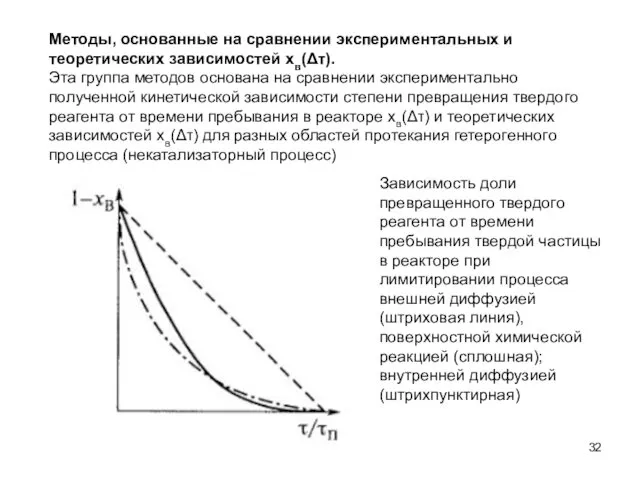
- 32. Методы, основанные на сравнении экспериментальных и теоретических зависимостей хв(Δτ). Эта группа методов основана на сравнении экспериментально
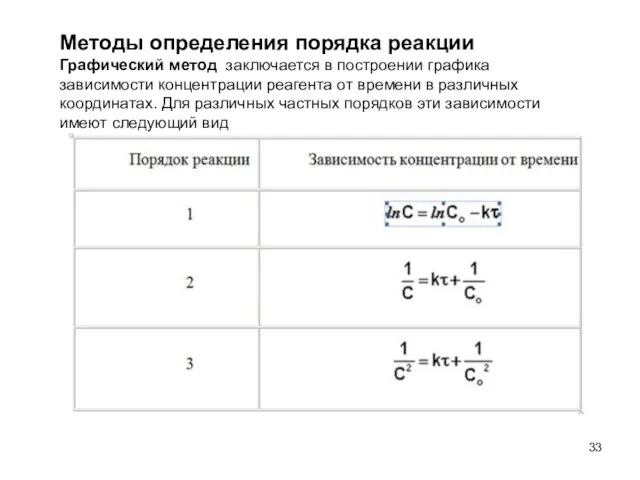
- 33. Методы определения порядка реакции Графический метод заключается в построении графика зависимости концентрации реагента от времени в
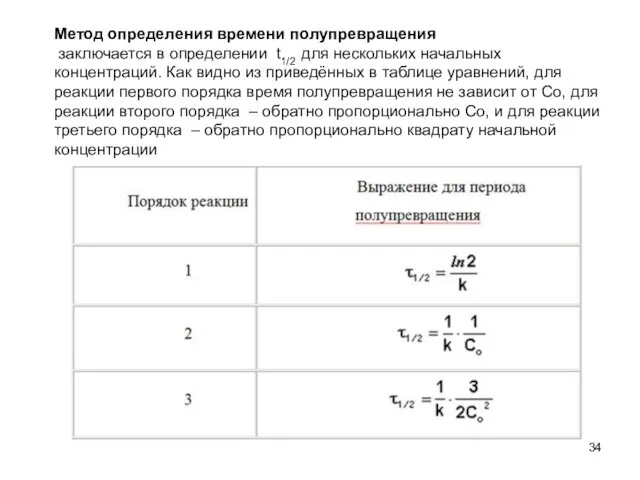
- 34. Метод определения времени полупревращения заключается в определении t1/2 для нескольких начальных концентраций. Как видно из приведённых
- 35. Общие способы увеличения скорости гетерогенного процесса Анализ направлений интенсификации химико-технологических процессов производится при помощи основных формул
- 36. Регулирование температуры процесса как средство повышения движущей силы применяется главным образом в сорбционных и десорбционных процессах.
- 38. Скачать презентацию




















 Современные проблемы химической технологии керамики
Современные проблемы химической технологии керамики Твердое состояние вещества. Плавление
Твердое состояние вещества. Плавление Биологически активные вещества. Витамины. Ферменты. Гормоны
Биологически активные вещества. Витамины. Ферменты. Гормоны Формирование системы знаний о веществе. Лекция 14-15
Формирование системы знаний о веществе. Лекция 14-15 Что изучает химия
Что изучает химия Презентация по Химии "Полезные ископаемые." - скачать смотреть бесплатно_
Презентация по Химии "Полезные ископаемые." - скачать смотреть бесплатно_ Микроорганизмы и важнейшие химические факторы среды обитания
Микроорганизмы и важнейшие химические факторы среды обитания Фосфаттар - минералдар класы - ортофосфорлы қышқыл (Н3РO4) тұздары
Фосфаттар - минералдар класы - ортофосфорлы қышқыл (Н3РO4) тұздары Голубое золото
Голубое золото Валентность химических элементов
Валентность химических элементов Релаксационные свойства полимеров
Релаксационные свойства полимеров Происхождение жизни на Земле
Происхождение жизни на Земле Подготовка учащихся к практическим турам олимпиад по химии
Подготовка учащихся к практическим турам олимпиад по химии Химические свойства солей. Генетическая связь неорганических соединений
Химические свойства солей. Генетическая связь неорганических соединений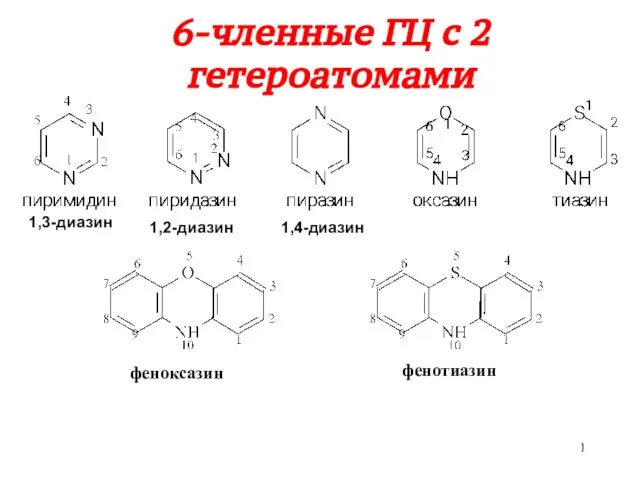 6-членные ГЦ с 2 гетероатомами
6-членные ГЦ с 2 гетероатомами Презентация по Химии "«Белки»" - скачать смотреть
Презентация по Химии "«Белки»" - скачать смотреть  Презентация по Химии "Промышленное получение аминокислот и их применение в медицыне и диетологии" - скачать смотреть бесплат
Презентация по Химии "Промышленное получение аминокислот и их применение в медицыне и диетологии" - скачать смотреть бесплат Урок химии на дне океана. Задача 13
Урок химии на дне океана. Задача 13 Презентация по Химии "Предмет органической химии. Органические вещества" - скачать смотреть
Презентация по Химии "Предмет органической химии. Органические вещества" - скачать смотреть  Углеводороды
Углеводороды Строение атома азота
Строение атома азота Полимеры и их использование
Полимеры и их использование Химическое равновесие. Термодинамика химического равновесия
Химическое равновесие. Термодинамика химического равновесия Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Альдегиды и кетоны
Альдегиды и кетоны Электролиз. Задание № 20
Электролиз. Задание № 20 Радон и его дочерние продукты распада радона
Радон и его дочерние продукты распада радона Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы
Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы