Содержание
- 2. План лекции Общие понятия Свойства разбавленных растворов неэлектролитов Закон Вант-Гоффа для осмотического давления Закон Рауля Закон
- 3. Реальный раствор Идеальный раствор Раствор, в котором нет химического взаимодействия между растворенным веществом и растворителем Не
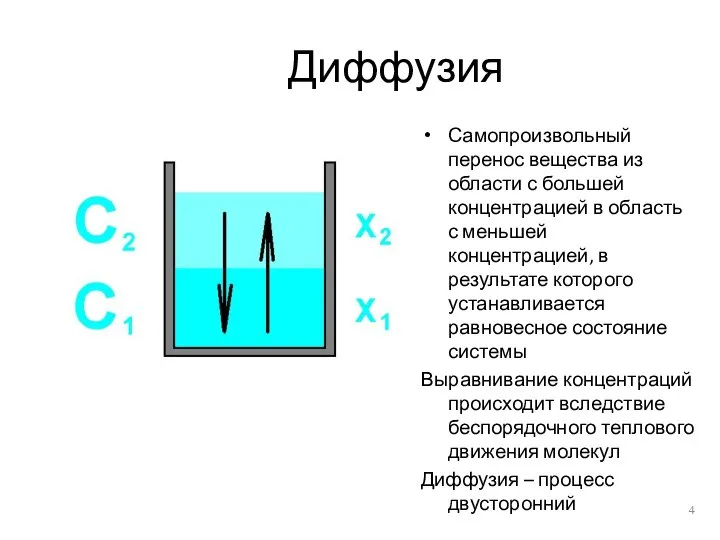
- 4. Диффузия Самопроизвольный перенос вещества из области с большей концентрацией в область с меньшей концентрацией, в результате
- 5. Скорость диффузии Измеряется количеством вещества, перенесенного в единицу времени через единицу площади. Пропорциональна площади переноса и
- 6. Коэффициент диффузии (Д) Определяет собой количество вещества, продиффундировавшего через единицу поверхности за единицу времени при градиенте
- 7. Анализ уравнения Величина диффузии зависит: От площади переноса От градиента концентрации От расстояния диффузии От температуры
- 8. Значение диффузии для биологических процессов Всасывание питательных веществ из просвета кишечника в кровь Поступление питательных веществ
- 9. Диффузия в живых организмах регулируется функциональным состоянием тканей и зависит от их физико-химического строения Диффузия против
- 10. Виды диффузии в организме Диффузия через клеточную мембрану: Пассивная – ей подвергаются низкомолекулярные вещества, растворимые в
- 11. Коллигативные свойства разбавленных растворов неэлектролитов Осмотическое давление Понижение давления насыщенного пара Понижение температуры замерзания Повышение температуры
- 12. Полупроницаемая мембрана Способна пропускать в большей степени молекулы растворителя, чем молекулы растворенного вещества Стенки клеток живых
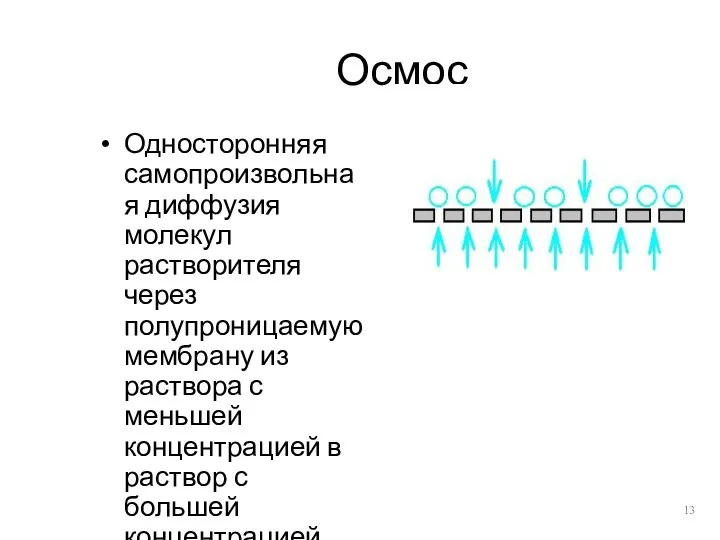
- 13. Осмос Односторонняя самопроизвольная диффузия молекул растворителя через полупроницаемую мембрану из раствора с меньшей концентрацией в раствор
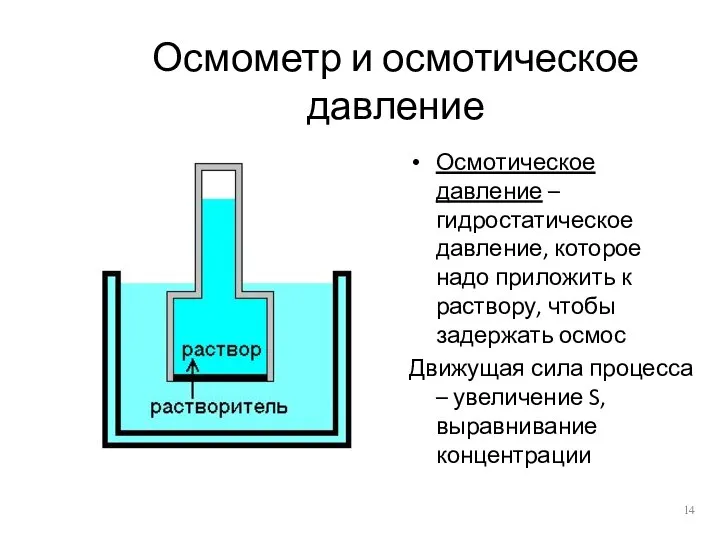
- 14. Осмометр и осмотическое давление Осмотическое давление – гидростатическое давление, которое надо приложить к раствору, чтобы задержать
- 15. Закон Вант-Гоффа для осмотического давления Осмотическое давление разбавленных растворов неэлектролитов равно тому газовому давлению, которое производило
- 16. Осмотическое давление 1 М раствора при 0°С должно быть равно 22,4 атм Величина осмотического давления зависит
- 17. Значение осмоса для биологических систем Тургор – упругое состояние клеток, обусловленное повышенным осмотическим давлением, способствующее сохранению
- 18. Изотонические растворы Растворы, обладающие при одинаковых условиях одинаковым осмотическим давлением Изотоническими по отношению к плазме крови
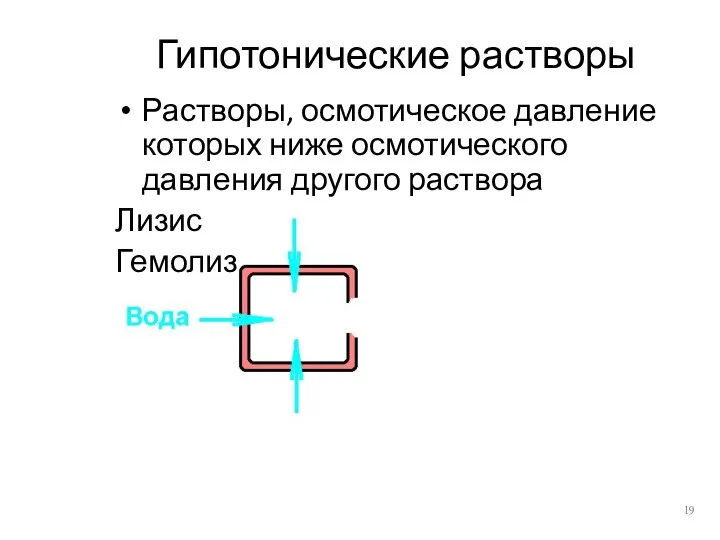
- 19. Гипотонические растворы Растворы, осмотическое давление которых ниже осмотического давления другого раствора Лизис Гемолиз
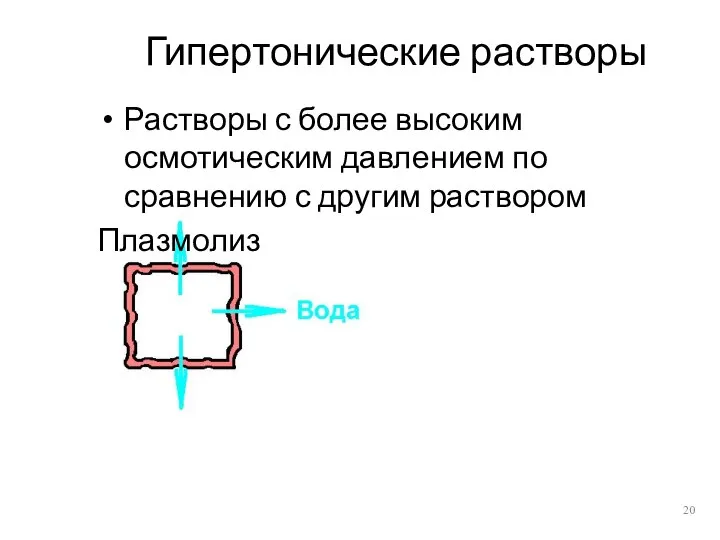
- 20. Гипертонические растворы Растворы с более высоким осмотическим давлением по сравнению с другим раствором Плазмолиз
- 21. Применение гипертонических растворов Наружно: гипертонические повязки (10 – 20% раствор NaCl) Внутривенно: при глаукоме (повышении внутриглазного
- 22. Онкотическое давление крови Белки плазмы крови не проходят через клеточную мембрану, но обладают способностью удерживать определенное
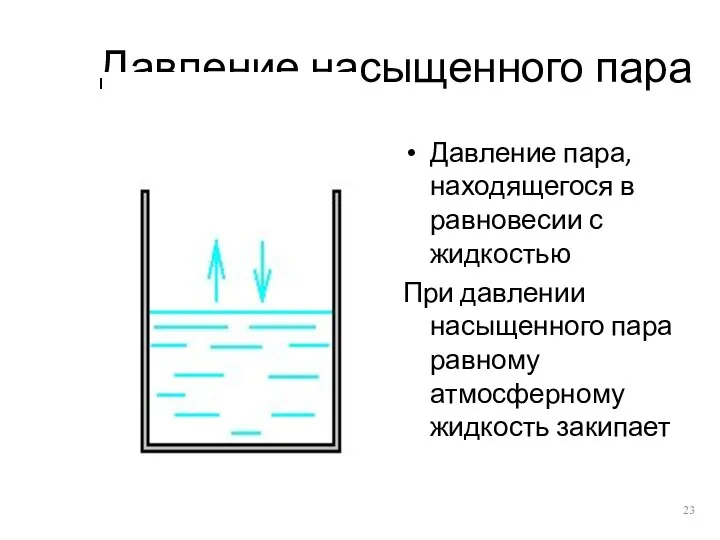
- 23. Давление насыщенного пара Давление пара, находящегося в равновесии с жидкостью При давлении насыщенного пара равному атмосферному
- 24. Давление насыщенного пара над раствором Испарение жидкости Конденсация паров на поверхности Давление насыщенного пара растворителя над
- 25. Закон Рауля Относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного вещества Р0
- 26. ν N = ---------- ν + ν0 ν – число молей растворенного вещества ν0 – число
- 27. Следствия из закона Рауля Растворы кипят при более высокой температуре, чем чистый растворитель Растворы замерзают при
- 28. Замерзание и кипение растворов «Морозы соленого рассолу не могут в лед приводить удобно, как одолевают пресную
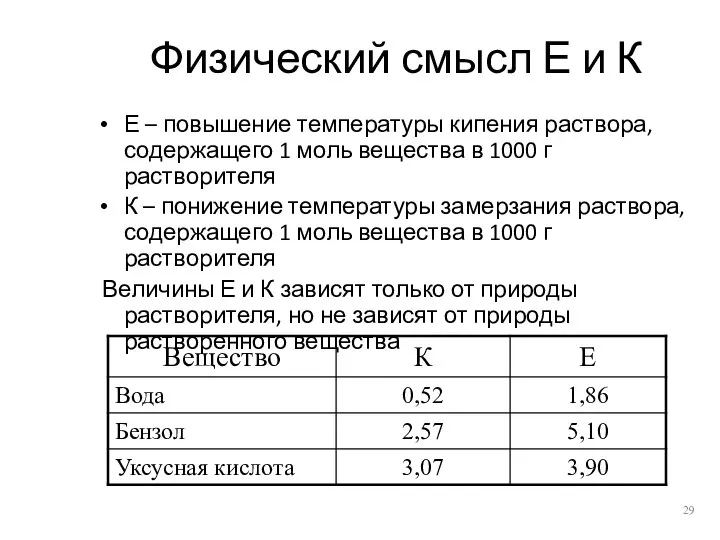
- 29. Физический смысл Е и К Е – повышение температуры кипения раствора, содержащего 1 моль вещества в
- 30. Методы определения молекулярных масс Эбулиометрия – применяют в случае недостаточно растворимых соединений Криометрия – применяют в
- 31. Закон Нернста – Шилова Вещество, способное растворяться в двух несмешивающихся жидкостях, распределяется между ними так, что
- 33. Скачать презентацию























 Химия биогенных элементов. Лекция 14
Химия биогенных элементов. Лекция 14 The Shapes of Molecules
The Shapes of Molecules Презентация по Химии "Химия, нефтехимия. Производство неорганических веществ" - скачать смотреть
Презентация по Химии "Химия, нефтехимия. Производство неорганических веществ" - скачать смотреть  Аминокислоты
Аминокислоты Общие химические свойства металлов
Общие химические свойства металлов Различные виды дисперсных систем. Аэрозоли; эмульсии; коллоидные ПАВ; ВМС
Различные виды дисперсных систем. Аэрозоли; эмульсии; коллоидные ПАВ; ВМС Природный газ
Природный газ Silīcija savienojumi
Silīcija savienojumi Биохимия печени и крови
Биохимия печени и крови Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері
Алкандар. Метан молекуласының құрылысы Метан және оның гомологтарының қасиеттері Вклад М.В. Ломоносова в развитие химии
Вклад М.В. Ломоносова в развитие химии Аттестационная работа. Программа элективного курса по химии экологическая химия
Аттестационная работа. Программа элективного курса по химии экологическая химия Опыты по химии
Опыты по химии Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Вторичный метаболизм и запасные вещества семени растений
Вторичный метаболизм и запасные вещества семени растений Лекарственные растения и сырье, содержащие флавоноиды. (Лекция 12)
Лекарственные растения и сырье, содержащие флавоноиды. (Лекция 12) Особенности КИМ ЕГЭ 2015 года по химии Составитель: Снастина М. Г. Москва 2014 г.
Особенности КИМ ЕГЭ 2015 года по химии Составитель: Снастина М. Г. Москва 2014 г.  Презентація на тему: синтетичні та штучні волокна Виконав учень 11-Б класу Путьо Михайло
Презентація на тему: синтетичні та штучні волокна Виконав учень 11-Б класу Путьо Михайло  Эфиры. Жиры
Эфиры. Жиры Координационные соединения и их применение в медицине, фармакологии
Координационные соединения и их применение в медицине, фармакологии Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10)
Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10) Органические вещества
Органические вещества Инфузионая терапия новорожденных
Инфузионая терапия новорожденных Получение и применение радиоактивных изотопов
Получение и применение радиоактивных изотопов Коррозия
Коррозия Процесс электролиза
Процесс электролиза Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Алкены. Олефины, этиленовые углеводороды. (Лекция 5)
Алкены. Олефины, этиленовые углеводороды. (Лекция 5)