Содержание
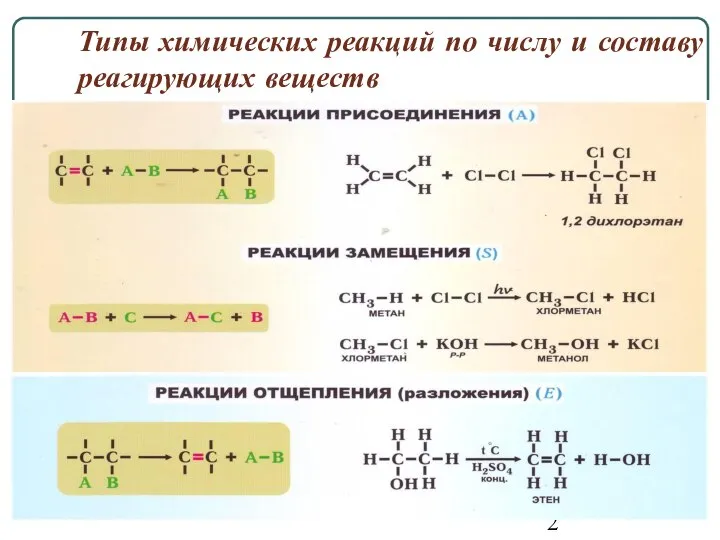
- 2. Типы химических реакций по числу и составу реагирующих веществ
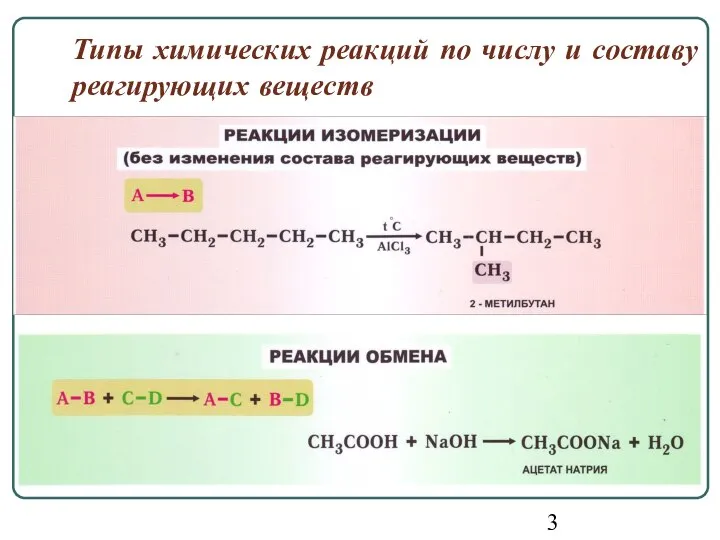
- 3. Типы химических реакций по числу и составу реагирующих веществ
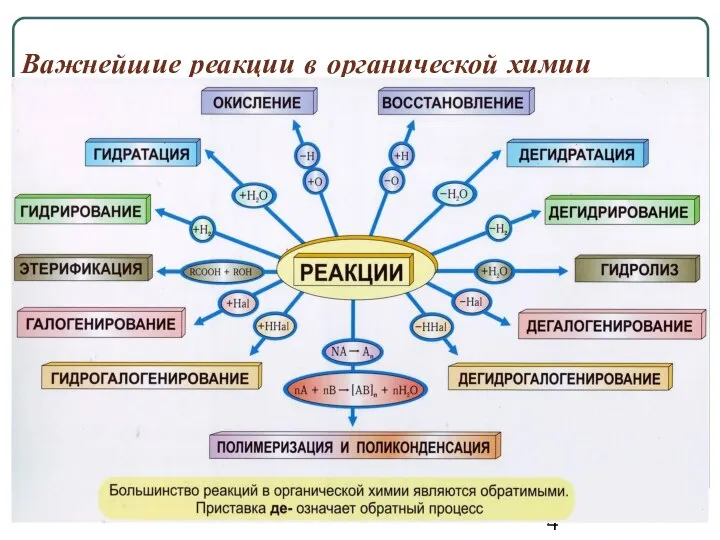
- 4. Важнейшие реакции в органической химии
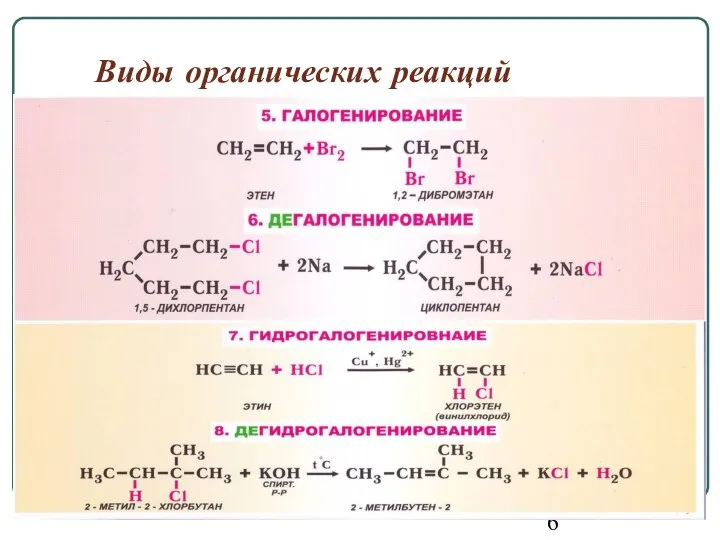
- 5. Виды органических реакций
- 6. Виды органических реакций
- 7. Виды органических реакций
- 8. Виды органических реакций
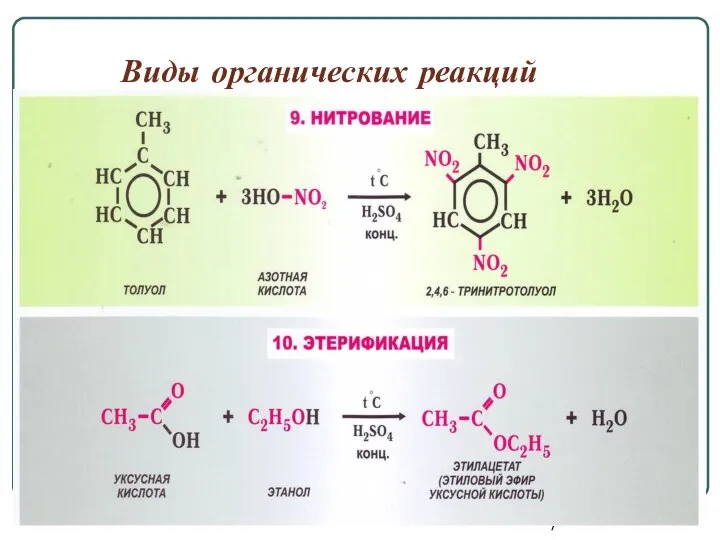
- 9. Виды органических реакций
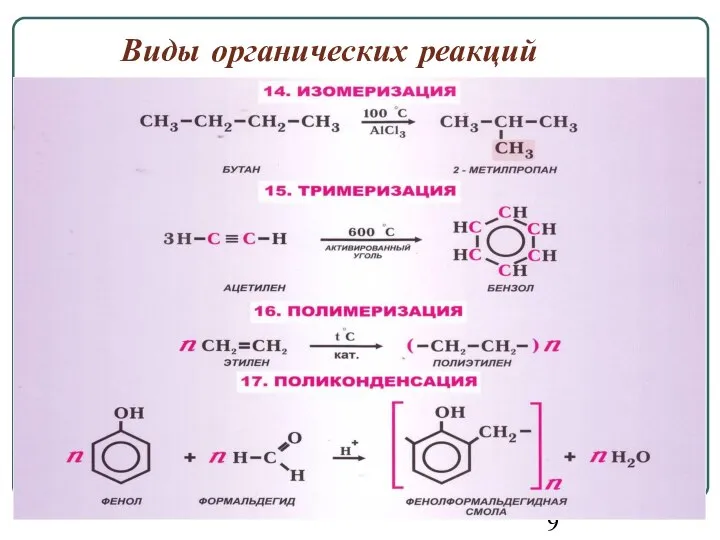
- 10. Виды органических реакций
- 11. 2. Сопряжение В молекулах органических соединений возникают различные электронные эффекты, сопровождающиеся перераспределением электронной плотности ковалентных связей.
- 12. Сопряжёнными называются системы с чередующимися простыми и кратными связями или системы, в которых у атома соседнего
- 13. Различают 2 основных вида сопряжения: π-π - сопряжение и p-π – сопряжение. π-π – сопряженная система
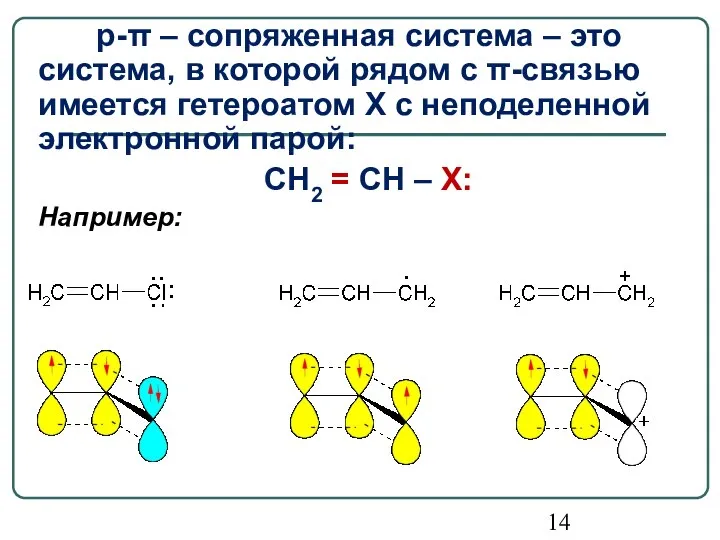
- 14. p-π – сопряженная система – это система, в которой рядом с π-связью имеется гетероатом X с
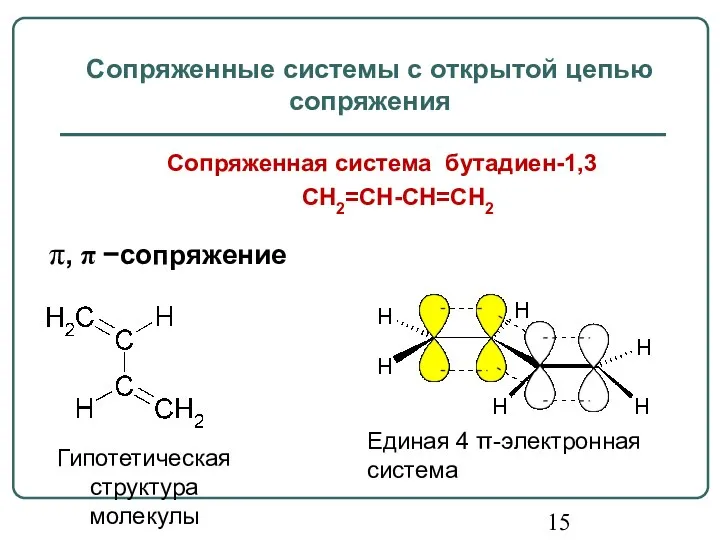
- 15. Сопряженная система бутадиен-1,3 CH2=CH-CH=CH2 Сопряженные системы с открытой цепью сопряжения π, π −сопряжение Гипотетическая структура молекулы
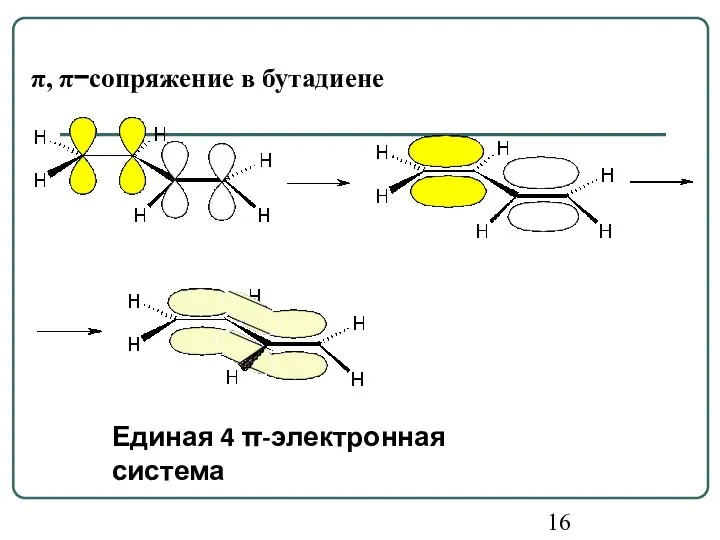
- 16. π, π−сопряжение в бутадиене Единая 4 π-электронная система
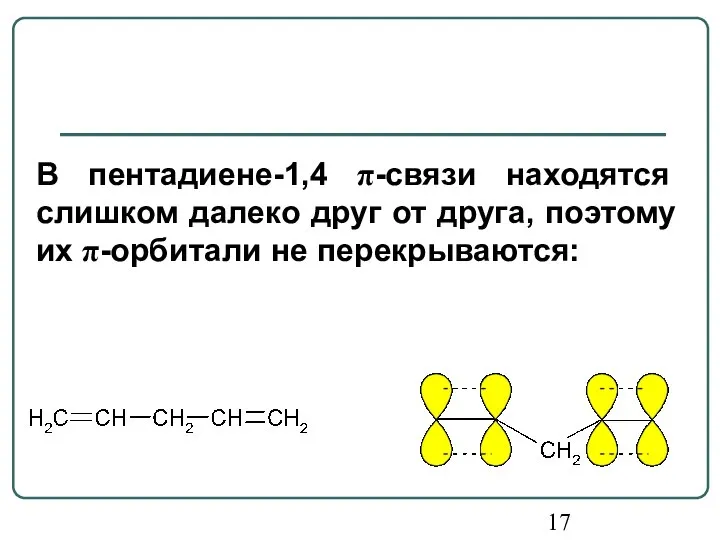
- 17. В пентадиене-1,4 π-связи находятся слишком далеко друг от друга, поэтому их π-орбитали не перекрываются:
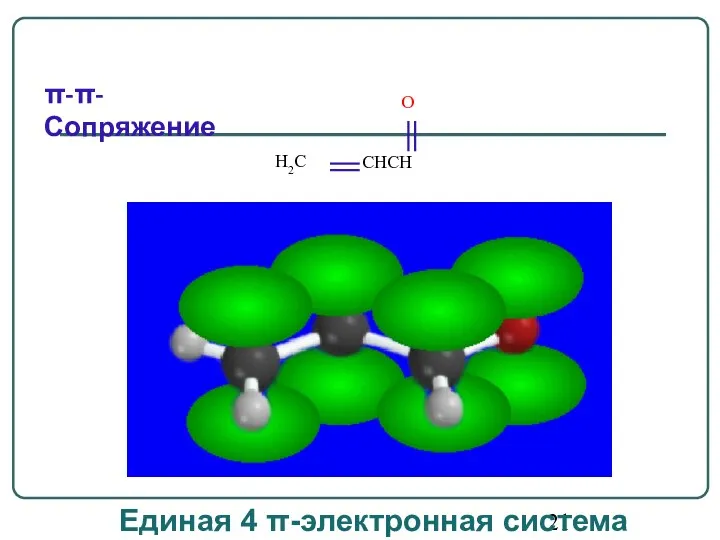
- 18. Система сопряжения может включать и гетероатом (О, N, S). π-π-сопряжение c гетероатомом в цепи осуществляется в
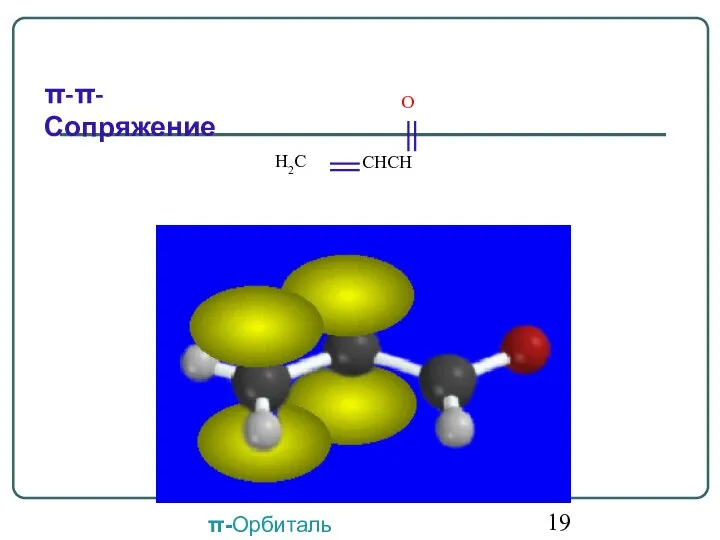
- 19. π-π-Сопряжение π-Орбиталь
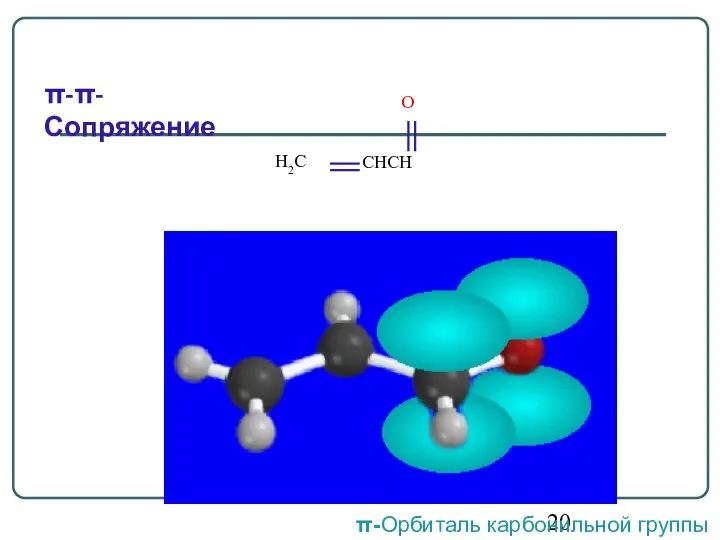
- 20. π-π-Сопряжение π-Орбиталь карбонильной группы
- 21. π-π-Сопряжение Единая 4 π-электронная система
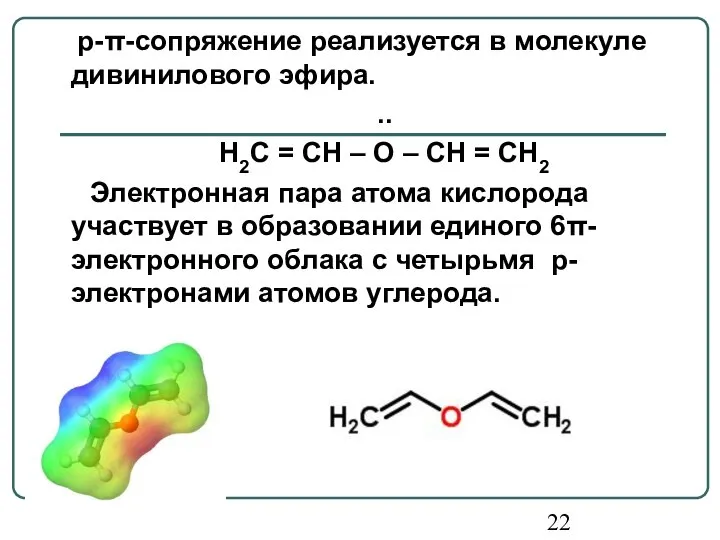
- 22. p-π-сопряжение реализуется в молекуле дивинилового эфира. .. H2C = CH – O – CH = CH2
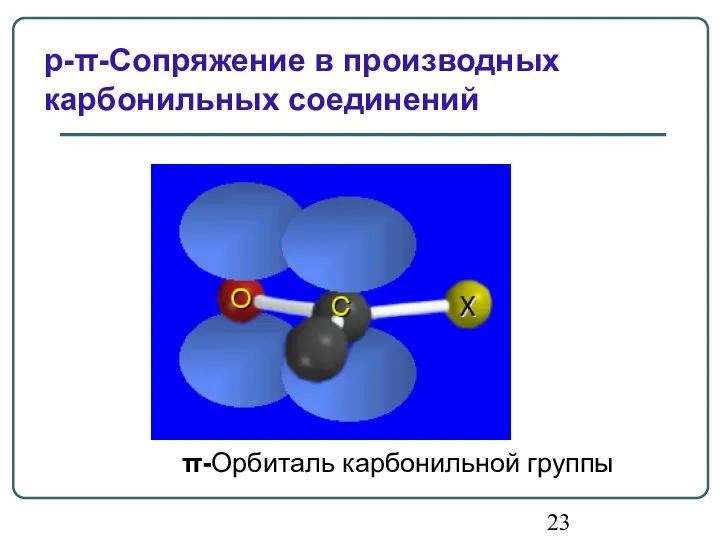
- 23. π-Орбиталь карбонильной группы p-π-Сопряжение в производных карбонильных соединений
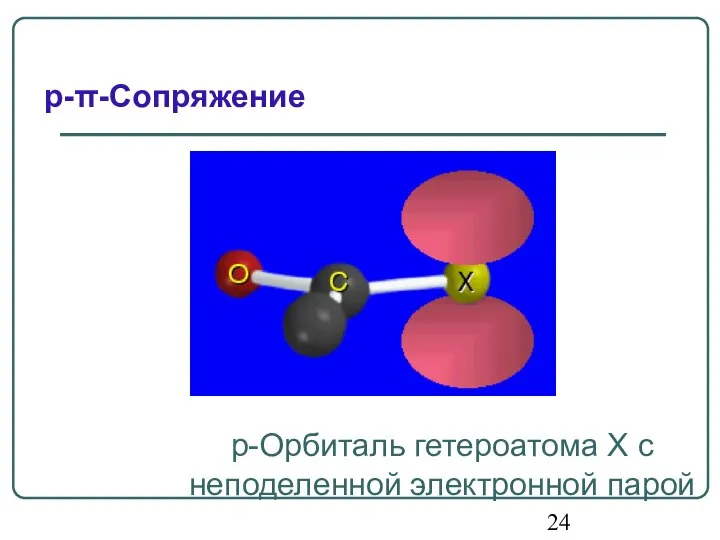
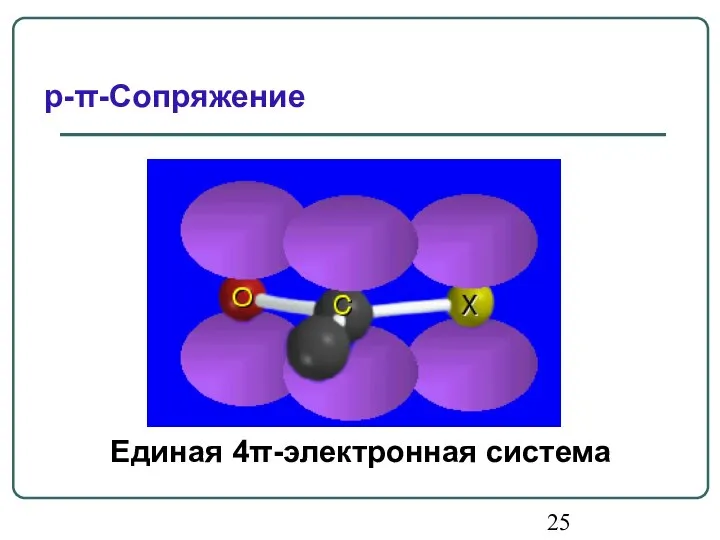
- 24. p-Орбиталь гетероатома X с неподеленной электронной парой p-π-Сопряжение
- 25. Единая 4π-электронная система p-π-Сопряжение
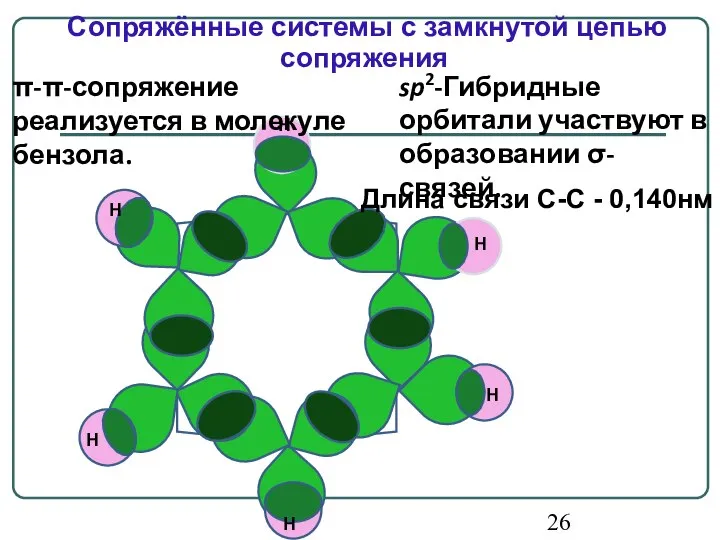
- 26. Длина связи С-С - 0,140нм Н Н Н Н Н Н sp2-Гибридные орбитали участвуют в образовании
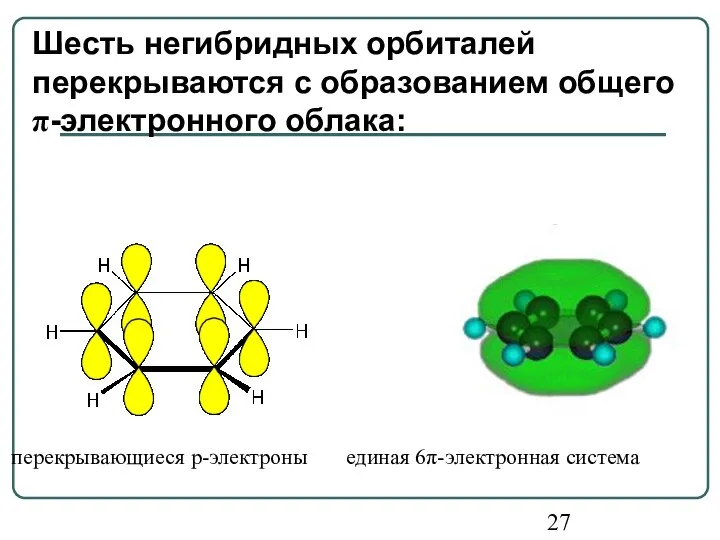
- 27. перекрывающиеся p-электроны единая 6π-электронная система Шесть негибридных орбиталей перекрываются с образованием общего π-электронного облака:
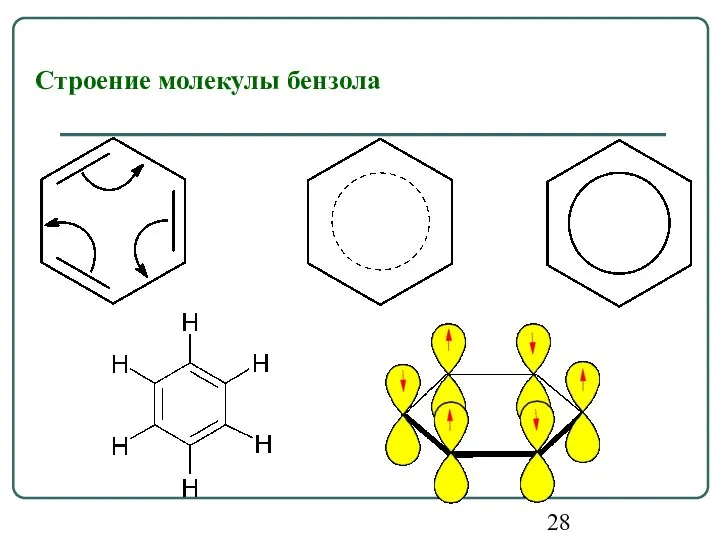
- 28. Строение молекулы бензола
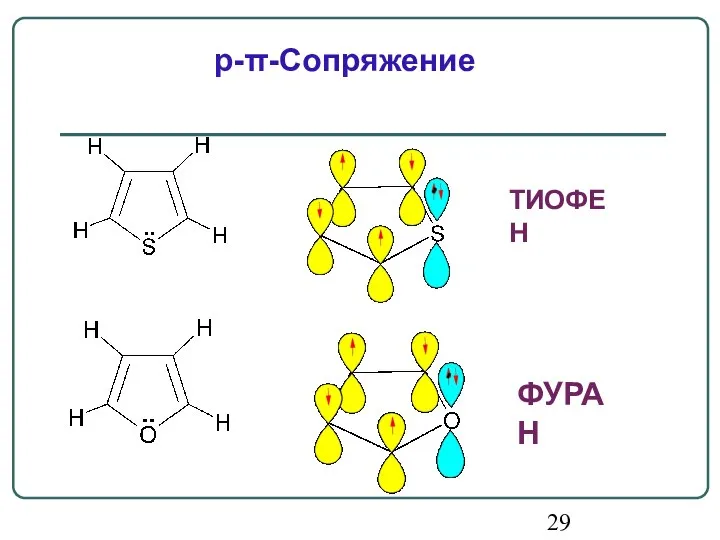
- 29. ФУРАН ТИОФЕН p-π-Сопряжение
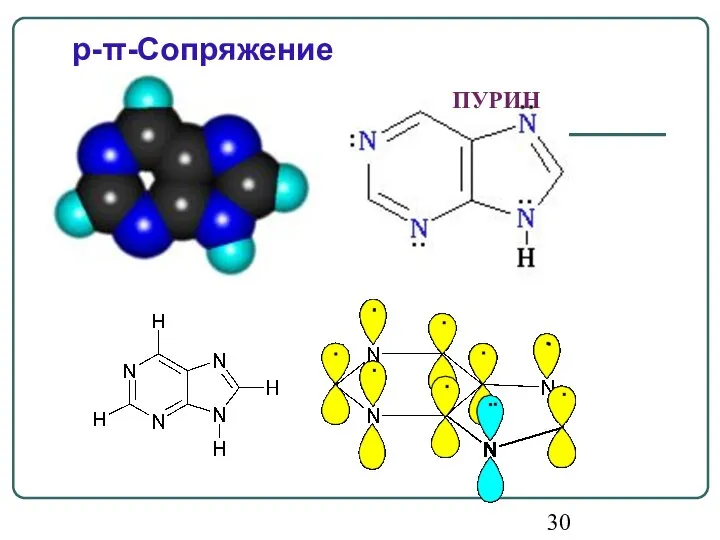
- 30. ПУРИН p-π-Сопряжение
- 31. Ароматическими называют циклические соединения, имеющие замкнутую сопряженную систему, единое π-электронное облако в которых делокализовано на всех
- 32. Эрих Хюккель 1896-1980 Бензол С6Н6 является ароматическим соединением, т.к. отвечает критериям ароматичности . Хюккель Ароматичность
- 33. Критерии ароматичности 1. Молекула имеет циклическое строение. 2. Все атомы цикла находятся в состоянии sp2-гибридизации, образуя
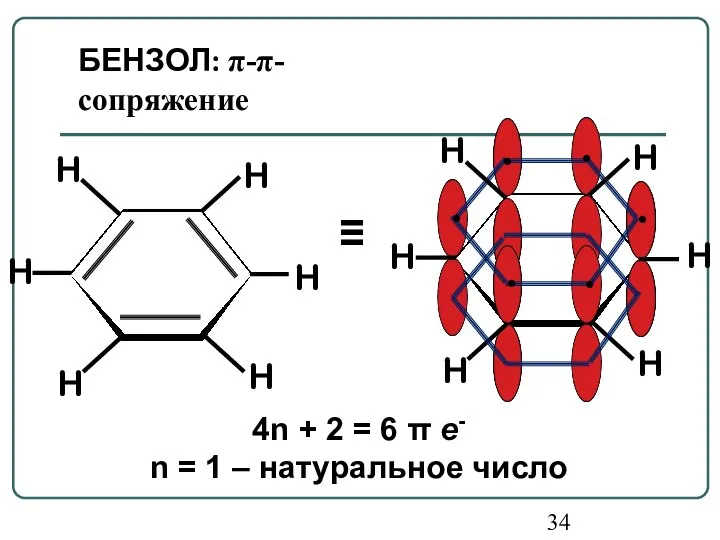
- 34. 4n + 2 = 6 π е- n = 1 – натуральное число БЕНЗОЛ: π-π-сопряжение ≡
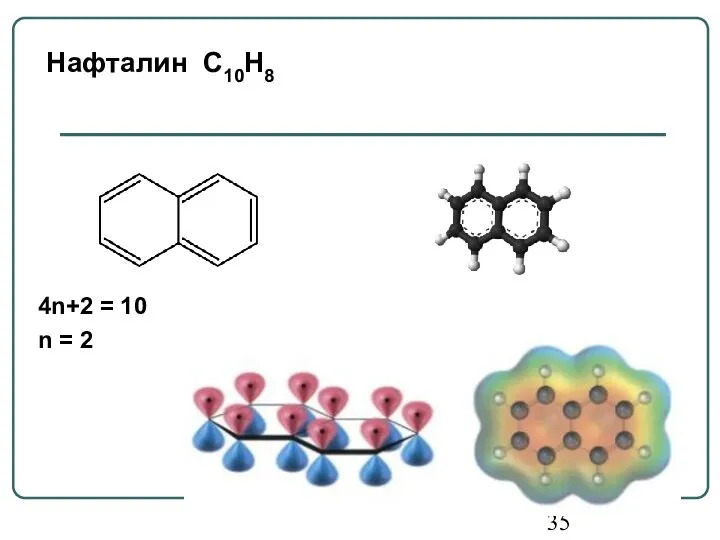
- 35. Нафталин С10Н8 4n+2 = 10 n = 2
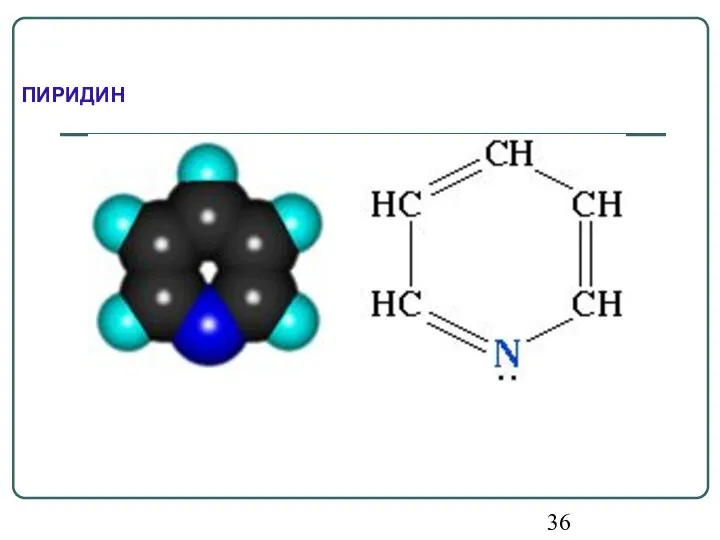
- 36. ПИРИДИН
- 37. Пиридин отвечает критериям ароматичности: 1. Молекула имеет циклическое строение. 2. Все атомы цикла находятся в состоянии
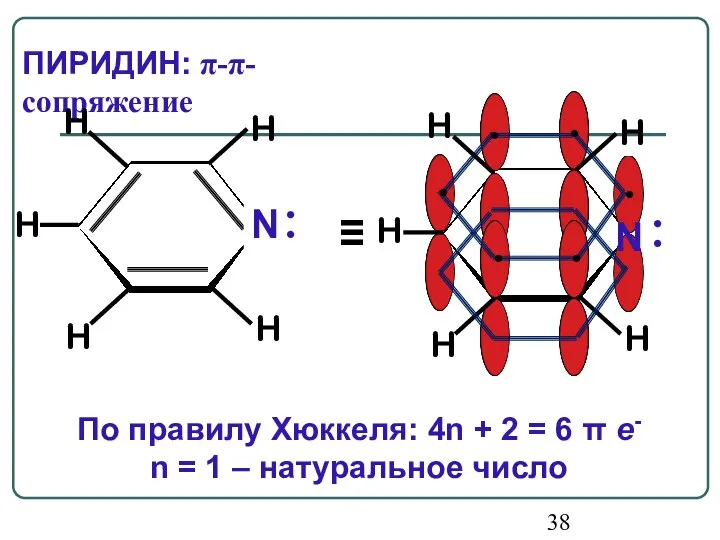
- 38. По правилу Хюккеля: 4n + 2 = 6 π е- n = 1 – натуральное число
- 39. Атом азота поставляет в сопряженную цепь один электрон и сохраняет пару электронов вне сопряженной цепи. За
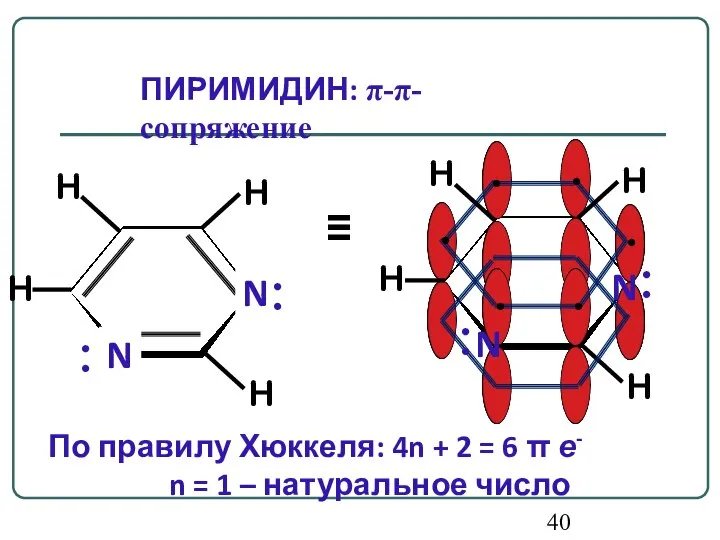
- 40. По правилу Хюккеля: 4n + 2 = 6 π е- n = 1 – натуральное число
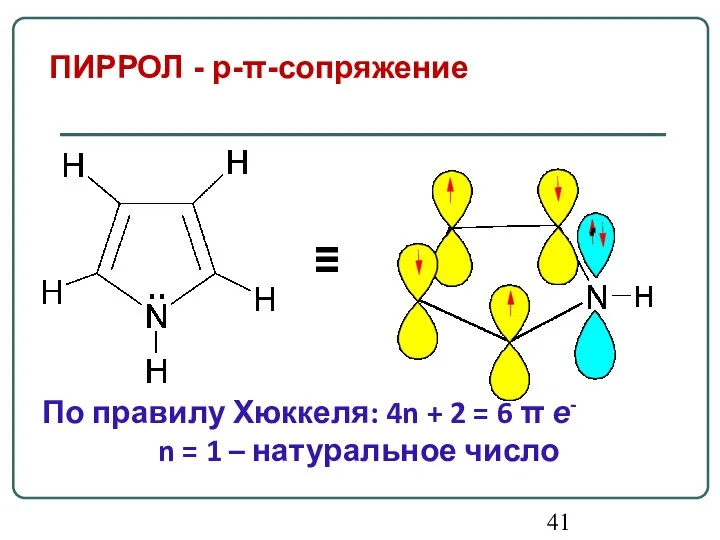
- 41. ПИРРОЛ - p-π-сопряжение ≡ По правилу Хюккеля: 4n + 2 = 6 π е- n =
- 42. Взаимное влияние атомов в молекуле может осуществляться по системе δ-связей (индуктивный эффект), по системе π-связей (мезомерный
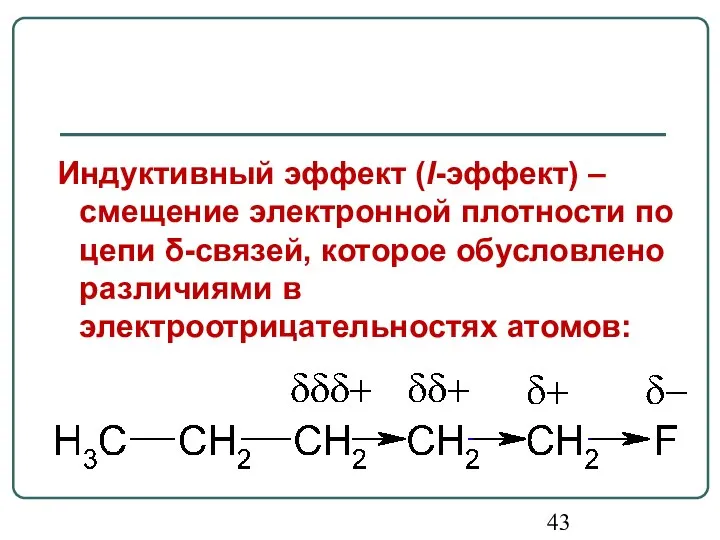
- 43. Индуктивный эффект (I-эффект) – смещение электронной плотности по цепи δ-связей, которое обусловлено различиями в электроотрицательностях атомов:
- 44. Индуктивный эффект обозначают буквой I и графически изображают стрелкой, остриё которой направлено в сторону более ЭО
- 45. –I эффект проявляют заместители, которые содержат атомы с большей ЭО, чем у углерода: -F, -Cl, -Br,
- 46. +I эффект проявляют заместители, содержащие атомы с низкой электроотрицательностью: металлы (-Mg, -Li); насыщенные углеводородные радикалы (-CH3,
- 47. Мезомерный эффект – смещение электронной плотности по цепи сопряженных π-связей. Возникает только при наличии сопряжения связей.
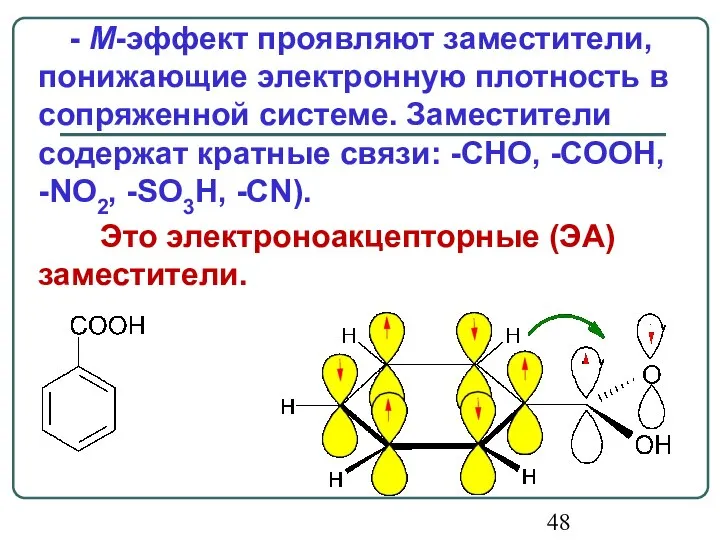
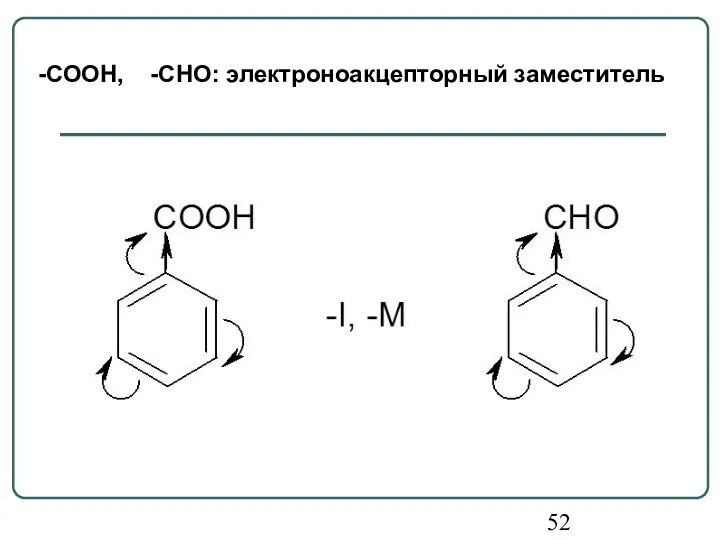
- 48. - М-эффект проявляют заместители, понижающие электронную плотность в сопряженной системе. Заместители содержат кратные связи: -CHO, -COOH,
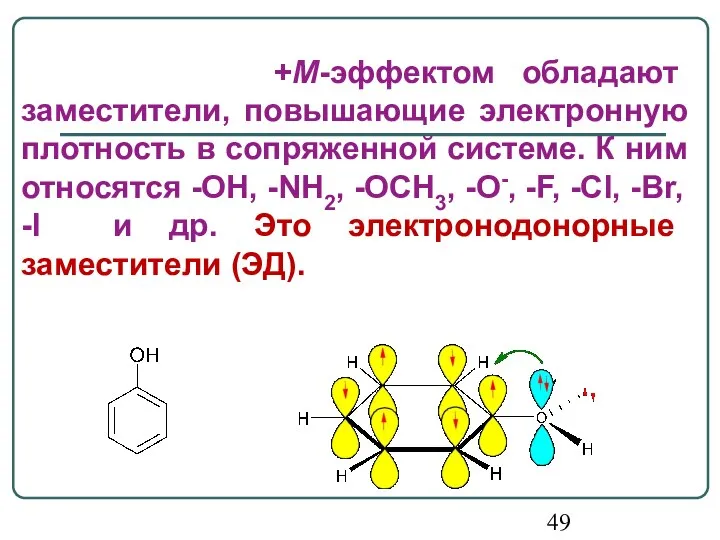
- 49. +М-эффектом обладают заместители, повышающие электронную плотность в сопряженной системе. К ним относятся -OH, -NH2, -OCH3, -O-,
- 50. В молекулах органических соединений индуктивный и мезомерный эффекты заместителей, действуют одновременно.
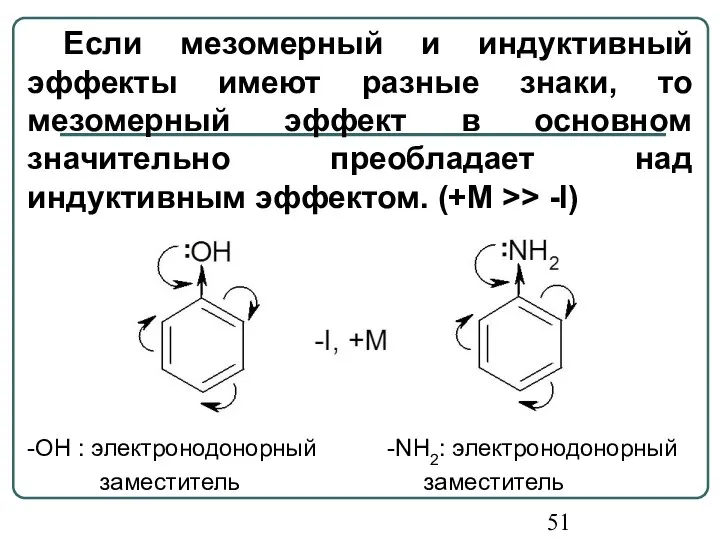
- 51. Если мезомерный и индуктивный эффекты имеют разные знаки, то мезомерный эффект в основном значительно преобладает над
- 52. -СООН, -СНО: электроноакцепторный заместитель
- 53. Таким образом, учитывая перераспределение электронной плотности в молекулах органических соединений, в том числе биологически активных веществ,
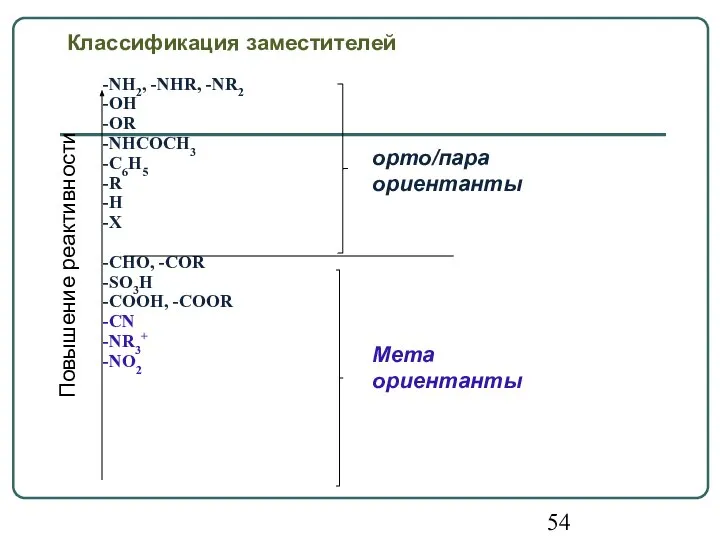
- 54. Классификация заместителей -NH2, -NHR, -NR2 -OH -OR -NHCOCH3 -C6H5 -R -H -X -CHO, -COR -SO3H -COOH,
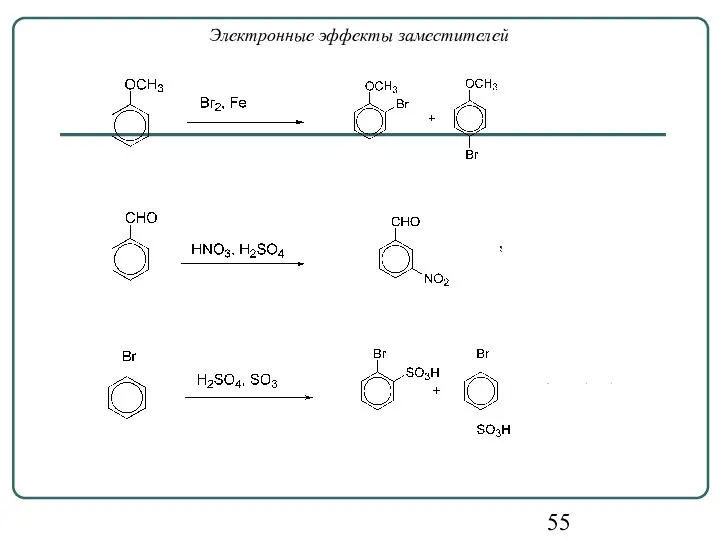
- 55. Электронные эффекты заместителей
- 56. Спасибо за внимание!
- 57. 3. Кислотность органических соединений Кислотно-основные свойства органических веществ рассматривают, основываясь на положениях протонной теории кислот и
- 58. Основные положения теории: Кислота – частица (молекула или ион), отдающая протон в данной реакции, т.е. донор
- 59. 2. Основание – частица (молекула или ион), присоединяющая протон в данной реакии, т.е. акцептор H+.
- 60. Протолитическая теория кислот и оснований Основание – частица (молекула или ион), присоединяющая протон в данной реакии,
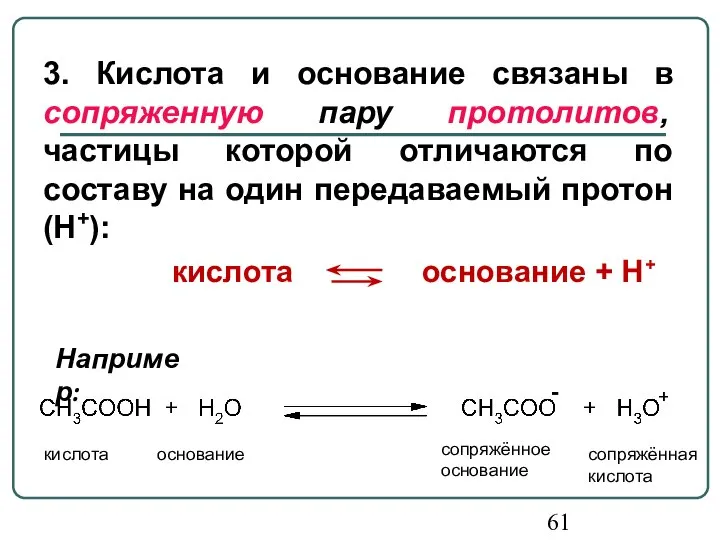
- 61. 3. Кислота и основание связаны в сопряженную пару протолитов, частицы которой отличаются по составу на один
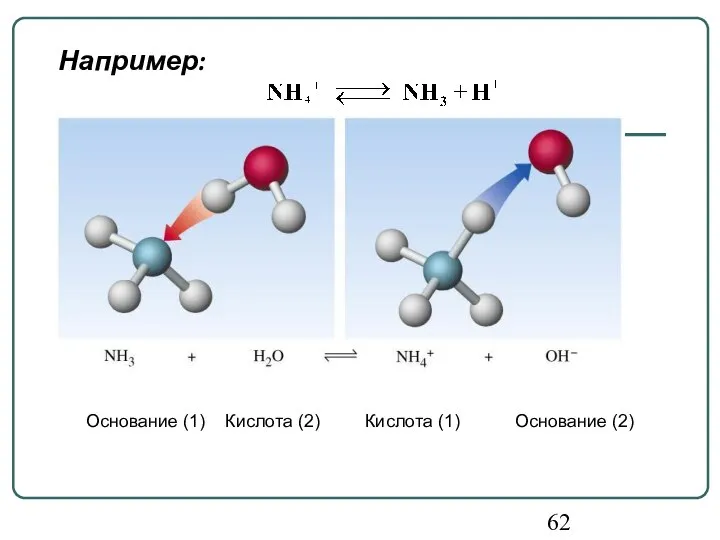
- 62. Основание (1) Кислота (2) Кислота (1) Основание (2) Например:
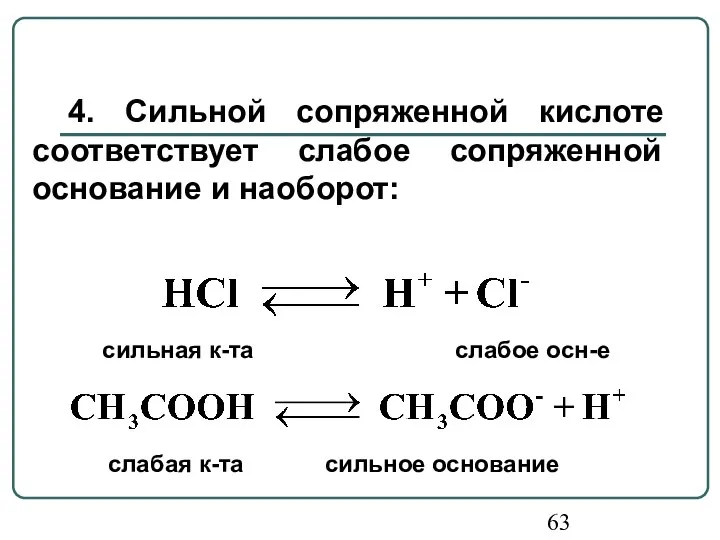
- 63. 4. Сильной сопряженной кислоте соответствует слабое сопряженной основание и наоборот: сильная к-та слабое осн-е слабая к-та
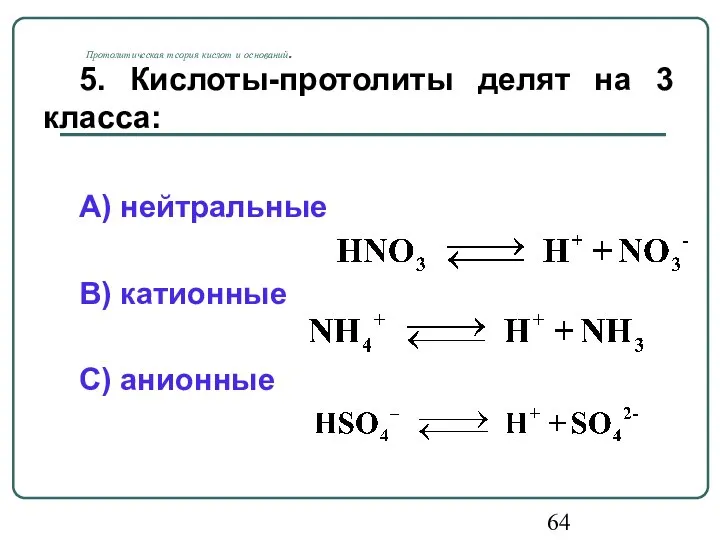
- 64. Протолитическая теория кислот и оснований. 5. Кислоты-протолиты делят на 3 класса: А) нейтральные В) катионные С)
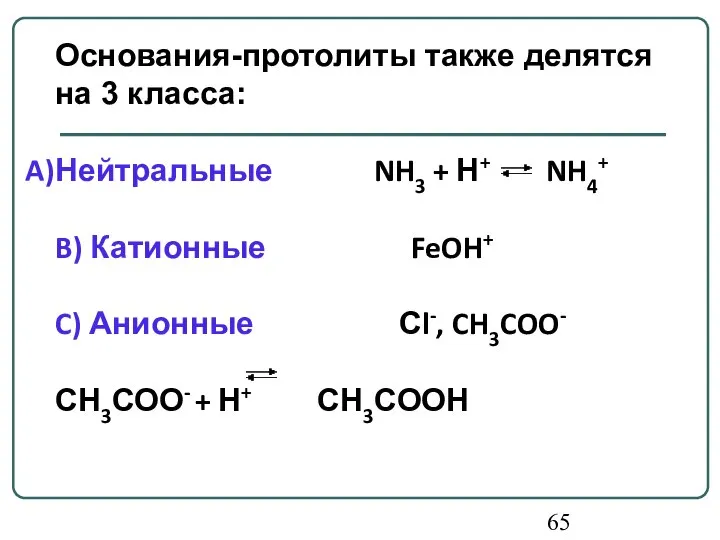
- 65. Основания-протолиты также делятся на 3 класса: Нейтральные NH3 + Н+ NH4+ B) Катионные FeOH+ C) Анионные
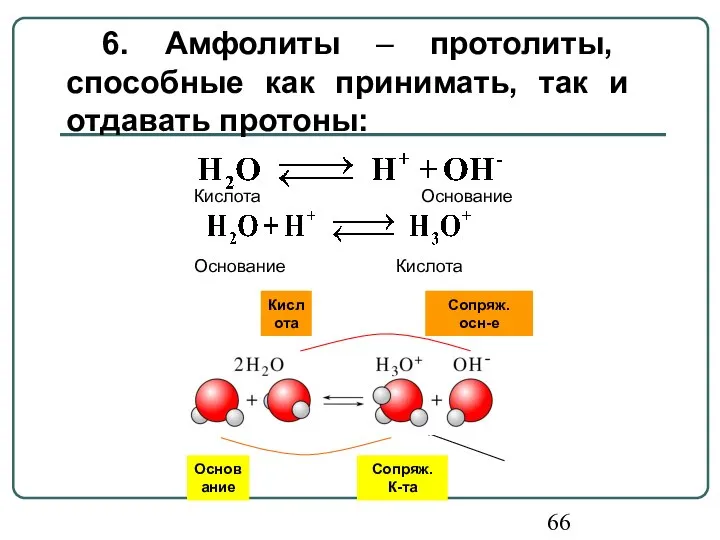
- 66. Кислота Сопряж. осн-е Основание Сопряж. К-та 6. Амфолиты – протолиты, способные как принимать, так и отдавать
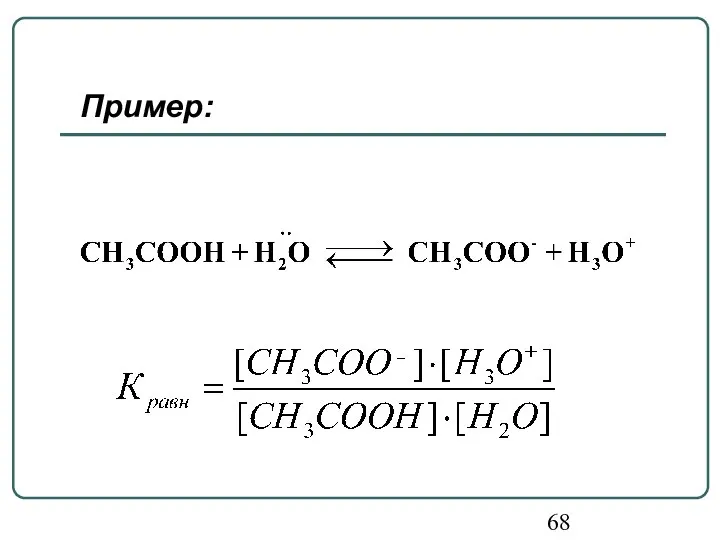
- 67. 7. Количественно сила кислот-протолитов оценивается величиной константы кислотности (Ка). Ка характеризует момент химического равновесия в процессе
- 68. Пример:
- 69. Таким образом, чем выше концентрация сопряженных частиц продуктов протонного переноса, тем больше значение Ка, а значит
- 70. На практике используют показатель константы кислотности (pKa): Чем меньше значение pKa, тем сильнее кислота.
- 71. Кислотным центром называется элемент (С, S, O, N) и связанный с ним атом водорода. Органические кислоты
- 72. Формулы и названия веществ рКа 18 С2Н5ОН этанол 10,5 С2Н5SH этантиол 30 С2Н5NH2 этанамин 9,9 С6Н5ОН
- 73. На стабильность аниона оказывают влияние следующие факторы: 1. Природа элемента в кислотном центре. а) электроотрицательность элемента
- 74. кислород более электроотрицательный элемент связь О-Н более полярна, чем N-H, что способствует более легкой отщепляемости в
- 75. б) поляризуемость элемента в кислотном центре. Сравним кислотные свойства веществ с одинаковыми радикалами: СН3–СН2 –ОН (рКа=18)
- 76. Благодаря большему радиусу и более высокой поляризуемости атома серы, отрицательный заряд в анионе СН3–СН2–S- (меркаптид-ион) делокализован
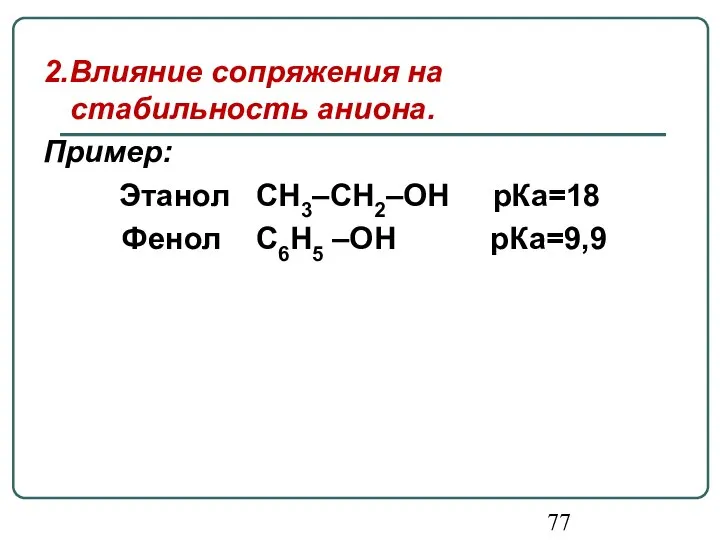
- 77. 2.Влияние сопряжения на стабильность аниона. Пример: Этанол СН3–СН2–ОН рКа=18 Фенол С6Н5 –ОН рКа=9,9
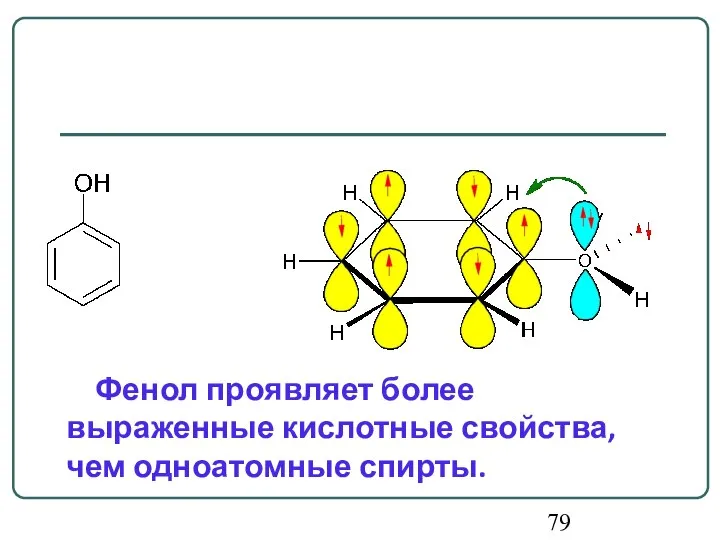
- 78. В молекуле фенола под влиянием ЭД-заместителя электронная плотность смещена от заместителя и делокализована по ароматическому кольцу.
- 79. Фенол проявляет более выраженные кислотные свойства, чем одноатомные спирты.
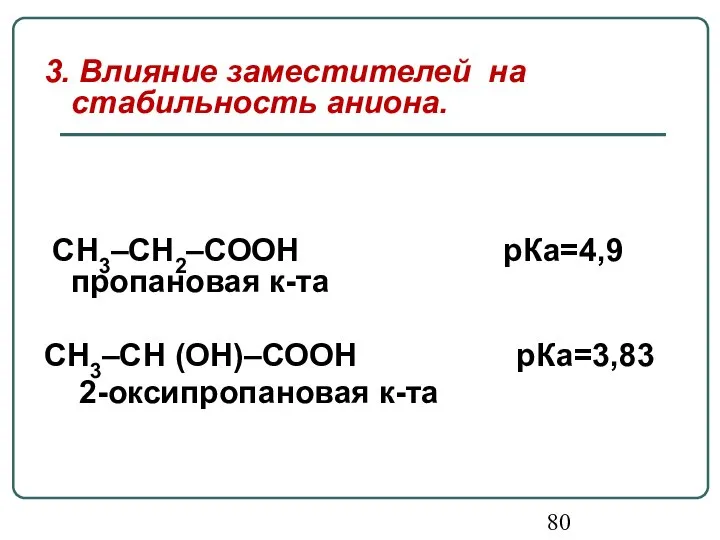
- 80. 3. Влияние заместителей на стабильность аниона. СН3–СН2–СООН рКа=4,9 пропановая к-та СН3–СН (ОН)–СООН рКа=3,83 2-оксипропановая к-та
- 81. Наличие в радикале кислоты ЭА заместителя –ОН-группы способствует делокализации отрицательного заряда в лактат-анионе, что повышает его
- 82. 4. Влияние растворителя на стабильность аниона. Чем меньше радикал аниона, тем он более гидратирован и стабилен.
- 84. Скачать презентацию

































 Установка изомеризации пентан гексановой фракции
Установка изомеризации пентан гексановой фракции Структура белка
Структура белка Предельные углеводороды
Предельные углеводороды Биологическая роль макро и микроэлементов. (Лекция 17)
Биологическая роль макро и микроэлементов. (Лекция 17) pH жидкостей, необходимых для человека Выполнили: Учащиеся 11 класса МОУ «СОШ №16» Самоделкин Василий Шадрин Константин
pH жидкостей, необходимых для человека Выполнили: Учащиеся 11 класса МОУ «СОШ №16» Самоделкин Василий Шадрин Константин  Мило та його склад
Мило та його склад  Растворение. Растворимость веществ.
Растворение. Растворимость веществ. Химия морской воды
Химия морской воды Теория диаграмм состояния
Теория диаграмм состояния Углеводы. Структура
Углеводы. Структура Биогеохимические эндемии и их профилактика
Биогеохимические эндемии и их профилактика Органикалық қосылыстар
Органикалық қосылыстар Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания
Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания Закономерности химических реакций
Закономерности химических реакций Азотная кислота
Азотная кислота Гидролиз солей
Гидролиз солей Химические свойства кислот.
Химические свойства кислот. Презентация по Химии "Спирты" - скачать смотреть _
Презентация по Химии "Спирты" - скачать смотреть _ Основные типы химических реакций
Основные типы химических реакций Презентация по химии Применение электролиза
Презентация по химии Применение электролиза  Классификация и ассортимент клея
Классификация и ассортимент клея Фосфор, фосфор оксидтері
Фосфор, фосфор оксидтері Выполнил учениц__ 9 «___» класса __________________
Выполнил учениц__ 9 «___» класса __________________  Химические свойства алкинов
Химические свойства алкинов Воздух. Состав воздуха. Реакция горения
Воздух. Состав воздуха. Реакция горения Химический элемент сера
Химический элемент сера Ionic polymerization
Ionic polymerization Неорганическая химия
Неорганическая химия