Содержание
- 2. Растворы играют важную роль в природе, науке и технике. Особую роль на нашей планете играет вода.
- 3. Изучение свойств растворов занимает важное место в современной науке. В химии процессы растворения рассматриваются с позиций
- 4. Физическая теория Якоб Хендрик Вант-Гофф Сванте Август Аррениус Вильгельм Фридрих Оствальд Процесс растворения является процессом диффузии,
- 5. Химическая теория Дмитрий Иванович Менделеев Иван Алексеевич Каблуков Процесс растворения – это результат взаимодействия вещества с
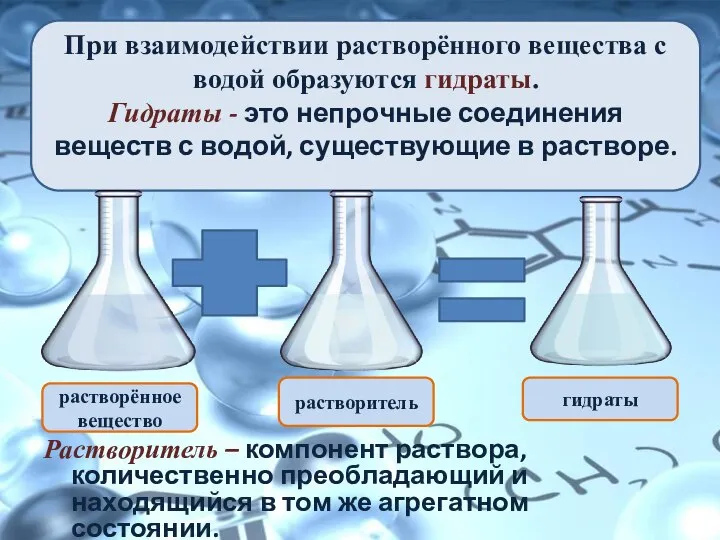
- 6. При взаимодействии растворённого вещества с водой образуются гидраты. Гидраты - это непрочные соединения веществ с водой,
- 7. Косвенным доказательством гидратации является существование твердых кристаллогидратов Кристаллогидраты – соли и другие твердые вещества, в состав
- 8. Физико-химическая теория В настоящее время принята теория, которая объединяет обе точки зрения,- физико-химическая теория растворов. Её
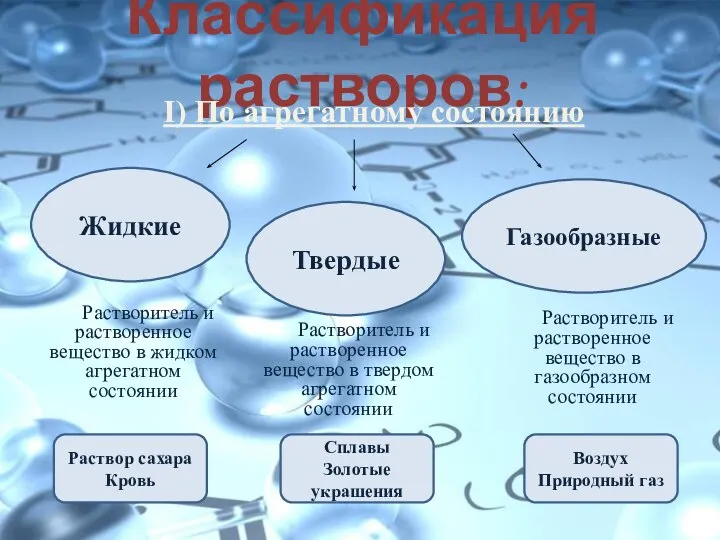
- 9. Классификация растворов: I) По агрегатному состоянию Жидкие Газообразные Твердые Растворитель и растворенное вещество в газообразном состоянии
- 10. 2. От природы растворителя От чего зависит растворимость веществ? От температуры 3. От природы вещества
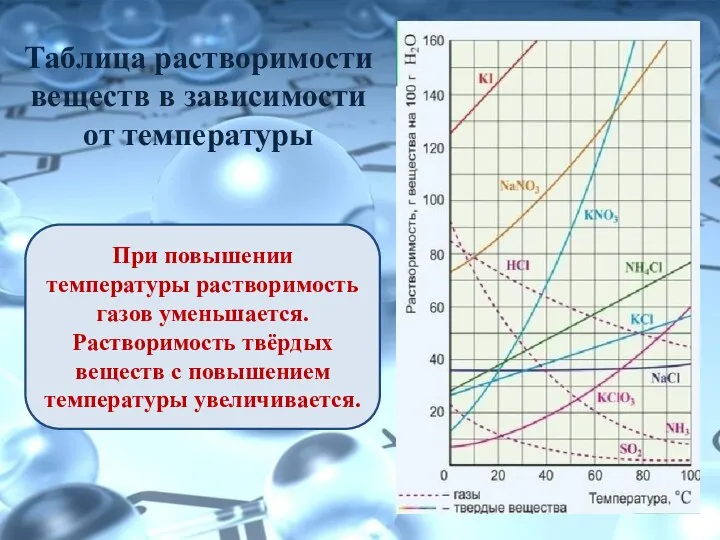
- 11. Таблица растворимости веществ в зависимости от температуры При повышении температуры растворимость газов уменьшается. Растворимость твёрдых веществ
- 12. II) В зависимости от количества растворённого в растворителе вещества Классификация растворов: Насыщенные Ненасыщенные Перенасыщенные Ненасыщенным называют
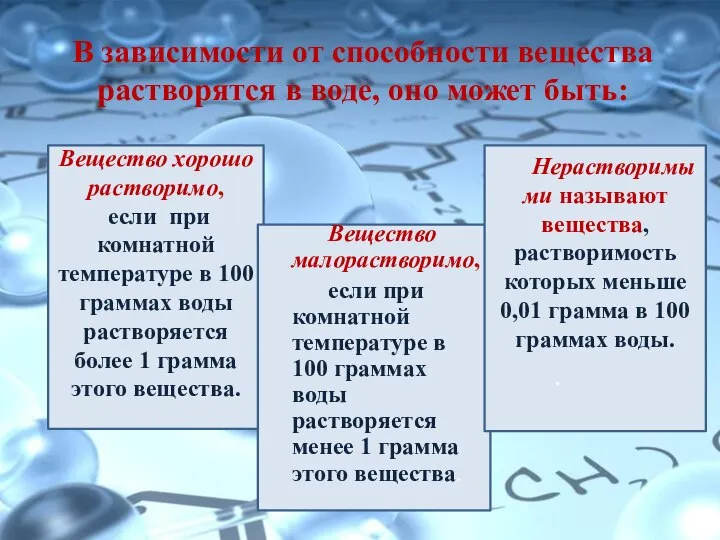
- 13. В зависимости от способности вещества растворятся в воде, оно может быть: Вещество хорошо растворимо, если при
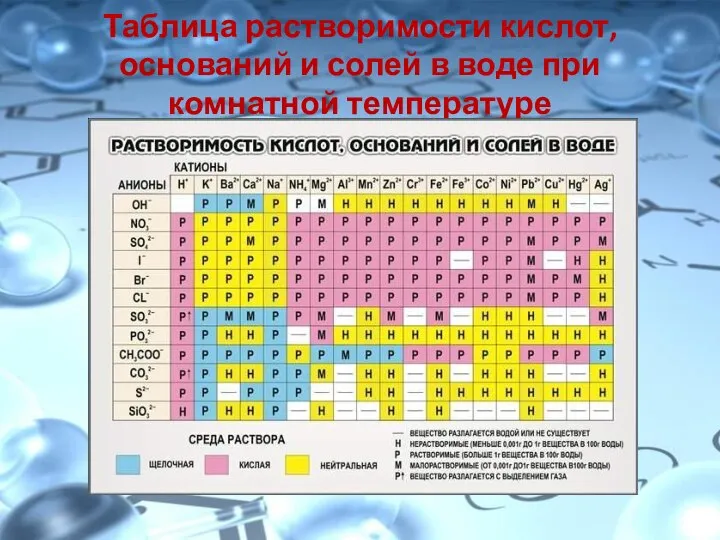
- 14. Таблица растворимости кислот, оснований и солей в воде при комнатной температуре
- 15. III) по количеству растворенного вещества Классификация растворов: Концентрированные Разбавленные Концентрированный раствор — раствор с высоким содержанием
- 16. Вставьте пропущенные слова: Природная вода практически не является чистым веществом, а представляет собой _____________. Растворы –
- 18. Скачать презентацию









 Строение соединений d-элементов
Строение соединений d-элементов Aлканы. Определение. Общая формула класса углеводородов
Aлканы. Определение. Общая формула класса углеводородов Углерод. Аллотропные модификации
Углерод. Аллотропные модификации Ендотермічні реакції на службі людини
Ендотермічні реакції на службі людини Фазовая диаграмма GaAs. Ретроградная растворимость. Селективная летучесть мышьяка из расплава. Методы борьбы с этими проблемами
Фазовая диаграмма GaAs. Ретроградная растворимость. Селективная летучесть мышьяка из расплава. Методы борьбы с этими проблемами Исследовательская работа «Волшебная соль»
Исследовательская работа «Волшебная соль» Фенол. Получение и использование, физические и химические свойства. Биологическая роль
Фенол. Получение и использование, физические и химические свойства. Биологическая роль Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент
Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент Презентация по Химии "Высшие природные полимеры - Белки и Нуклеиновые кислоты" - скачать смотреть
Презентация по Химии "Высшие природные полимеры - Белки и Нуклеиновые кислоты" - скачать смотреть  Введение. Развитие химической технологии как науки
Введение. Развитие химической технологии как науки Антибиотики-аминогликозиды: получение, свойства, исследование и применение. Связь между химическим строением и действием
Антибиотики-аминогликозиды: получение, свойства, исследование и применение. Связь между химическим строением и действием Вода - растворитель
Вода - растворитель Беседа с в 11 классе
Беседа с в 11 классе Простые и сложные вещества. Металлы и неметаллы. Бинарные соединения
Простые и сложные вещества. Металлы и неметаллы. Бинарные соединения Галогены. Основные химические свойства. Качественные реакции
Галогены. Основные химические свойства. Качественные реакции Алкалоидтар. Алкалоидтар туралы жалпы түсінік
Алкалоидтар. Алкалоидтар туралы жалпы түсінік Актиний
Актиний Краткий очерк истории развития химии
Краткий очерк истории развития химии Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой
Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой Неметаллы
Неметаллы Конфигурация макромолекулы
Конфигурация макромолекулы Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Содержание витамина С (аскорбиновой кислоты) в натуральных и консервированных соках.
Содержание витамина С (аскорбиновой кислоты) в натуральных и консервированных соках. Азотсодержащие вещества. Амины
Азотсодержащие вещества. Амины Открытая школа по химии
Открытая школа по химии Предмет и задачи биохимии. Белки. (Лекция 1)
Предмет и задачи биохимии. Белки. (Лекция 1) Radical Approach to the Chiral Quaternary Center in Asperaculin A: Synthesis of 9‑Deoxyasperaculin A
Radical Approach to the Chiral Quaternary Center in Asperaculin A: Synthesis of 9‑Deoxyasperaculin A Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно
Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно