Содержание
- 2. Литература 1. Попков В.А., Пузаков С.А. Общая химия: Учебник. - М.: ГЭОТАР-Медиа, 2007. -976 с. 2.Пузаков
- 3. 5.Биоорганическая химия. Учебник. (Тюкавкина Н.А., Бауков Ю.И.). 7 изд., Дрофа. 2008 – 543 с. 6.Руководство к
- 4. Интернет-источники http://www.chem.msu.su http://www.xumuk.ru/ http://www.alhimik.ru/ http://www.chemlib.ru http://alhimikov.net/ http://chemistry.narod.ru/ http://www.chemport.ru/
- 5. Значение химии в медицине 1.78 химических элементов входят в состав живых организмов. 2.44 элемента входят в
- 6. Задача, стоящая перед медиками в ближайшее время, предупреждать, а не лечить болезни. Чтобы стать высококвалифицированным специалистом
- 7. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
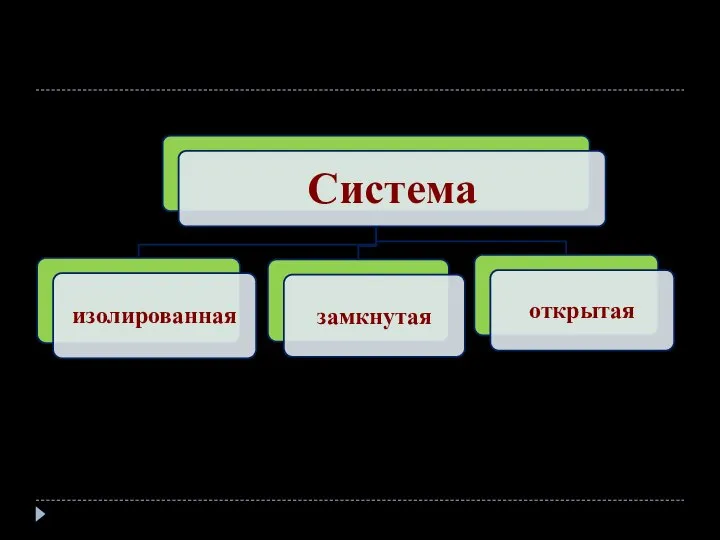
- 8. Термодинамика – наука, изучающая общие законы взаимного превращения одной формы энергии в другую. Система – это
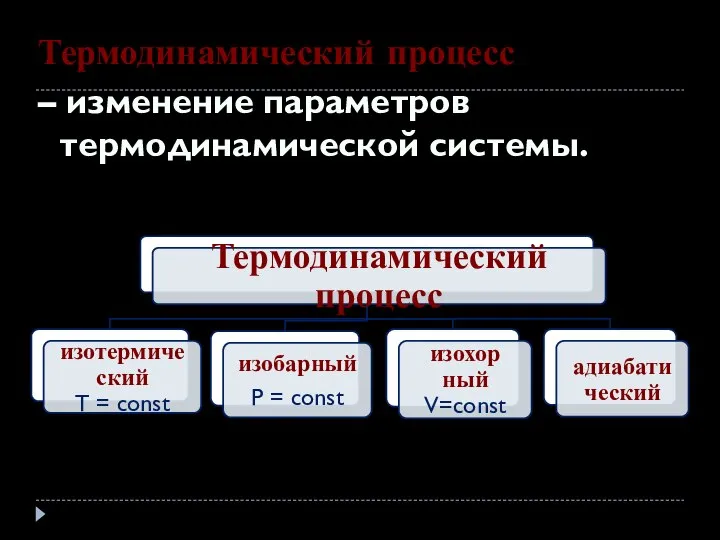
- 11. Термодинамический процесс – изменение параметров термодинамической системы.
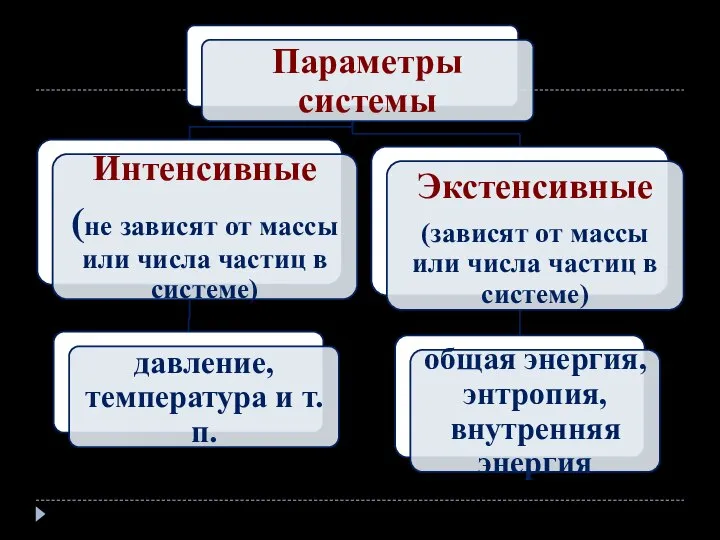
- 12. Энергия системы (W) - совокупность двух частей: зависящей от движения и положения системы как целого (Wц)
- 13. Внутренняя энергия разделяется на свободную энергию и связанную энергию: U = G + Wсв Свободная энергия
- 14. При сообщении термодинамической системе некоторого количества теплоты Q в общем случае происходит изменение внутренней энергии системы
- 15. Энергия расширенной системы, или внутреннее теплосодержание системы называется энтальпией (Н). Для экзотермических реакций Q>0, ΔH Для
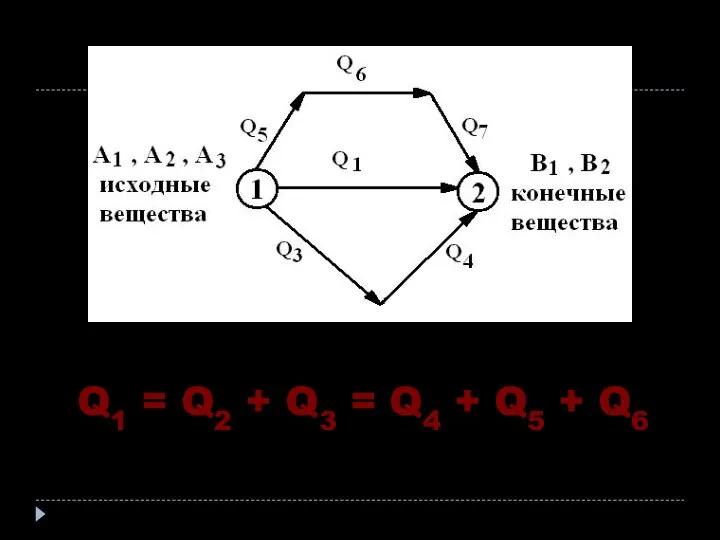
- 16. Q1 = Q2 + Q3 = Q4 + Q5 + Q6
- 17. I следствие закона Гесса где νн, νк - стехиометрические коэффициенты для реакции аА + bB→dD ∆Hреакц.
- 18. Величина и знак теплоты образования характеризуют устойчивость соединения в данных условиях Вещество NH3 PH3 AsH3 SbH3
- 19. Энтропия (S) - функция состояния термодинамической системы, используемая во втором законе т/д для выражения через нее
- 20. ΔG – изобарно-изотермический потенциал (свободная энергия Гиббса) ΔG = ΔH – T · ΔS где ΔH
- 21. Особенности живых организмов с позиции термодинамики 1.Живой организм – открытая система, непрерывно обменивающаяся с окружающей средой
- 22. 3. Все биохимические процессы, происходящие в клетках живых организмов, протекают при постоянной температуре, давлении, при незначительных
- 23. Главными компонентами пищи являются углеводы, жиры и белки. Калорийность, то есть энергия, выделяемая в процессе диссимиляции
- 24. ХИМИЧЕСКАЯ КИНЕТИКА И КАТАЛИЗ
- 25. Химическая кинетика занимается исследованием механизмов реакций и течения их во времени. Механизм реакции – последовательность и
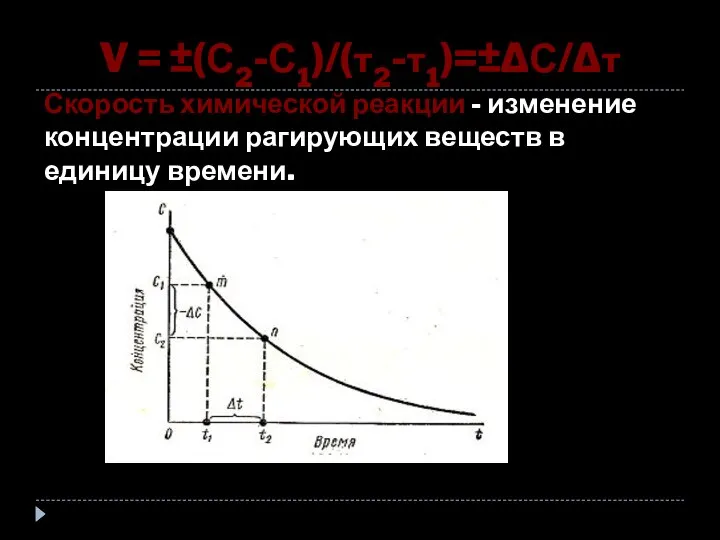
- 27. V = ±(С2-С1)/(τ2-τ1)=±ΔС/Δτ Скорость химической реакции - изменение концентрации рагирующих веществ в единицу времени.
- 29. Факторы, влияющие на скорость химических реакций Концентрация (давление) природа и дисперсность реагентов температура присутствие катализатора рН
- 30. Закон действующих масс (К. Гульдберг и П. Вааге) При постоянной температуре скорость химической реакции прямо пропорциональна
- 31. Реакции I порядка СuО(к) + Н2(г) = Сu(к) + Н2О (г) v=kC(H2) Реакции II порядка H2+
- 32. 2N2O5=4NO2+O2 N2O5=N2O3+O2 N2O3 + N2O5=4NO2
- 33. τ1/2 = Время, в течение которого прореагировала половина начального количества вещества, называется временем полураспада и обозначается
- 34. правило Вант - Гоффа γ (Δt/10)=kt+10/ kt γ - температурный коэффициент реакции, показывающий, во сколько раз
- 35. Энергия активации - избыточная энергия, которой должны обладать молекулы для того, чтобы их столкновение могло привести
- 36. Уравнение Аррениуса k = Aexp(-Ea/RT) ln k = - (Ea/RT) + C еxp (е) – основание
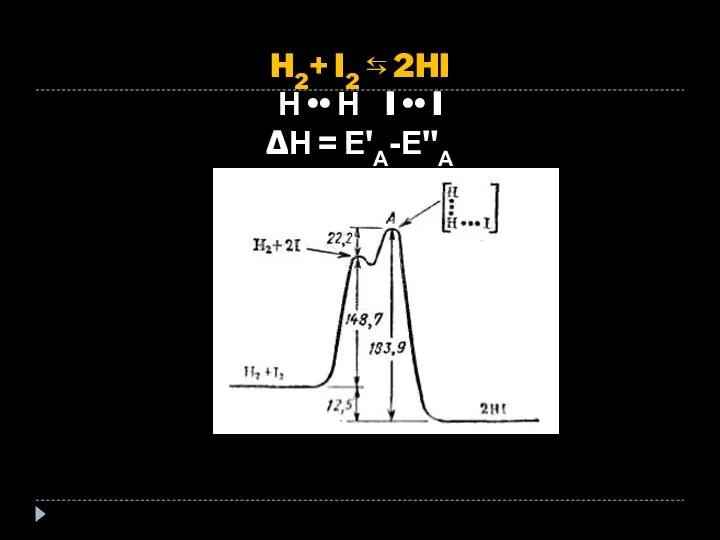
- 37. H2+ I2 ⇆ 2HI Н •• Н I •• I ΔН = Е'А-Е"А
- 38. Катализ
- 40. Механизм гомогенной каталитической реакции А+В К АВ A + K = AK AK + B =
- 41. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- 42. Mg+2HCl=MgCl2 + H2↑ Данная реакция протекает только в одном направлении и поэтому называется необратимой. H2+ I2⇆
- 43. Химическое равновесие — состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём
- 44. mA + nB ↔ pC + qD v1= k1 ·CАm ·CBn v2=k2 ·CCp ·CDq v1=v2 k1
- 45. ΔG°= -RT lnKр Если ΔG° Если же ΔG° > 0, то в равновесной смеси преобладают исходные
- 46. Принцип Ле-Шателье 2SO2(г)+О2(г)⇆2SO3(г),ΔH=396,1кДж/моль Т↑ ← С(SO2 ) ↑ → С(SO3 ) ↓ → Т↓ → С(SO2
- 48. Скачать презентацию







































 Основы безопасности при уничтожении химического оружия
Основы безопасности при уничтожении химического оружия Ароматичні аміни
Ароматичні аміни Аттестационная работа. Рабочая программа по курсу внеурочной деятельности для обучающихся 7 класса «Химия в профессиях»
Аттестационная работа. Рабочая программа по курсу внеурочной деятельности для обучающихся 7 класса «Химия в профессиях» Угольная кислота и ее производные. Сульфокислоты. (Лекция 12)
Угольная кислота и ее производные. Сульфокислоты. (Лекция 12)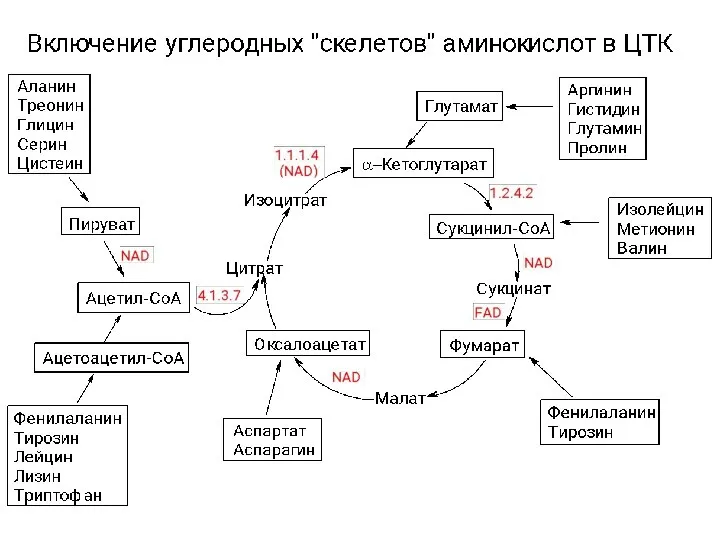 Катаболизм аминокислот
Катаболизм аминокислот Элементы химической кинетики
Элементы химической кинетики Электролитная адсорбция
Электролитная адсорбция Элементы подгруппы алюминия
Элементы подгруппы алюминия Фотолабораторный процесс. Основные этапы фото обработки. Рентгеновского изображения
Фотолабораторный процесс. Основные этапы фото обработки. Рентгеновского изображения Этилен. Действие этилена на рост проростков гороха
Этилен. Действие этилена на рост проростков гороха Аттестационная работа. Образовательная программа (элективный курс) Решение задач по химии
Аттестационная работа. Образовательная программа (элективный курс) Решение задач по химии Детонаційна стійкість бензину
Детонаційна стійкість бензину Ағзаның барлық жасушасындағы белок алмасу. Аминқышқылдарының дезаминденуі, пурин және пиримидиндердің ыдырауынан
Ағзаның барлық жасушасындағы белок алмасу. Аминқышқылдарының дезаминденуі, пурин және пиримидиндердің ыдырауынан Углеводородное топливо, его виды и назначения
Углеводородное топливо, его виды и назначения Aromatik uglevodorodlar (Arenlar)
Aromatik uglevodorodlar (Arenlar) Инертные газы
Инертные газы Презентация по Химии "сера" - скачать смотреть
Презентация по Химии "сера" - скачать смотреть  Аттестационная работа. Химия, помощница автолюбителю
Аттестационная работа. Химия, помощница автолюбителю Кристаллохимические радиусы
Кристаллохимические радиусы Органічні сполуки в побуті
Органічні сполуки в побуті  Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Содержание ртути и её соединений в воздухе при использовании осветительных ламп
Содержание ртути и её соединений в воздухе при использовании осветительных ламп Аттестационная работа. Мини-проекты на уроках химии. 8 класс
Аттестационная работа. Мини-проекты на уроках химии. 8 класс Виды химической связи (8 класс)
Виды химической связи (8 класс) Карбоновые кислоты
Карбоновые кислоты Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Молекулярные базы данных. Принцип действия и характеристики основных компьютерных программ
Молекулярные базы данных. Принцип действия и характеристики основных компьютерных программ Электроизоляционные материалы. Лаки и класки
Электроизоляционные материалы. Лаки и класки