Содержание
- 2. Что читать? Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. Ахметов Н. С. Общая
- 3. Сближение атомов Перекрывание 1s-АО при сближении атомов водорода Образование молекулярной орбитали в результате перекрывания двух 1s-АО:
- 4. Кулоновские силы При сближении двух атомов водорода электрон атома A притягивается к ядру атома B, а
- 5. Силы в природе Гравитационное взаимодействие Слабое ядерное взаимодействие Электромагнитное взаимодействие Сильное ядерное взаимодействие При сближении ядер
- 6. Сложение потенциалов электромагнитного и сильного ядерного взаимодействий Кулоновское взаимодействие Сильное ядерное взаимодействие
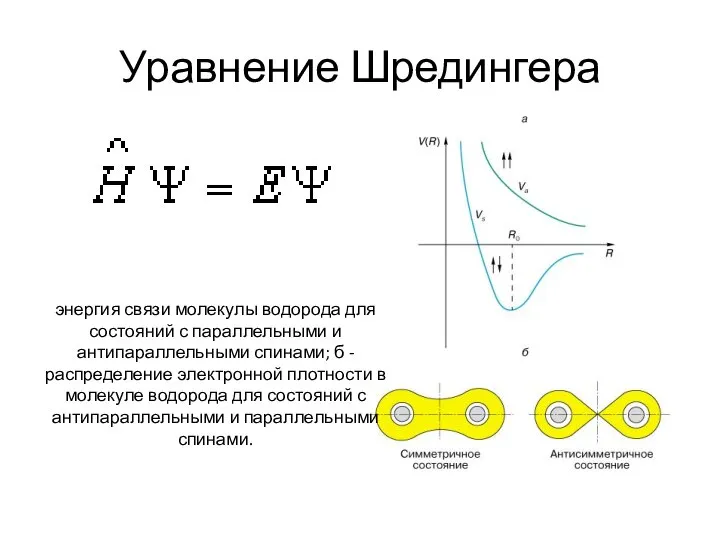
- 7. Уравнение Шредингера энергия связи молекулы водорода для состояний с параллельными и антипараллельными спинами; б - распределение
- 8. Диаграмма сближения атомов водорода
- 9. Химическая связь Химическая связь это энергетически выгодное взаимодействие атомов, приводящие к образованию устойчивых групп атомов (молекул).
- 10. Молекула Моле́кула (новолат. molecula, уменьшительное от лат. moles — масса) — электрически нейтральная частица, образованная из
- 11. Таблица типов связи
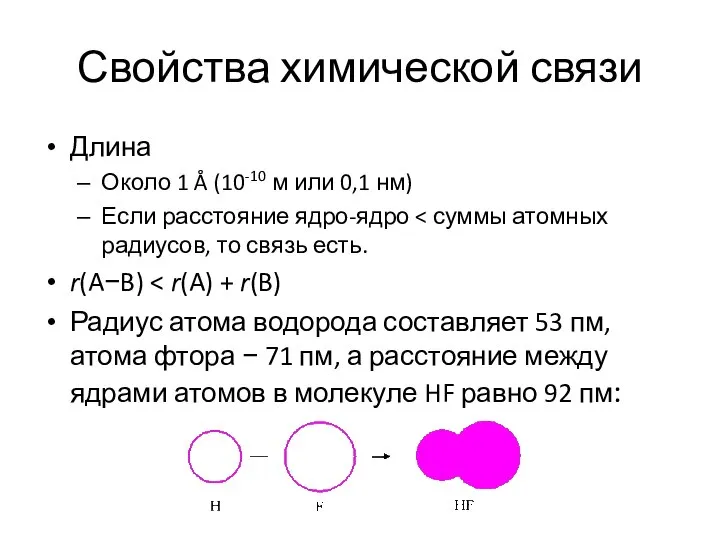
- 12. Свойства химической связи Длина Около 1 Å (10-10 м или 0,1 нм) Если расстояние ядро-ядро r(A−B)
- 13. Прочность энергия гомолитического разрыва. гомо - AB → А + В гетеро - AB → А+
- 14. Ковалентные связи Ковалентные химические связи обычно образуются при обобществлении принадлежащих первоначально разным атомам неспаренных электронов с
- 15. Ковалентные связи Донорно-акцепторный механизм образования ковалентной связи когда один из пары образующих связь атомов предоставляет пару
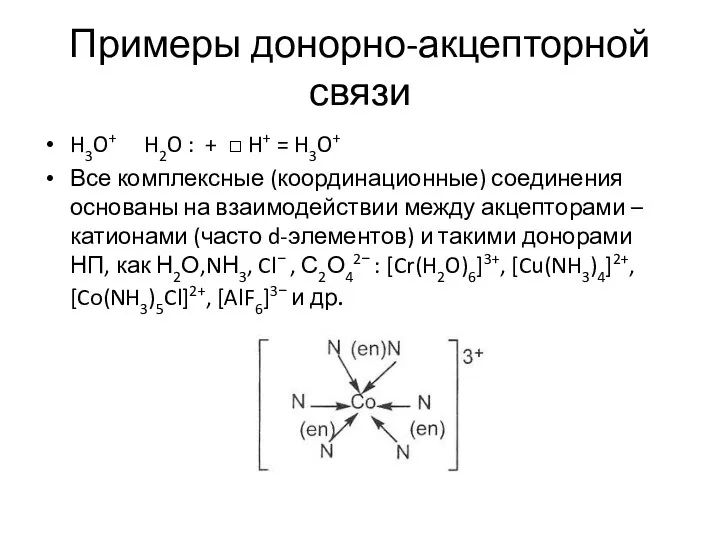
- 16. Примеры донорно-акцепторной связи H3O+ H2O : + □ H+ = H3O+ Все комплексные (координационные) соединения основаны
- 17. Электронные пары Участвующие в образовании связи обобществлённые пары электронов называют связывающими (СП), Не участвующие, принадлежащие и
- 18. Электронные пары
- 19. Радикалы Частицы с неспаренными электронами называются радикалами. Примеры радикалов: Н·, Сl·, ·ОН, ·СН3. Стабильные радикалы редки,
- 20. Электронные формулы Электроны изображаются точками
- 21. Структурные формулы Химические связи (связывающие электронные пары) обозначается черточками.
- 22. Стехиометрические формулы В стехиометрических формулах, (HCl, BCl3, H2O, H2S2, SO32– ит. п.), указан только состав частицы
- 23. Формулы
- 24. Химическое соединение Химическое соединение – вещество, состоящее из разных элементов в определенных соотношениях, т.е. имеющее определенный
- 25. Ковалентность / кратность связи ковалентность: количество образованных данным атомом ковалентных связей. Кратность связи = ковалентность.
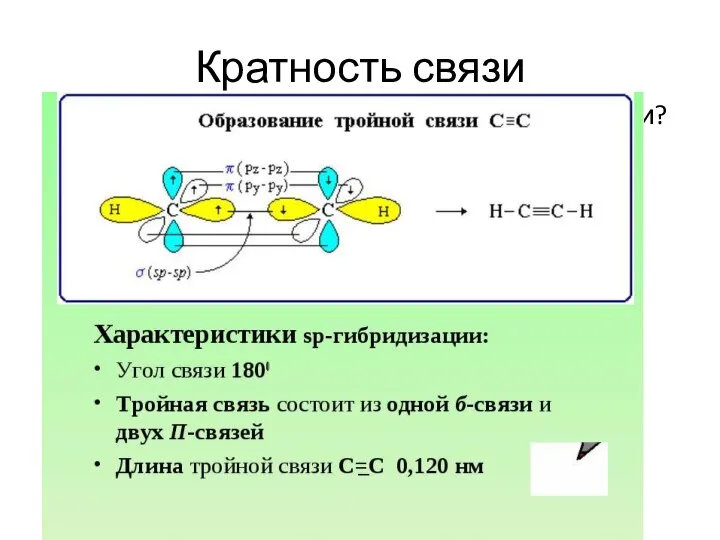
- 26. Кратность связи Откуда так много электронов между атомами? Сигма- и пи- связи (Ϭ- и π-)
- 27. Ковалентность / кратность связи Кратность связи может быть дробной H2+ H • H+ H … H+
- 28. Сопряжение связей Сопряжение в частицах СО2, N2О, ВО33− на основе резонанса
- 29. Насыщенность связи Насыщенность связи - максимально возможная ковалентность/кратность. Определяется: количеством орбиталей. Взаимодействие орбиталей крайне необходимо для
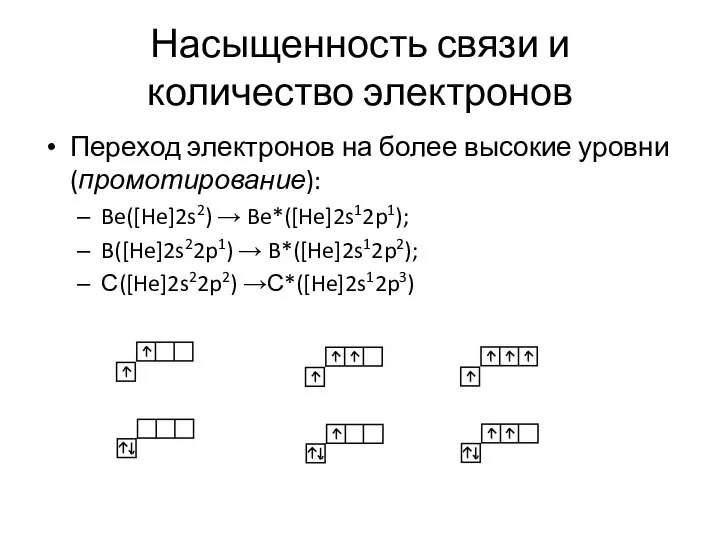
- 30. Насыщенность связи и количество электронов Переход электронов на более высокие уровни (промотирование): Be([He]2s2) → Be*([He]2s12p1); B([He]2s22p1)
- 31. Насыщенность связи и количество электронов N([He]2s22p3) →N*([He]2s12p33s1) Нужно много энергии. Да и валентность 1.
- 32. Насыщенность связи и количество электронов P([Ne]3s23p3) →P*([Ne]3s13p33d1)
- 33. Насыщенность связи и количество электронов O([He]2s22p6) → O*([He]2s12p43s1); F([He]2s22p1) → F*([He]2s12p53s1) Слишком большие энергии. Cl([Ne]3s23p5) →Cl*([Ne]3s13p33d3)
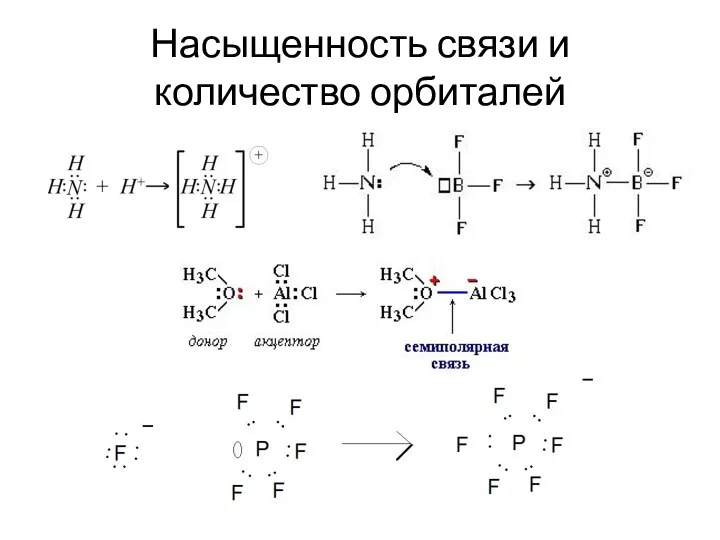
- 34. Насыщенность связи и количество орбиталей
- 35. КЧ Количество ближайших к выделенному атому соседних атомов (ближайших соседей) называют координационным числом(КЧ). Для частиц с
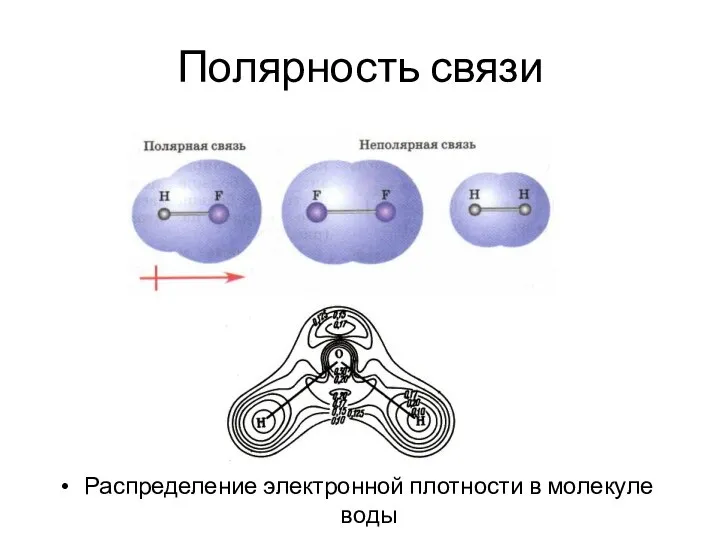
- 36. Полярность связи Распределение электронной плотности в молекуле воды
- 37. Смещение зарядов при полярной связи
- 38. Электроотрицательность Кто у кого забирает электроны? Электроотрицательность (ЭО) это свойство атомов оттягивать на себя электронную плотность
- 39. Степень окисления Степень окисления (СО) – условный заряд атома в соединении, если считать все связи полностью
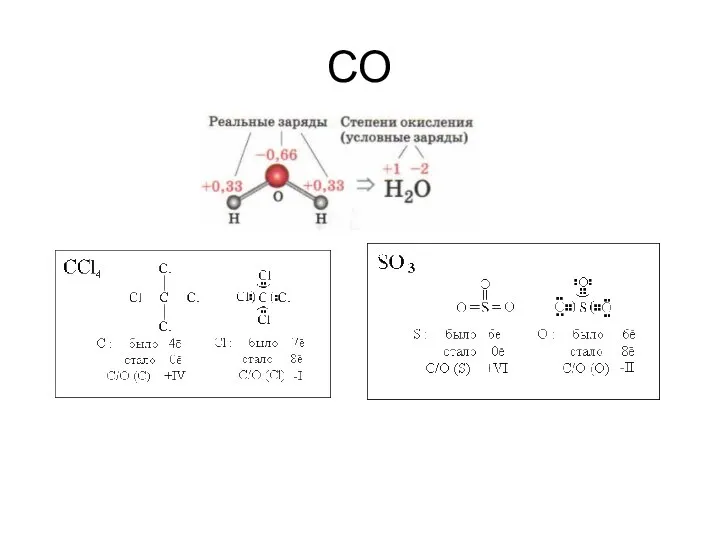
- 40. СО
- 41. Дипольный момент
- 42. Дипольный момент Дипольные моменты молекул обычно измеряют в дебаях (D): 1D = 3,34·10-30 Кл·м.
- 44. Скачать презентацию























![Насыщенность связи и количество электронов N([He]2s22p3) →N*([He]2s12p33s1) Нужно много энергии. Да и валентность 1.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397674/slide-30.jpg)
![Насыщенность связи и количество электронов P([Ne]3s23p3) →P*([Ne]3s13p33d1)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397674/slide-31.jpg)
![Насыщенность связи и количество электронов O([He]2s22p6) → O*([He]2s12p43s1); F([He]2s22p1) → F*([He]2s12p53s1) Слишком большие энергии. Cl([Ne]3s23p5) →Cl*([Ne]3s13p33d3)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397674/slide-32.jpg)






 Вклад ученых Казахстана в развитие органической химии
Вклад ученых Казахстана в развитие органической химии Metals
Metals Классификация нефтей и нефтепродуктов
Классификация нефтей и нефтепродуктов Гидролиз солей
Гидролиз солей Презентация Химический состав мороженного
Презентация Химический состав мороженного Квантовая механика- теоретическая основа современной химии
Квантовая механика- теоретическая основа современной химии Названия алканов
Названия алканов Обмен веществ и энергии в клетке
Обмен веществ и энергии в клетке Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования
Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования Железо, хром, марганец. Свойства, получение
Железо, хром, марганец. Свойства, получение Розв’язування задач і вправ з теми Алкани. 9 клас
Розв’язування задач і вправ з теми Алкани. 9 клас Алкалоиды природного происхождения
Алкалоиды природного происхождения II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Тема: «Алкины»
Тема: «Алкины»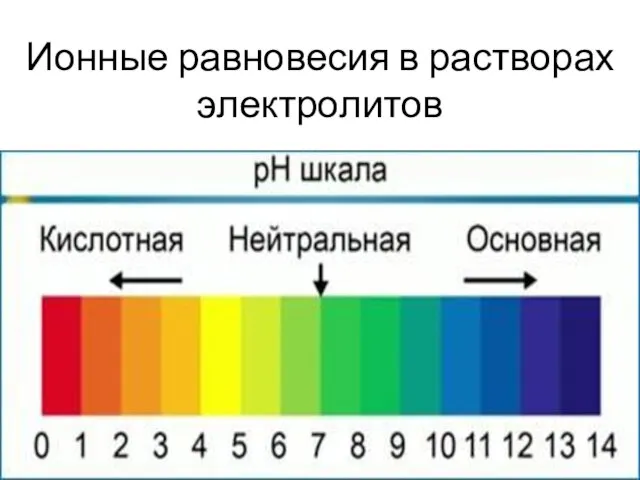 Ионные равновесия в растворах электролитов
Ионные равновесия в растворах электролитов Металлические стёкла (аморфные металлы)
Металлические стёкла (аморфные металлы) Алкины
Алкины Строение атома
Строение атома Презентация по Химии "Биохимия печени" - скачать смотреть
Презентация по Химии "Биохимия печени" - скачать смотреть  Нанохимия и нанотехнологии. Методы и средства исследования нанообъектов. (Лекция 3)
Нанохимия и нанотехнологии. Методы и средства исследования нанообъектов. (Лекция 3) Сера. Нахождение в природе. Химические свойства серы
Сера. Нахождение в природе. Химические свойства серы Anti-anxiety drugs
Anti-anxiety drugs Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Серебро - химический элемент в периодической таблице с атомным номером 47. 8 класс
Серебро - химический элемент в периодической таблице с атомным номером 47. 8 класс Нефть и способы её переработки
Нефть и способы её переработки Именные реакции в органической химии
Именные реакции в органической химии Неоднородные системы (процессы и аппараты химической технологии, 8 лекция)
Неоднородные системы (процессы и аппараты химической технологии, 8 лекция) Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока
Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока