Содержание
- 2. Амины – органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены
- 3. Свойства аминов В аминах имеются связи С–Н и С–C , а также связи N–H и N–C.
- 4. Физические свойства аминов Связь N–H является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные связи
- 5. Химические свойства аминов Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Модели молекул
- 6. Основность аминов Для аминов характерны ярко выраженные основные свойства (за что их часто называют органическими основаниями).
- 7. Окисление аминов Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные амины
- 8. Взаимодействие с азотистой кислотой Азотистая кислота HNO2 - неустойчивое соединение. Поэтому она используется только в момент
- 9. Анилин Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов: Он находит широкое применение в качестве полупродукта
- 10. Анилин Такое взаимное влияние атомов в молекуле анилина объясняется сопряжением π-электронов бензольного кольца с неподеленной электронной
- 11. Получение аминов В аминах атом азота находится в низшей степени окисления, поэтому многие способы их получения
- 12. Получение аминов 3. Восстановление нитрилов с образованием первичных аминов: R-C N + 4[H] R-CH2NH2 Этим способом
- 13. Аминокислоты Аминокислоты — органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы -NH2.
- 14. Свойства аминокислот Физические свойства. Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в
- 15. Свойства аминокислот Как карбоновые кислоты они образуют функциональные производные: а) соли H2N–CH2–COOH + NaOH H2N–CH2–COO– Na+
- 16. Получение аминокислот 1. Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах: 2. Присоединение аммиака к α,β-непредельным
- 17. Белки Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями. Формально образование белковой
- 18. Белки Функции белков в природе универсальны: каталитические (ферменты); регуляторные (гормоны); структурные (кератин шерсти, фиброин шелка, коллаген);
- 19. Белки Выделяют 4 уровня структурной организации белков.
- 20. Нуклеиновые кислоты Нуклеиновые кислоты - это биополимеры, макромолекулы которых состоят из многократно повторяющихся звеньев - нуклеотидов.
- 22. Скачать презентацию
Амины – органические производные аммиака NH3, в молекуле которого один, два
Амины – органические производные аммиака NH3, в молекуле которого один, два
Амины
Простейший представитель – метиламин:
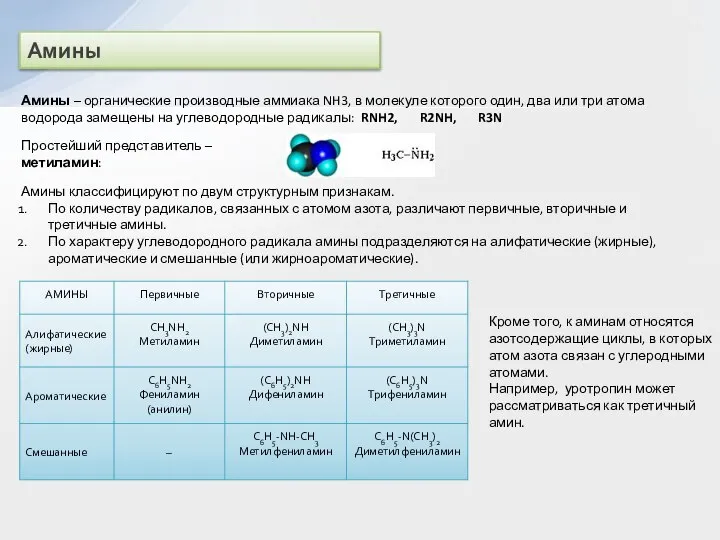
Амины классифицируют по двум структурным признакам.
По количеству радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины.
По характеру углеводородного радикала амины подразделяются на алифатические (жирные), ароматические и смешанные (или жирноароматические).
Кроме того, к аминам относятся азотсодержащие циклы, в которых атом азота связан с углеродными атомами. Например, уротропин может рассматриваться как третичный амин.
Свойства аминов
В аминах имеются связи С–Н и С–C , а также
Свойства аминов
В аминах имеются связи С–Н и С–C , а также
Нуклеофильность - способность частицы предоставить электронную пару на образование связи с углеродом или с другим положительно заряженным атомом, кроме протона (H+). Стремление отдать пару электронов протону называется основностью.
Кроме того, атом азота в аминах имеет самую низкую для этого элемента степень окисления (-3). Поэтому амины могут вступать в реакции окисления по связям C–N и N–H, проявляя восстановительные свойства.
Физические свойства аминов
Связь N–H является полярной, поэтому первичные и вторичные амины
Физические свойства аминов
Связь N–H является полярной, поэтому первичные и вторичные амины
Это объясняет относительно высокую температуру кипения аминов по сравнению с неполярными соединениями со сходной молекулярной массой. Например:
Третичные амины не образуют ассоциирующих водородных связей (отсутствует группа N–H). Поэтому их температуры кипения ниже, чем у изомерных первичных и вторичных аминов (триэтиламин кипит при 89 °С, ан-гексиламин – при 133 °С).
По сравнению со спиртами алифатические амины имеют более низкие температуры кипения (т. кип. метиламина -6 °С, т. кип. метанола +64,5 °С). Это свидетельствует о том, что амины ассоциированы в меньшей степени, чем спирты, поскольку прочность водородных связей с атомом азота меньше, чем с участием более электроотрицательного кислорода.
При обычной температуре только низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха. Ароматические амины – бесцветные высококипящие жидкости или твердые вещества.
Амины способны к образованию водородных связей с водой:
Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается, т.к. увеличиваются пространственные препятствия образованию водородных связей. Ароматические амины в воде практически не растворяются.
Химические свойства аминов
Амины имеют сходное с аммиаком строение и проявляют подобные
Химические свойства аминов
Амины имеют сходное с аммиаком строение и проявляют подобные
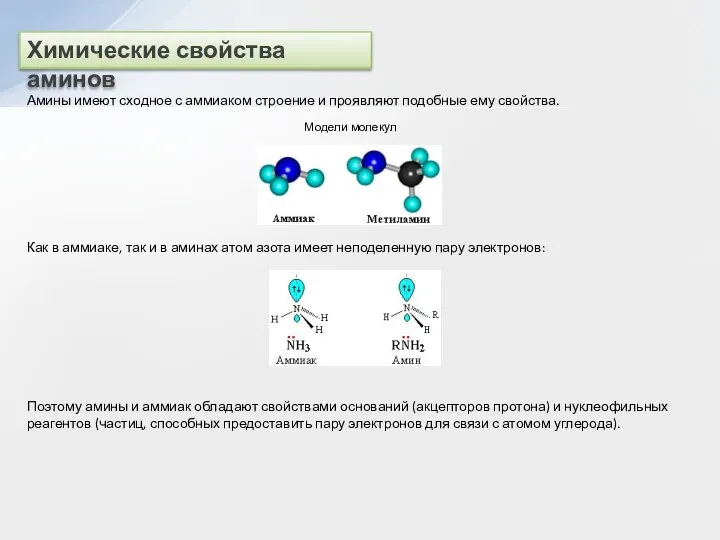
Модели молекул
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов:
Поэтому амины и аммиак обладают свойствами оснований (акцепторов протона) и нуклеофильных реагентов (частиц, способных предоставить пару электронов для связи с атомом углерода).
Основность аминов
Для аминов характерны ярко выраженные основные свойства (за что их
Основность аминов
Для аминов характерны ярко выраженные основные свойства (за что их
1. Водные растворы алифатических аминов проявляют щелочную реакцию, т.к. при их взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония:
Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами.
Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H2SO4) и, в отличие от алифатических аминов и аммиака, не образует с водой гидроксида.
2. Взаимодействуя с кислотами, амины образуют соли:
Соли аминов – твердые вещества, хорошо растворимые в воде. Щелочи (более сильные основания) легко вытесняют из них амины:
Основность простейших аминов (в растворе) возрастает в ряду:
C6H5NH2 < NH3 < (CH3)3N < CH3NH2 < (CH3)2NH
Окисление аминов
Алифатические амины окисляются под действием сильных окислителей. В отличие от
Окисление аминов
Алифатические амины окисляются под действием сильных окислителей. В отличие от
4СH3NH2 + 9O2 4CO2 + 10H2O + 2N2
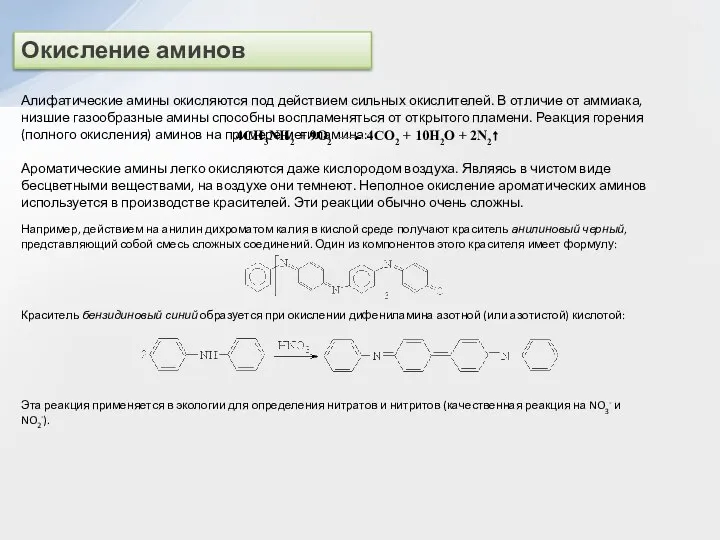
Ароматические амины легко окисляются даже кислородом воздуха. Являясь в чистом виде бесцветными веществами, на воздухе они темнеют. Неполное окисление ароматических аминов используется в производстве красителей. Эти реакции обычно очень сложны.
Например, действием на анилин дихроматом калия в кислой среде получают краситель анилиновый черный, представляющий собой смесь сложных соединений. Один из компонентов этого красителя имеет формулу:
Краситель бензидиновый синий образуется при окислении дифениламина азотной (или азотистой) кислотой:
Эта реакция применяется в экологии для определения нитратов и нитритов (качественная реакция на NO3- и NO2-).
Взаимодействие с азотистой кислотой
Азотистая кислота HNO2 - неустойчивое соединение. Поэтому она используется
Взаимодействие с азотистой кислотой
Азотистая кислота HNO2 - неустойчивое соединение. Поэтому она используется
KNO2 + HCl НNO2 + KCl
Строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различения первичных, вторичных и третичных аминов. Важное практическое значение имеет реакция азотистой кислоты с первичными ароматическими аминами
Первичные алифатические амины c HNO2 образуют спирты. Характерным признаком реакции является выделение азота (дезаминирование аминов):
Первичные ароматические амины при комнатной температуре реагируют аналогично, образуя фенолы и выделяя азот. При низкой температуре (около 0 °С) реакция идет иначе .
Вторичные амины (алифатические, ароматические и смешанные) под действием HNO2 превращаются внитрозоамины R2N-N=O – маслообразные вещества желтого цвета (нитрозо – название группы -N=O):
Третичные алифатические амины при комнатной температуре и низкой концентрации HNO2 с ней не реагируют. Реакция при нагревании приводит к образованию смеси продуктов и не имеет практического значения.
Третичные жирноароматические амины при действии азотистой кислоты вступают в реакцию электрофильного замещения по бензольному кольцу и превращаются в пара-нитрозопроизводные(кристаллические вещества зеленого цвета):
Анилин
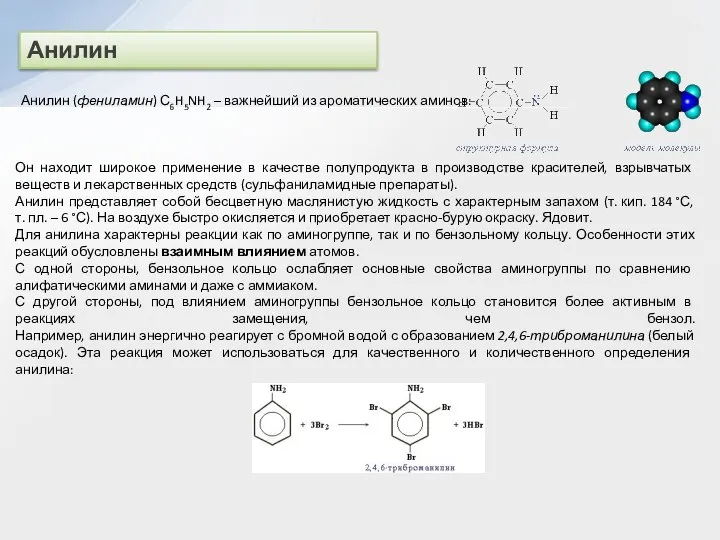
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
Он находит широкое применение в
Анилин
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
Он находит широкое применение в
Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип. 184 °С, т. пл. – 6 °С). На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов.
С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком.
С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок). Эта реакция может использоваться для качественного и количественного определения анилина:
Анилин
Такое взаимное влияние атомов в молекуле анилина объясняется сопряжением π-электронов бензольного
Анилин
Такое взаимное влияние атомов в молекуле анилина объясняется сопряжением π-электронов бензольного
Практическое значение имеет реакция анилина с азотистой кислотой при пониженной температуре (около 0 °С). В результате этой реакции (реакции диазотирования) образуются соли диазония (арилдиазониевые соли), которые используются в синтезе азокрасителей и ряда других соединений.
При более высокой температуре реакция идет с выделением азота и анилин превращается в фенол:
Подобно анилину реагируют с азотистой кислотой и другие первичные ароматические амины.
Получение аминов
В аминах атом азота находится в низшей степени окисления, поэтому
Получение аминов
В аминах атом азота находится в низшей степени окисления, поэтому
Наиболее общим методом получения первичных аминов является восстановление нитросоединений:
Важнейший ароматический амин - анилин - образуется при восстановлении нитробензола (восстановители - водород в присутствии металлических катализаторов, Fe + HCl, сульфиды):
Эта реакция носит имя русского химика Н.Н. Зинина, осуществившего ее впервые в 1842 г.
2. Восстановление амидов (восстановитель - алюмогидрид лития LiAH4):
Получение аминов
3. Восстановление нитрилов с образованием первичных аминов:
R-C N + 4[H]
Получение аминов
3. Восстановление нитрилов с образованием первичных аминов:
R-C N + 4[H]
Этим способом в промышленности получают гексаметилендиамин, который используется в производстве полиамидного волокна найлон.
4. Получение аминов путём введения алкильных групп в молекулы аммиака и аминов (реакции алкилирования).
При нагревании галогеналканов с аммиаком образуется смесь первичных, вторичных и третичных аминов.
В основе этих превращений лежит реакция нуклеофильного замещения галогена в галогеналканах. Роль нуклеофила играют молекулы аммиака и аминов, имеющие неподеленную пару электронов на атоме азота.
В промышленности алкилирование аммиака в большинстве случаев проводится не галогеналканами, а спиртами, в молекулах которых происходит нуклеофильное замещение ОН-группы на аминогруппу.
Действием галогеналканов на первичные алифатические и ароматические амины получают вторичные и третичные амины, в том числе, смешанные.
Аминокислоты
Аминокислоты — органические бифункциональные соединения, в состав которых входят карбоксильные группы
Аминокислоты
Аминокислоты — органические бифункциональные соединения, в состав которых входят карбоксильные группы
Простейший представитель — аминоуксусная кислота H2N-CH2-COOH (глицин)
Аминокислоты классифицируют по двум структурным признакам.
В зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты подразделяют на α-, β-, γ-, δ-, ε- и т. д.
По характеру углеводородного радикала различают алифатические (жирные) и ароматические аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду. Примером ароматической аминокислоты может служить пара-аминобензойная кислота:
Свойства аминокислот
Физические свойства. Аминокислоты – твердые кристаллические вещества с высокой температурой
Свойства аминокислот
Физические свойства. Аминокислоты – твердые кристаллические вещества с высокой температурой
Аминокислоты с одной карбоксильной группой и одной аминогруппой имеют нейтральную реакцию.
Аминокислоты как амфотерные соединения образуют соли как с кислотами (по группе NH2), так и со щелочами (по группе СООН):
С ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.
Химические свойства. Аминокислоты проявляют свойства оснований за счет аминогруппы и свойства кислот за счет карбоксильной группы, т.е. являются амфотерными соединениями. Подобно аминам, они реагируют с кислотами с образованием солей аммония:
H2N–CH2–COOH + HCl [H3N+–CH2–COOH] Cl–
Свойства аминокислот
Как карбоновые кислоты они образуют функциональные производные:
а) соли
H2N–CH2–COOH + NaOH
Свойства аминокислот
Как карбоновые кислоты они образуют функциональные производные:
а) соли
H2N–CH2–COOH + NaOH
б) сложные эфиры
Кроме того, возможно взаимодействие амино- и карбоксильной групп как внутри одной молекулы (внутримолекулярная реакция), так и принадлежащих разным молекулам (межмолекулярная реакция).
Практическое значение имеет внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона):
Межмолекулярное взаимодействие α-аминокислот приводит к образованию пептидов. При взаимодействии двух α-аминокислот образуется дипептид.
Межмолекулярная реакция с участием трех α-аминокислот приводит к образованию трипептида и т.д.
Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH - пептидной связью.
Важнейшие природные полимеры - белки - относятся к полипептидам, т.е. представляют собой продукт поликонденсации α-аминокислот
Получение аминокислот
1. Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:
2. Присоединение
Получение аминокислот
1. Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:
2. Присоединение
CH2=CH–COOH + NH3 H2N–CH2–CH2–COOH
3. α-Аминокислоты образуются при гидролизе пептидов и белков.
4. Восстановление нитрозамещенных карбоновых кислот (применяется обычно для получения ароматических аминокислот):
O2N-C6H4-COOH + 3H2 H2N-C6H4-COOH + 2H2O
5. Биотехнологический способ получения чистых α-аминокислот в виде индивидуальных оптических изомеров. Этот способ основан на способности специальных микроорганизмов вырабатывать в питательной среде определенную аминокислоту.
Белки
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными)
Белки
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными)
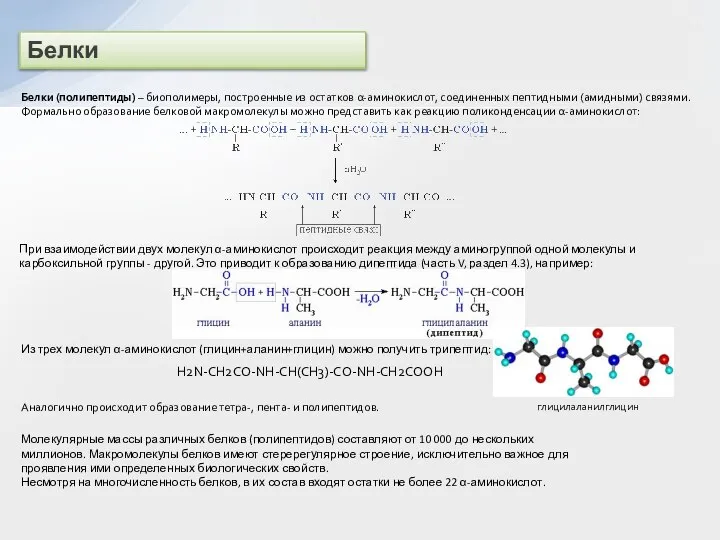
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:
При взаимодействии двух молекул α-аминокислот происходит реакция между аминогруппой одной молекулы и карбоксильной группы - другой. Это приводит к образованию дипептида (часть V, раздел 4.3), например:
Из трех молекул α-аминокислот (глицин+аланин+глицин) можно получить трипептид:
H2N-CH2CO-NH-CH(CH3)-CO-NH-CH2COOH
глицилаланилглицин
Аналогично происходит образование тетра-, пента- и полипептидов.
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов. Макромолекулы белков имеют стеререгулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Несмотря на многочисленность белков, в их состав входят остатки не более 22 α-аминокислот.
Белки
Функции белков в природе универсальны:
каталитические (ферменты);
регуляторные (гормоны);
структурные (кератин шерсти, фиброин шелка,
Белки
Функции белков в природе универсальны:
каталитические (ферменты);
регуляторные (гормоны);
структурные (кератин шерсти, фиброин шелка,
двигательные (актин, миозин);
транспортные (гемоглобин);
запасные (казеин, яичный альбумин);
защитные (иммуноглобулины) и т.д.
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Белки
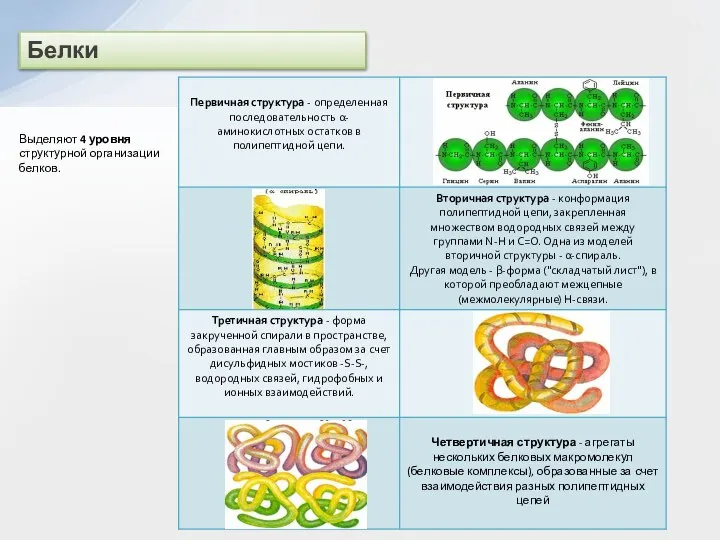
Выделяют 4 уровня структурной организации белков.
Белки
Выделяют 4 уровня структурной организации белков.
Нуклеиновые кислоты
Нуклеиновые кислоты - это биополимеры, макромолекулы которых состоят из многократно
Нуклеиновые кислоты
Нуклеиновые кислоты - это биополимеры, макромолекулы которых состоят из многократно
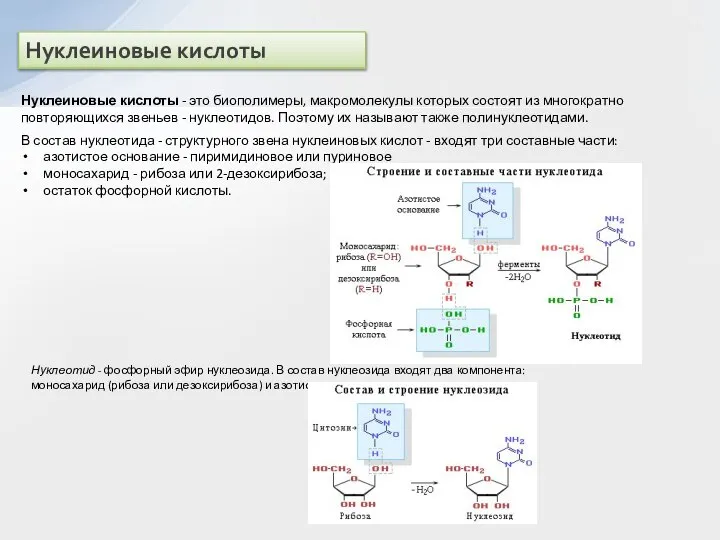
В состав нуклеотида - структурного звена нуклеиновых кислот - входят три составные части:
азотистое основание - пиримидиновое или пуриновое
моносахарид - рибоза или 2-дезоксирибоза;
остаток фосфорной кислоты.
Нуклеотид - фосфорный эфир нуклеозида. В состав нуклеозида входят два компонента: моносахарид (рибоза или дезоксирибоза) и азотистое основание.











 Презентация по Химии "Природные источники углеводородов" - скачать смотреть бесплатно
Презентация по Химии "Природные источники углеводородов" - скачать смотреть бесплатно Физические свойства металлов
Физические свойства металлов Нафта та її переробка
Нафта та її переробка  Презентация по Химии "Искусственные полимеры" - скачать смотреть
Презентация по Химии "Искусственные полимеры" - скачать смотреть  Сильные и слабые электролиты. Степень диссоциации
Сильные и слабые электролиты. Степень диссоциации Гидролиз. Лекция 03-2
Гидролиз. Лекция 03-2 Презентация по Химии "Водорастворимый упаковочный материал" - скачать смотреть
Презентация по Химии "Водорастворимый упаковочный материал" - скачать смотреть  Виды композитных материалов, исследование их свойств и областей применения
Виды композитных материалов, исследование их свойств и областей применения Непредельные углеводороды - алкены
Непредельные углеводороды - алкены Лизиметр
Лизиметр Положение азота и фосфора в периодической системе химических элементов, строение их атомов. Азот: свойства и применение
Положение азота и фосфора в периодической системе химических элементов, строение их атомов. Азот: свойства и применение Адсорбция на твердых телах
Адсорбция на твердых телах Physical chemistry of nanostructured systems.( lecture no. 7)
Physical chemistry of nanostructured systems.( lecture no. 7) Энтропия. Изменение энтропии в изопроцессах
Энтропия. Изменение энтропии в изопроцессах Система приготовления и подачи реагентов KPJ
Система приготовления и подачи реагентов KPJ Физические и химические явления
Физические и химические явления Галогены
Галогены Обмен нуклеотидов. Матричные биосинтезы
Обмен нуклеотидов. Матричные биосинтезы Транспорт веществ через биологические мембраны. (Лекция 12)
Транспорт веществ через биологические мембраны. (Лекция 12) Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Практика по химии
Практика по химии Катализ. Гетерогенные катализаторы
Катализ. Гетерогенные катализаторы Химическая кинетика, химическое равновесие и катализ
Химическая кинетика, химическое равновесие и катализ Качественные реакции
Качественные реакции Курс химии (Литвиновой Татьяны Николаевны)
Курс химии (Литвиновой Татьяны Николаевны) Тема урока ОСНОВАНИЯ
Тема урока ОСНОВАНИЯ Аттестационная работа. Образовательная программа (элективный курс) Решение задач по химии
Аттестационная работа. Образовательная программа (элективный курс) Решение задач по химии Презентация по Химии "Методы разделения и концентрирования" - скачать смотреть бесплатно
Презентация по Химии "Методы разделения и концентрирования" - скачать смотреть бесплатно