Содержание
- 3. С новым годом! Всем здоровья, успехов в учебе и спорте!
- 4. Биохимия изучает: Химический состав организма (строение и свойства молекул, входящих в состав организма); Обмен веществ (химические
- 5. Роль биохимии в подготовке специалиста в области физической культуры и спорта Специалист в области физической культуры
- 6. Тренер и преподаватель физического воспитания должны знать особенности обмена веществ во время физической работы и отдыха,
- 7. Биохимия является базовой, фундаментальной дисциплиной, создающей необходимые предпосылки для последующего освоения других медико-биологических предметов, а также
- 9. 2009, 2010
- 10. Химический состав организма Вода – 60-65 % (≈ 2/3 от массы тела) Органические соединения - 30-32
- 11. Органические соединения 1. Белки 2. Нуклеиновые кислоты 3. Углеводы 4. Липиды
- 12. Б Е Л К И
- 13. Биологические функции белков
- 14. Структурная (строительная, пластическая) функция Эта функция заключается в том, белки являются универсальным строительным материалом, из которого
- 15. Транспортная функция Белковые молекулы имеют большой размер, хорошо растворимы в воде и, перемещаясь по водным пространствам
- 16. Каталитическая функция В организме имеются особые белки, являющиеся катализаторами химических реакций; Такие белки получили название ферменты
- 17. Сократительная функция В основе всех форм движения и в первую очередь мышечного сокращения и расслабления лежит
- 18. Защитная функция Белки выполняют защитную функцию, участвуя в обеспечении иммунитета; К защитной функции относится участие белков
- 19. Энергетическая функция Окисление белков, как и всех других органических соединений, сопровождается выделением энергии; Однако роль белков
- 20. Исходя из важнейшей биологической роли белков в организме, их еще называют протеинами (от греч. рroteus –
- 21. Строение белков
- 22. Белки - высокомолекулярные азотсодержащие соединения, состоящие из аминокислот; В одну молекулу белков входят десятки, сотни, тысячи
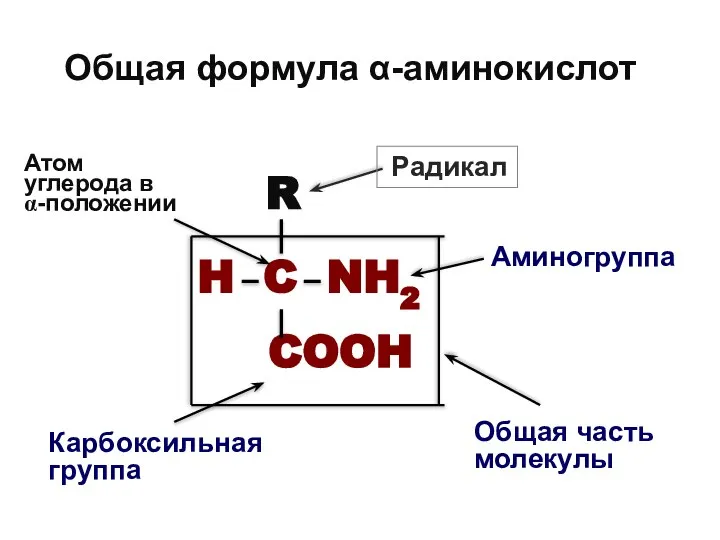
- 23. Общая формула α-аминокислот R H C NH2 COOH Общая часть молекулы Радикал Аминогруппа Карбоксильная группа Атом
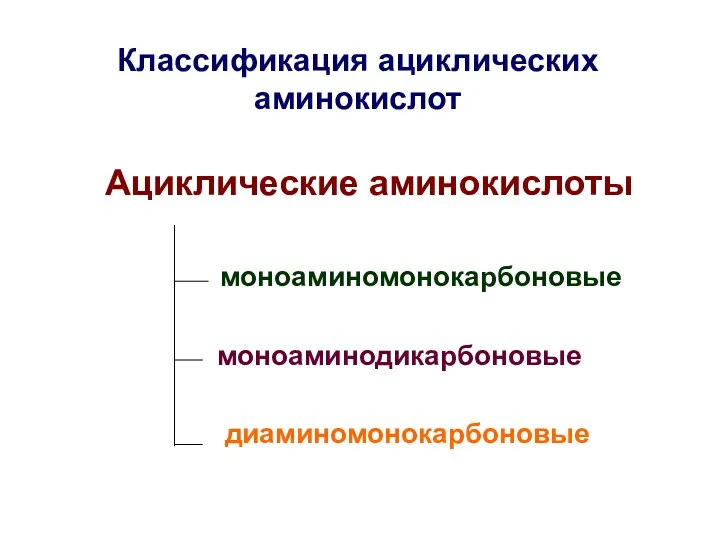
- 24. Классификация ациклических аминокислот Ациклические аминокислоты моноаминомонокарбоновые моноаминодикарбоновые диаминомонокарбоновые
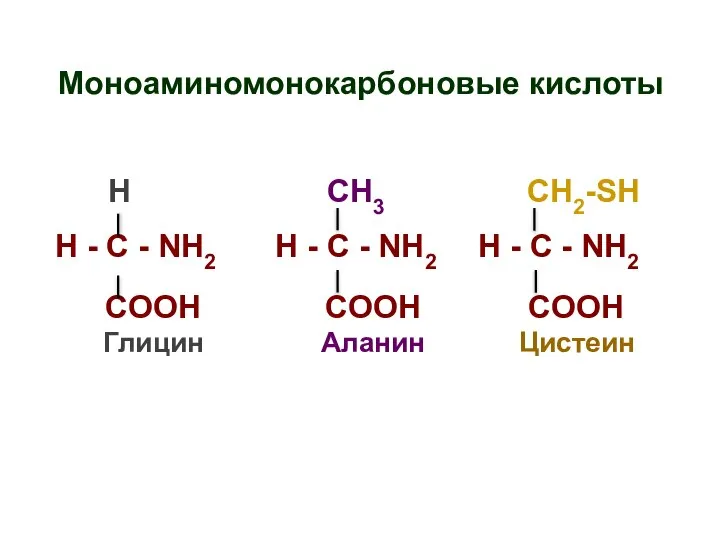
- 25. Моноаминомонокарбоновые кислоты H СН3 СН2-SH H - C - NH2 H - C - NH2 H
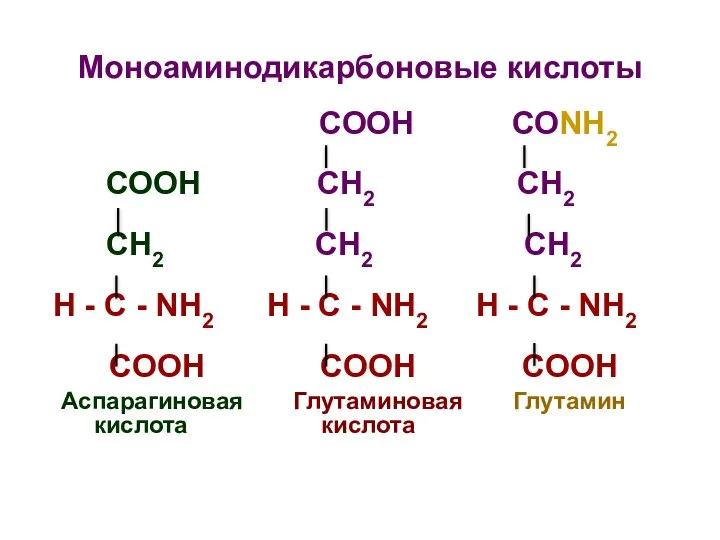
- 26. Моноаминодикарбоновые кислоты СООН СОNH2 СООН СН2 СН2 СH2 СН2 СН2 H - C - NH2 H
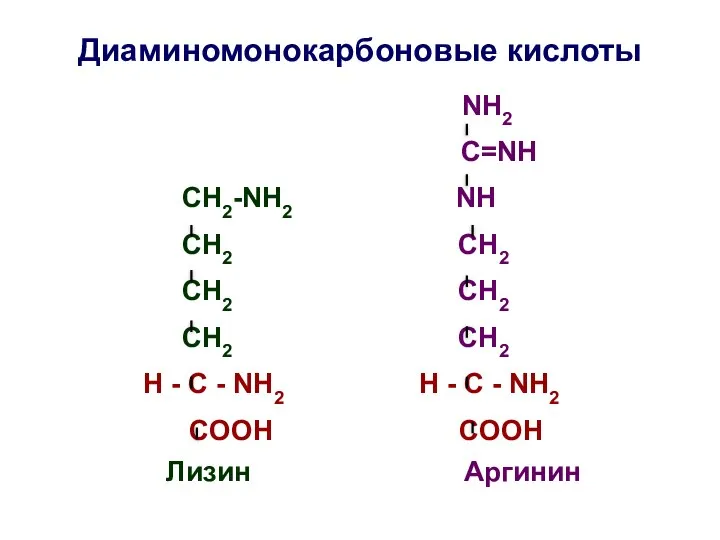
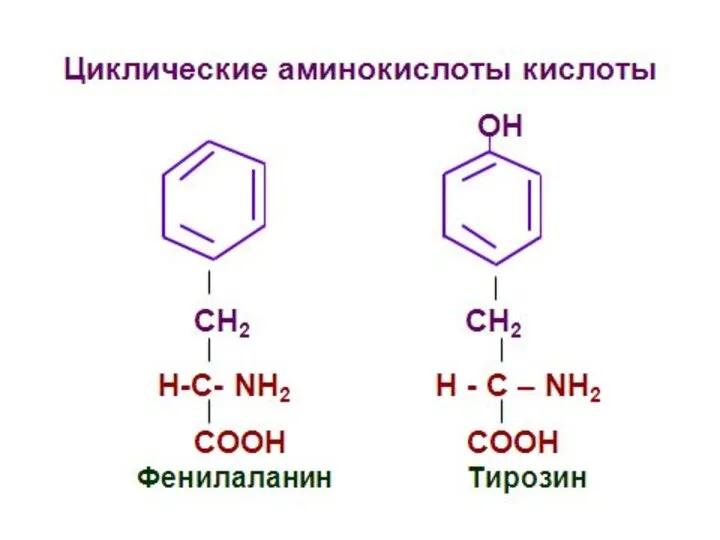
- 27. Диаминомонокарбоновые кислоты NH2 C=NH СН2-NH2 NH СH2 СH2 СН2 СН2 СH2 СН2 H - C -
- 29. В молекуле белка аминокислоты, соединяясь друг с другом, образуют длинные неразветвленные цепи под названием полипептиды; Химическая
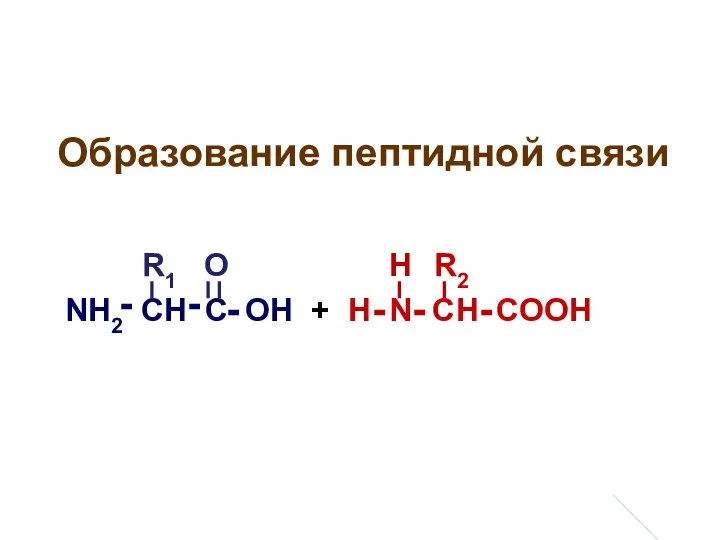
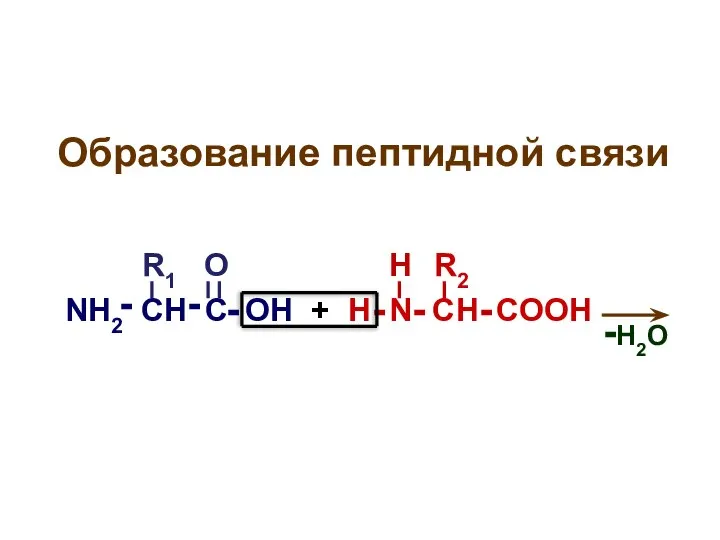
- 30. Образование пептидной связи NH2 CH C OH + H N CH COOH R1 R2 - -
- 31. Образование пептидной связи NH2 CH C OH + H N CH COOH R1 R2 - -
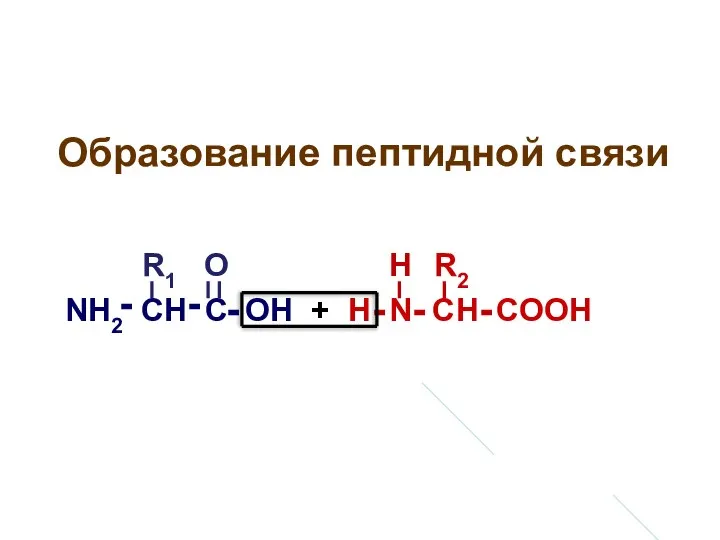
- 32. Образование пептидной связи NH2 CH C OH + H N CH COOH R1 R2 - -
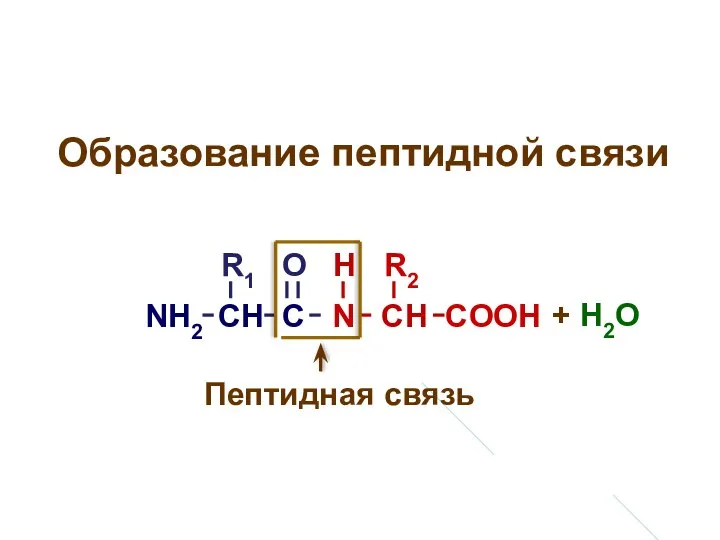
- 33. Образование пептидной связи NH2 CH C N CH COOH R1 R2 О Н + H2O Пептидная
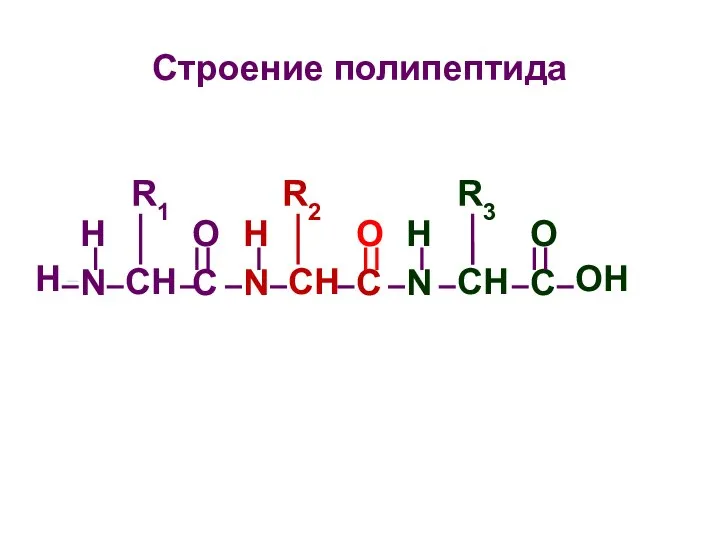
- 34. Строение полипептида H N O C O C H N O C OH CH CH CH
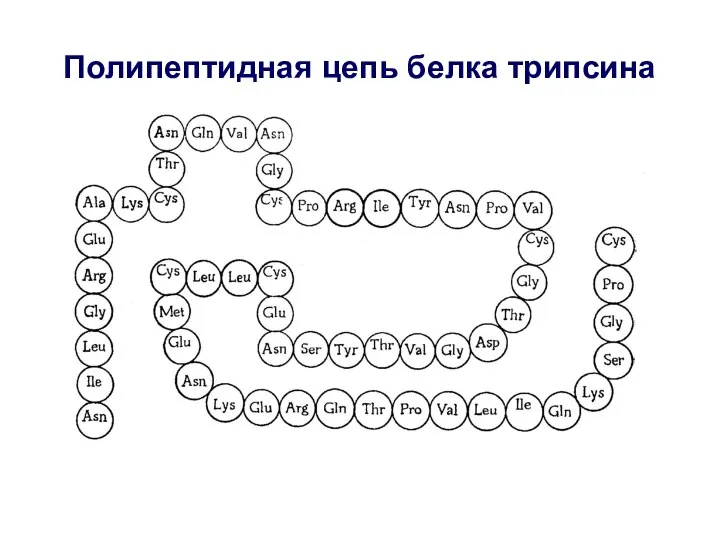
- 35. Полипептидная цепь белка трипсина
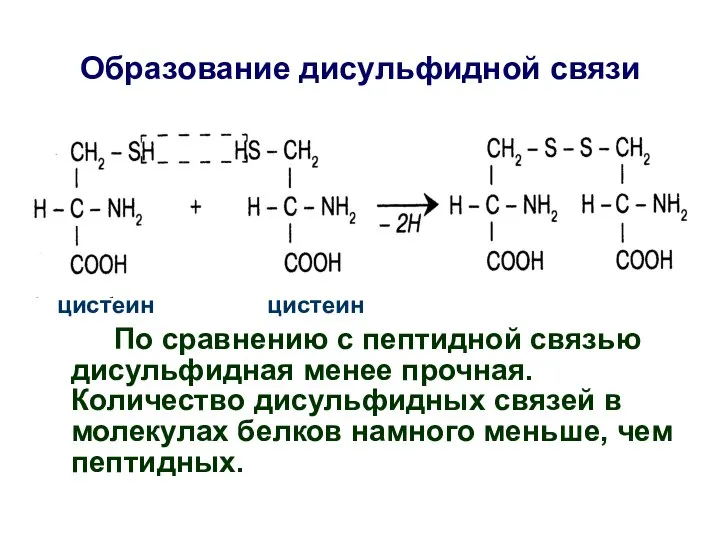
- 36. цистеин цистеин По сравнению с пептидной связью дисульфидная менее прочная. Количество дисульфидных связей в молекулах белков
- 37. Дисульфидные связи в молекуле белка-фермента РНК-азы
- 38. Дисульфидные связи в молекуле инсулина
- 39. Участок молекулы коллагена
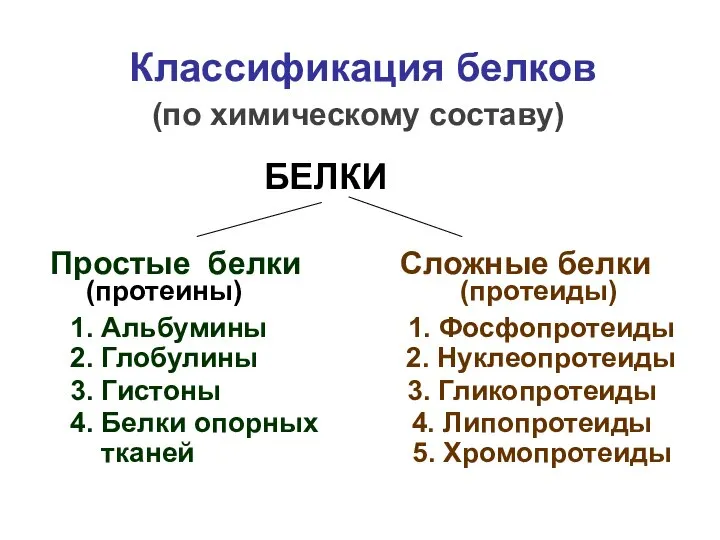
- 40. Классификация белков (по химическому составу) БЕЛКИ Простые белки Сложные белки (протеины) (протеиды) 1. Альбумины 1. Фосфопротеиды
- 41. Классификация белков (по форме молекул) БЕЛКИ Глобулярные Фибриллярные 1. Альбумины 1. Коллаген 2. Глобулины 2. Кератины
- 42. Тест 1 Содержание белков в организме взрослого человека составляет: а) 8-10 % б) 15-17 % в)
- 43. Тест 2 Обязательным химическим элементом, входящим в состав белков, является: а) азот б) кальций в) селен
- 44. Тест 3 Во все белки входят: а) 10 разновидностей аминокислот б) 20 разновидностей аминокислот в) 30
- 45. Тест 4 В состав аминокислот обязательно входят функциональные группы: а) альдегидная и спиртовая б) карбоксильная и
- 46. Тест 5 Главной химической связью в белках является: а) водородная б) дисульфидная в) ионная г) пептидная
- 47. Тест 6 Простые белки отличаются от сложных: а) молекулярной массой б) отсутствием дисульфидных связей в) отсутствием
- 48. Тест 7 Сложные белки отличаются от простых: а) изоэлектрической точкой б) наличием дисульфидных связей в) наличием
- 49. Тест 8 В образовании дисульфидной связи участвует аминокислота: а) аланин б) глицин в) глутамин г) цистеин
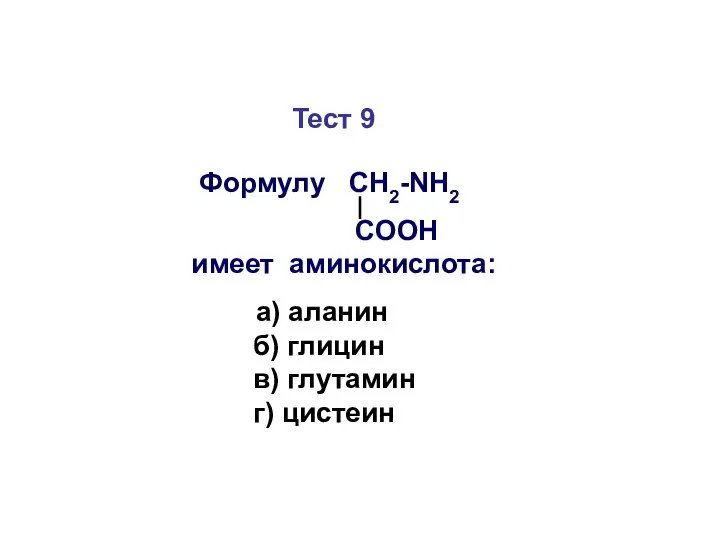
- 50. Тест 9 Формулу СН2-NH2 COOH имеет аминокислота: а) аланин б) глицин в) глутамин г) цистеин
- 52. Скачать презентацию


































 Анемии
Анемии Патофізіологічні особливості раннього неонатального періоду. Перехідні стани новонароджених
Патофізіологічні особливості раннього неонатального періоду. Перехідні стани новонароджених Социальная работа в больнице и хосписе
Социальная работа в больнице и хосписе Иммунопрофилактика и иммунотерапия. Конспект лекции
Иммунопрофилактика и иммунотерапия. Конспект лекции Как стать долгожителем?
Как стать долгожителем? Сыртқы құлақ жолында денені диагностикалау және алып шығару
Сыртқы құлақ жолында денені диагностикалау және алып шығару Сказкотерапия. Лаборатория Другой психологии. Введение в курс
Сказкотерапия. Лаборатория Другой психологии. Введение в курс Анатомо-физиологические особенности периодонта у детей различного возраста
Анатомо-физиологические особенности периодонта у детей различного возраста Энурез. Кіріспе бөлім. Энурез туралы түсінік
Энурез. Кіріспе бөлім. Энурез туралы түсінік Лекция-менингиты
Лекция-менингиты Әйелдердің жүктілік мерзімі
Әйелдердің жүктілік мерзімі Инфекционный процесс. Сепсис. ВИЧ - инфекция
Инфекционный процесс. Сепсис. ВИЧ - инфекция Заболевания перикарда
Заболевания перикарда Внутрішньоутробні інфекції
Внутрішньоутробні інфекції О методе Шичко. Как работать с дневниками. Формулы самовнушения. Часть 2. Урок № 4
О методе Шичко. Как работать с дневниками. Формулы самовнушения. Часть 2. Урок № 4 Гематурия. Классификация
Гематурия. Классификация Тропикалық жемістердің тамақтанудағы маңызы
Тропикалық жемістердің тамақтанудағы маңызы ЛФК при заболеваниях почек у детей
ЛФК при заболеваниях почек у детей Переливание крови
Переливание крови Координаторная система. Мозжечок, синдромы поражения. Экстрапирамидная система, синдромы поражения
Координаторная система. Мозжечок, синдромы поражения. Экстрапирамидная система, синдромы поражения Медико-социальная экспертиза при хронической болезни почек
Медико-социальная экспертиза при хронической болезни почек Характеристики физиологических и психологических особенностей людей с вариациями кариотипов
Характеристики физиологических и психологических особенностей людей с вариациями кариотипов Общий обзор выделительной системы
Общий обзор выделительной системы Различные положения пациента в постели
Различные положения пациента в постели Кровотечения. Первая помощь при кровотечениях
Кровотечения. Первая помощь при кровотечениях Кверцетин – корректор гастротоксического эффекта глюкокортикостероидов
Кверцетин – корректор гастротоксического эффекта глюкокортикостероидов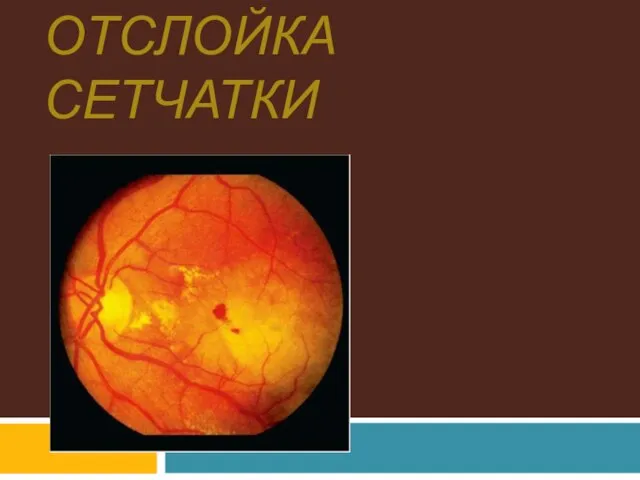 Отслойка сетчатки
Отслойка сетчатки Топографическая анатомия пищевода
Топографическая анатомия пищевода