Materials and methods
This was a randomised, stratified, multicentre, double-blind, double-dummy (i.e.
all patients received both devices, see below), parallel-group, salmeterol-controlled, active-controlled Phase III study of 12 weeks’ duration (GlaxoSmithKline study number: B2C112060; ClinicalTrials.gov number: NCT01181895). It was conducted between 15 September 2010 and 26 August 2011 at 34 centres in 5 countries (Germany, Peru, Poland, Ukraine and USA). The study was approved by local ethics review committees (see Additional file 4), and was conducted in accordance with the Declaration of Helsinki and Good Clinical Practice guidelines.
Әдіс-тәсілі мен материалдар:
Бұл-салыстырмалы
Салметерол бақылау тобымен активті бақылау тобы бақыланатын екі топқа жасырын түрде жүргізілетін зерттеудің үшінші фазасы 12 аптаға созылатын рандомизациялық,көп қабатты,мультицентрлі зерттеу.Ол 2010 жылдың 15 қыркүйегінен бастап 2011 жылдың 26 тамызына дейін 5 елдің 34 орталығында өтті (Германия,Перу Польша,Украина,АҚШ).Зерттеу этикалық экпертиза жөніндегі жергілікті комитетімен мақұлданып, Хельсинк декларациясы принциптарына сәйкес және жақсы клиникалық практикада өткізілді.

















 Ерте токсикоздардың сирек түрлері
Ерте токсикоздардың сирек түрлері Акушериядағы “жедел іш”. Жедел холецистит және жүктілік
Акушериядағы “жедел іш”. Жедел холецистит және жүктілік Изосенсибилизация
Изосенсибилизация Мочекаменная болезнь
Мочекаменная болезнь Иммунный патогенез и иммунный диагноз СПИДа
Иммунный патогенез и иммунный диагноз СПИДа Определение функционального состояния организма с использованием расчетных методов исследования
Определение функционального состояния организма с использованием расчетных методов исследования Характеристики дорожно-транспортных происшествий и катастроф. Медико-социальная значимость дорожно-транспортного травматизма
Характеристики дорожно-транспортных происшествий и катастроф. Медико-социальная значимость дорожно-транспортного травматизма История открытия и изучения антибиотиков как лекарственных средств
История открытия и изучения антибиотиков как лекарственных средств Наши врачи. Клиника Квадромед Лаб
Наши врачи. Клиника Квадромед Лаб Surgical Neonatal Vomiting
Surgical Neonatal Vomiting Паразитизм, патогенность и паразитарные системы
Паразитизм, патогенность и паразитарные системы Врожденная кишечная непроходимость
Врожденная кишечная непроходимость Очаговый туберкулез. Инфильтративный туберкулез. Казеозная пневмония. Туберкулема
Очаговый туберкулез. Инфильтративный туберкулез. Казеозная пневмония. Туберкулема FDA. Управление по санитарному надзору за качеством
FDA. Управление по санитарному надзору за качеством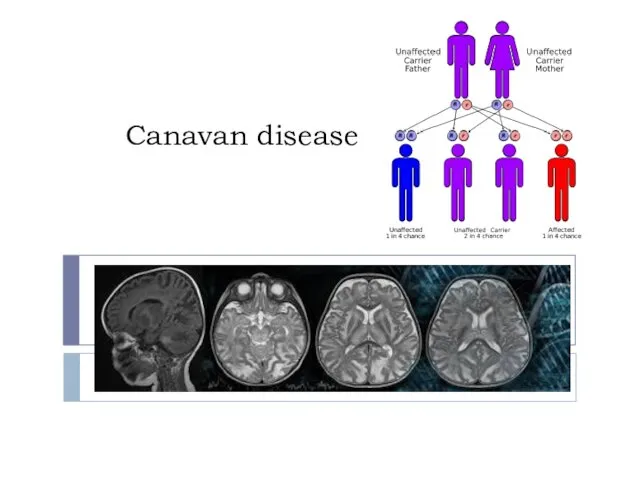 Canavan disease
Canavan disease Продукты крови и их клиническое применение
Продукты крови и их клиническое применение Диагностическая и лечебная интервенционная радиология в онкологии
Диагностическая и лечебная интервенционная радиология в онкологии Черепно-мозговая травма
Черепно-мозговая травма Автоматизация звука [Ш] в игровых упражнениях со Смешариками
Автоматизация звука [Ш] в игровых упражнениях со Смешариками Мiнез - ''charakter'‘ деген грек сөзiнен шыққан
Мiнез - ''charakter'‘ деген грек сөзiнен шыққан Процедура удаления зубных отложений
Процедура удаления зубных отложений Критерии и структура стандартного определения случая инфекционного заболевания
Критерии и структура стандартного определения случая инфекционного заболевания Патоморфологическая характеристика пищевода Баррета
Патоморфологическая характеристика пищевода Баррета Atherosclerosis and its treatment
Atherosclerosis and its treatment Болезни органов дыхания и их предупреждение. Гигиена дыхания
Болезни органов дыхания и их предупреждение. Гигиена дыхания Медицинские осмотры
Медицинские осмотры Общая гигиена и экология человека
Общая гигиена и экология человека Медикаментозное лечение дислипидемий
Медикаментозное лечение дислипидемий