Содержание
- 2. Клиническое исследование (КИ) – это изучение клинических, фармакологических, фармакодинамических свойств исследуемого препарата у человека, включая процессы
- 3. В процессе КИ новых ЛС выделяют 4 взаимосвязанные фазы: Определение безопасности ЛС и установление диапазона переносимых
- 4. Закон Украины «О лекарственных средствах» ОСТ 42-511-99 «Правила проведения качественных клинических исследований в Украине» Приказ Минздрава
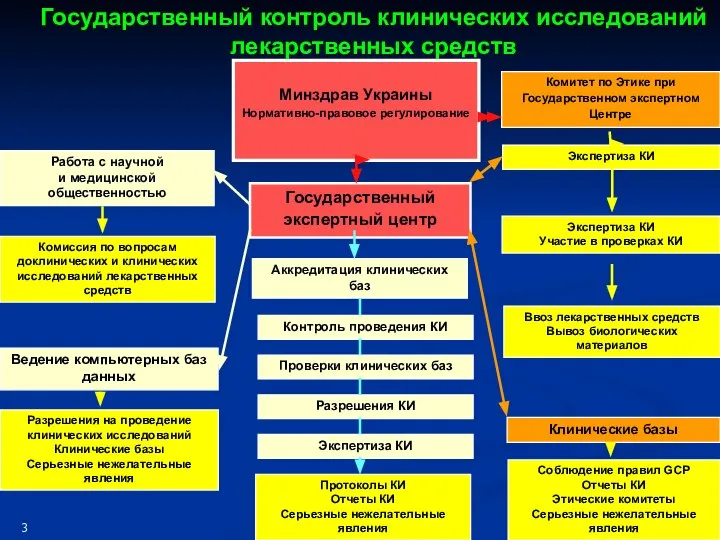
- 5. Минздрав Украины Нормативно-правовое регулирование Экспертиза КИ Аккредитация клинических баз Протоколы КИ Отчеты КИ Серьезные нежелательные явления
- 6. ВИДЫ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ: - открытое, когда все участники испытаний знают, какой препарат получает больной; - простое
- 7. ВИДЫ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ: (продолжение) Биоэквивалентность – основной вид контроля воспроизведенных ЛС, не отличающихся лекарственной формой и
- 8. Объектом изучения КИ являются ЛС как отечественного, так и зарубежного производства, область применения которых затрагивает все
- 9. Одной из тенденций в развитии сектора КИ в Украине следует признать быстрый рост числа КИ на
- 10. КИ проводятся в соответствии с международным стандартом – Good Clinical Practice (GCP) Принципы GCP КИ должны
- 11. Принципы GCP (продолжение) Все привлекаемые к проведению исследования лица должны иметь соответствующее образование, подготовку и опыт
- 12. ЭТИЧЕСКИЙ КОМИТЕТ Основными задачами этического комитета являются: Проведение качественной этической экспертизы материалов КИ ЛС с целью
- 13. Для проведения оценки рисков и ожидаемой пользы ЭК должен убедиться что: Необходимые данные не могут быть
- 14. При получении согласия на биомедицинское исследование, гражданину должна быть предоставлена следующая информация:: о ЛС и сущности
- 15. В случае согласия пациента учавствовать в КИ, он подписывет информационное согласие. Информсогласие (согласие информированного пациента) гарантирует,
- 16. NB!!! ЗАПРЕЩЕНО ПРОВЕДЕНИЕ КИ С УЧАСТИЕМ: Несовершеннолетних, не имеющих родителей; Беременных женщин, за исключением случаев, если
- 17. Допускаются КИ ЛС, предназначенных для лечения психических заболеваний с привлечением лиц с психическими заболеваниями и признанных
- 18. Декларации: Хельсинская декларация: биомедицинские исследования с участием людей должны соответствовать общепринятым научсным принципам и основываться на
- 19. Декларации (продолжение): «Международное руководство по этике биомедицинских исследований с вовлечением человека» (Совет Международных организаций по медицинской
- 20. Декларации (продолжение): «Конвенция о защите прав человека и человеческого достоинства в связи с применением биологии и
- 21. Программа исследования нового лечебного средства на человеке состоит из четырех фаз исследований. Первые три проводятся при
- 22. К началу клинических исследований должна быть представлена следующая информация: описание процесса химического синтеза, включая данные о
- 23. характер, выраженность и продолжительность фармакологического действия; частота и степень тяжести побочных явлений; скорость развития эффектов; поворотность
- 24. На І фазе клинических исследований оцениваются следующие характеристики лечебного средства: переносимость и безопасность, влияние на основные
- 25. метаболизм и взаимодействие, период полувывода лечебного средства. фармакокинетические и фармакодинамические показатели, связь с белками, сравнение форм
- 26. Главной целью ІІ фазы есть доведения клинической эфективности лечебного средства при исследовании определенной группы пациентов, а
- 27. При проведении исследований ІІ фазы необходимо придерживаться следующих условий: наличие контрольной группы, которая существенно не отличается
- 28. На протяжении ІІІ фазы клинических исследований проводят так называемые «мегаиследования» - исследование при участии 10000 пациентов.
- 29. ІV фаза исследований может быть использована для оценки следующих данных: усовершенствование схем дозирования лечебного средства; разнообразных
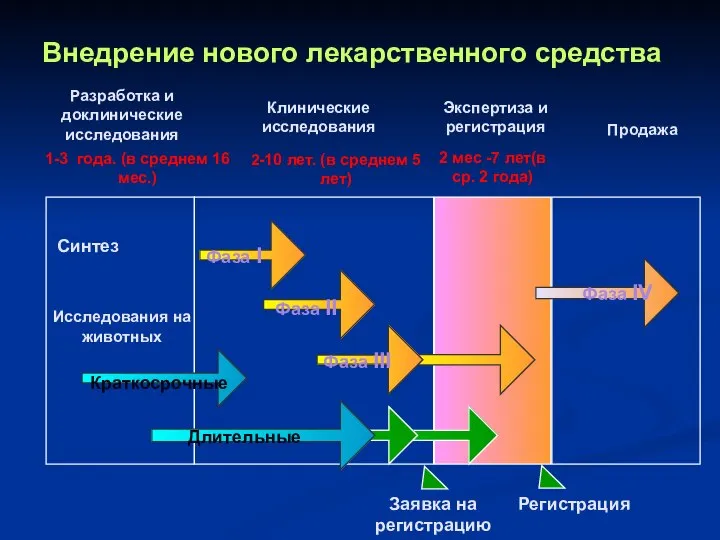
- 30. Разработка и доклинические исследования Клинические исследования Экспертиза и регистрация Продажа Фаза I Фаза II Фаза III
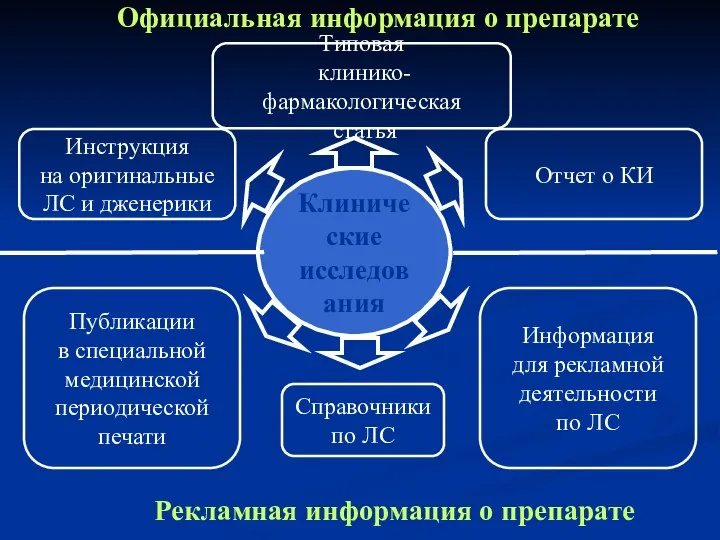
- 31. Клинические исследования Официальная информация о препарате Рекламная информация о препарате Инструкция на оригинальные ЛС и дженерики
- 32. Документы, необходимые для получения разрешения на проведение КИ Заявление Протокол клинического исследования Брошюра исследователя Информация для
- 33. Критерии оценки материалов, представленных для получения разрешения и отчетов о клинических исследований. Соответствие стандарту GCP; Адекватность
- 34. Протокол клинического исследования (типичные ошибки) При составлении протокола КИ: Отсутствует обоснование исследования данного ЛС по данному
- 35. Отчет клинического исследования (типичные ошибки) При представлении отчета КИ: Нечетко описаны исследуемые популяции, что не позволяет
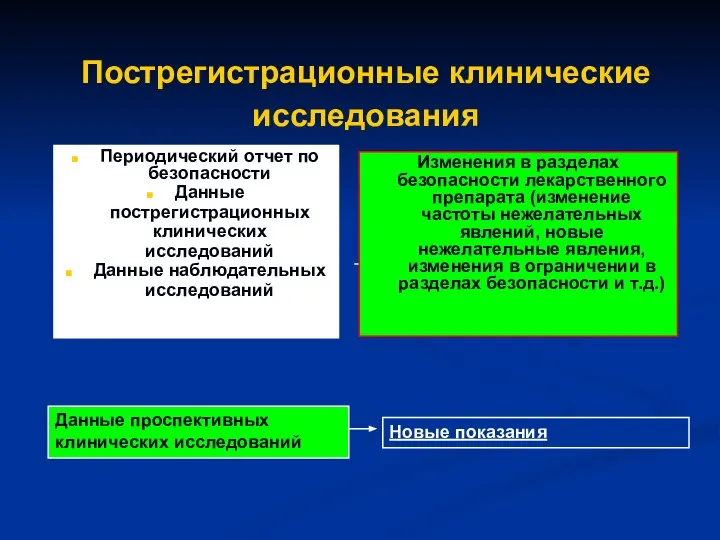
- 36. Пострегистрационные клинические исследования Периодический отчет по безопасности Данные пострегистрационных клинических исследований Данные наблюдательных исследований Изменения в
- 37. Гуманитарные катострофы, связанные с ЛС 1937 – р-р сульфаниламида в диэтиленгликоле 1964 – талидомид 1983 –
- 38. Мониторирование побочных эффектов лекарственных средств Извещения о побочных эффектах Периодически обновляемый отчет по безопасности Государственный экспертный
- 39. «Идеальное» лекарство: Эффективное Безопасное Удобное (для приема) Доступное (по цене)
- 40. Чем мы лечим? Оригинальными лекарствами Генерическими (воспроизведенными) лекарствами
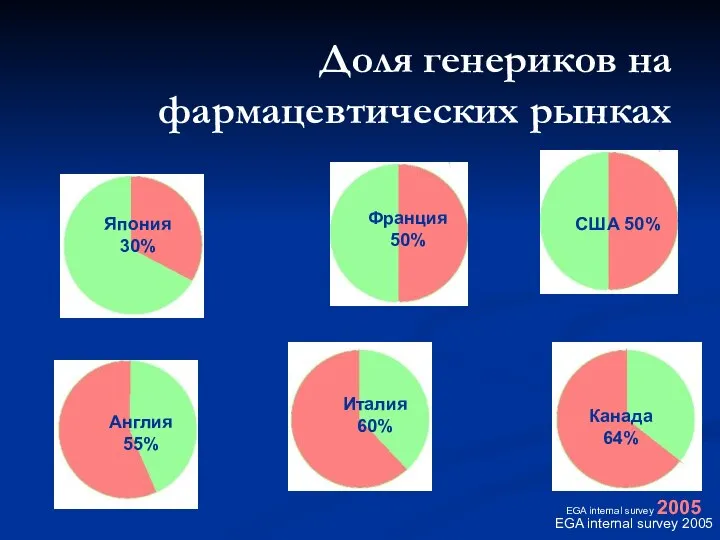
- 41. Доля генериков на фармацевтических рынках EGA internal survey 2005 EGA internal survey 2005 США 50% Франция50%
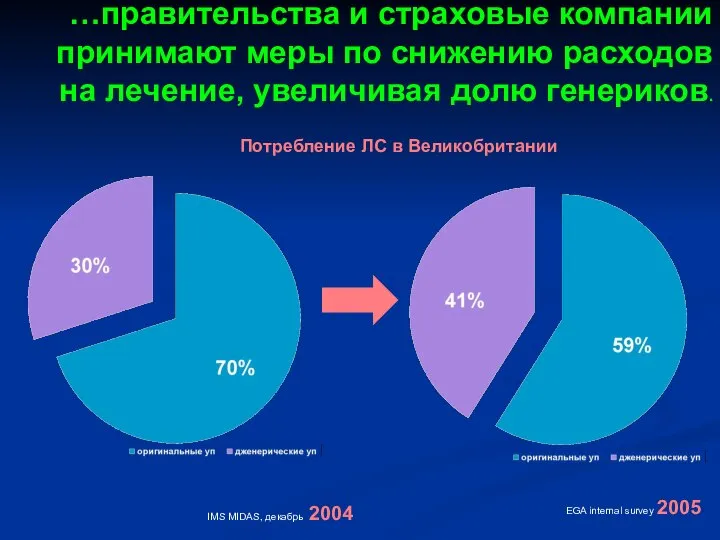
- 42. …правительства и страховые компании принимают меры по снижению расходов на лечение, увеличивая долю генериков. IMS MIDAS,
- 43. А ЧТО У НАС?
- 44. Экспансия генериков: выгоды Снижение затрат на лечение Доступность современных ЛС для большинства пациентов Сдерживание роста цен
- 45. Экспансия генериков: проблемы Большое количество копий оригинального препарата затрудняет оценку качества конкретного генерического препарата
- 46. Крайние суждения в отношении генерических лекарственных средств Генерики, если они зарегистрированы, всегда терапевтически эквивалентны оригинальному препарату
- 47. Принятые доказательства эквивалентности генерических лекарственных средств 1. Сравнение биоэквивалентности. 2. Сравнение терапевтической эквивалентности.
- 48. ЛЕКАРСТВО-ГЕНЕРИК ПОВТОРЯЕТ ЭФФЕКТ ОРИГИНАЛЬНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ЕСЛИ ЕСТЬ ДОКАЗАТЕЛЬСТВА ЕГО ТЕРАПЕВТИЧЕСКОЙ ЭКВИВАЛЕНТНОСТИ
- 49. Всегда ли генерические лекарственные средства так же безопасны, как оригинальные препараты ?
- 50. Когда можно быть уверенным в качестве генерического лекарственного средства Если он производится в соответствии с (Европейским)
- 51. Европейские компании включают информацию о безопасности производимых ими препаратов в регулярно обновляемые отчеты по безопасности (PSUR)
- 52. КОНЦЕПЦИЯ «ПЕРСОНАЛЬНЫХ» ЛЕКАРСТВЕННЫХ СРЕДСТВ- (П-лекарств) ВЫБОР П-ЛЕКАРСТВА ОСНОВАН НА УЧЕТЕ СЛЕДУЮЩИХ КРИТЕРИЕВ: ЭФФЕКТИВНОСТЬ БЕЗОПАСНОСТЬ ПРИЕМЛЕМОСТЬ СТОИМОСТЬ
- 53. КОНЦЕПЦИЯ «ПЕРСОНАЛЬНЫХ» ЛЕКАРСТВЕННЫХ СРЕДСТВ- (П-лекарств) П - лекарства - это лекарственные средства, которые врач на основании
- 54. КРИТЕРИИ ОЦЕНКИ ОБОСНОВАННОСТИ НАЗНАЧЕНИЯ П-ЛЕКАРСТВА КОНКРЕТНОМУ ПАЦИЕНТУ ЭФФЕКТИВНОСТЬ - анализ фармакодинамики, фармакокинетики, системных эффектов П-лекарства БЕЗОПАСНОСТЬ-
- 56. Скачать презентацию














































 Рак желудка
Рак желудка Определение биоэквивалентности ЛП. Международные документы. ЕАЭС и EMA
Определение биоэквивалентности ЛП. Международные документы. ЕАЭС и EMA Мiнез - ''charakter'‘ деген грек сөзiнен шыққан
Мiнез - ''charakter'‘ деген грек сөзiнен шыққан Психиатриялық науқастарды тексеру әдістері
Психиатриялық науқастарды тексеру әдістері Гендерная психология
Гендерная психология 5 и 6 меридианы в рефлексотерапии. Система у-син
5 и 6 меридианы в рефлексотерапии. Система у-син Эмбриональное развитие эндокринной системы. Аномалии развития
Эмбриональное развитие эндокринной системы. Аномалии развития Медицинская карта
Медицинская карта Аллергодиагностика in vitro
Аллергодиагностика in vitro Тұқым қуалайтын отбасылық гепатоздар
Тұқым қуалайтын отбасылық гепатоздар Сколько весит портфель первоклассника?
Сколько весит портфель первоклассника? Лечебный наркоз в терапевтической практике
Лечебный наркоз в терапевтической практике Альвеококкоз печени
Альвеококкоз печени Чему учат компьютерные игры
Чему учат компьютерные игры Эндокринная система: регуляция, нарушения, тесты оценки
Эндокринная система: регуляция, нарушения, тесты оценки Обучение и воспитание детей с комплексными нарушениями развития
Обучение и воспитание детей с комплексными нарушениями развития Инсектная аллергия
Инсектная аллергия Классификация, сбор и удаление отходов в ЛПУ
Классификация, сбор и удаление отходов в ЛПУ Наркомания у подростков
Наркомания у подростков Ферментодиагностика инфаркта миокарда
Ферментодиагностика инфаркта миокарда Аномалии конституции
Аномалии конституции Лейкоз. Этиологиясы
Лейкоз. Этиологиясы Профилактика ОРВИ и гриппа
Профилактика ОРВИ и гриппа Современная упаковка твердых лекарственных форм, виды, проблемы
Современная упаковка твердых лекарственных форм, виды, проблемы Терапиялық стоматологиядағы дәлелді медицина
Терапиялық стоматологиядағы дәлелді медицина Хронический панкреатит
Хронический панкреатит Изосерологическая несовместимость крови матери и плода
Изосерологическая несовместимость крови матери и плода Эталоны ответов и литература по генетике
Эталоны ответов и литература по генетике