Содержание
- 2. Гендік терапия − ақау генді алмастырып немесе қапына келтіріп, толық гендік өнімді экспрессиялайтын және мутантты немесе
- 3. Гендік терапия әдісі бойынша бірінші клиникалық сынақтар 1989 жылы 22 мамырда прогрессияланушы меланома жағыдайында ісік-инфильтрлеуші лимфоциттерді
- 4. Гендік терапияның түрлері Нәрестелердегі генотерапия Терапияның бұл түрінде генетикалық құрылымды зиготаға немесе эмбрионға дамудың ерте сатысында
- 5. Ағзаға терапевтік құрылымды енгізу әдістері In vivo технологиясы (қан арқылы жүйелі енгізу) әзірше практика жүзінде жүзеге
- 6. in situ жағдайындағы гендік терапияға мысалы: Тыныс жолының эпителиіне аденовирустық вектор құрамы арқылы терапевтік генді локальды
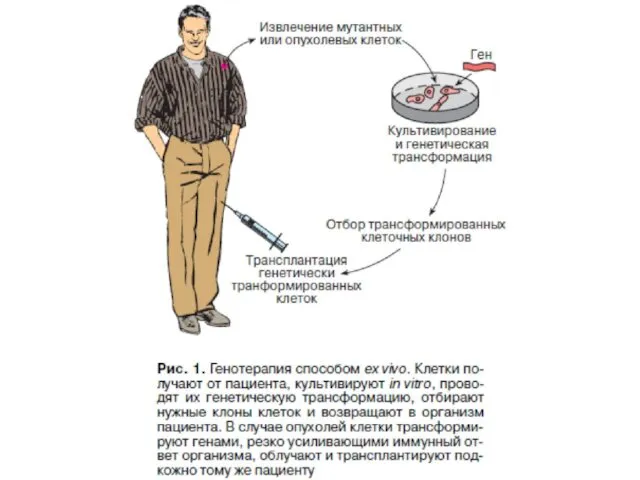
- 8. ex vivo жағдайында стратегия жүзеге асу үшін генетикалық ақпаратты тасымалдау құралы ретінде аутогендік біріншілік жасушалар қолданылуы
- 9. Фибробласт өте жақсы суррогат жасуша ретінде табылған. Олар культурада ұзақ пролиферациялану қабілетіне ие, донорларда іріктеу үшін
- 10. Ағзаның кез келген ұлпасымен жоғары сәйкестігі дін жасушаларының негізгі ерекшелігіне жатады. Яғни енгізілген генетикалық құрылымның ұзақ
- 11. Гендік терапиялық құралдардың емдік әсерінің жетістіктері ПОЗИТИВТІ ГЕНДІК ТЕРАПИЯ Позитивті гендік терапия экспрессиясы жеткіліксіз немесе толықтай
- 12. 1. хромосомалық ДНҚ деңгейінде генді түзету Геннің функциясын оны алмастыру арқылы немесе қосарлану арқылы қалпына келтіру.
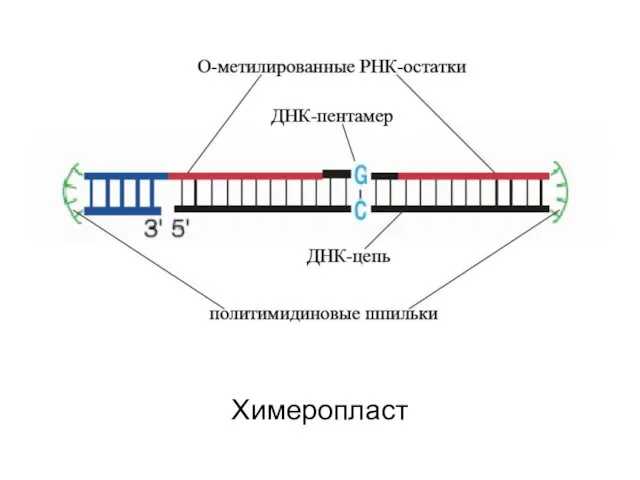
- 13. Химеропласт
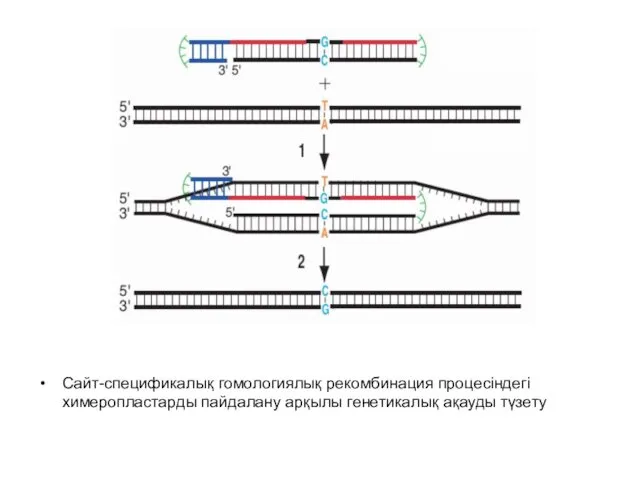
- 14. Сайт-спецификалық гомологиялық рекомбинация процесіндегі химеропластарды пайдалану арқылы генетикалық ақауды түзету
- 15. Химеропластияны жүргізу кезінде туындайтын негізгі мәселелерге жатады: Белгілі бір ақаудың молекулалық-генетикалық сипаты және оны анықтау; Арнайы
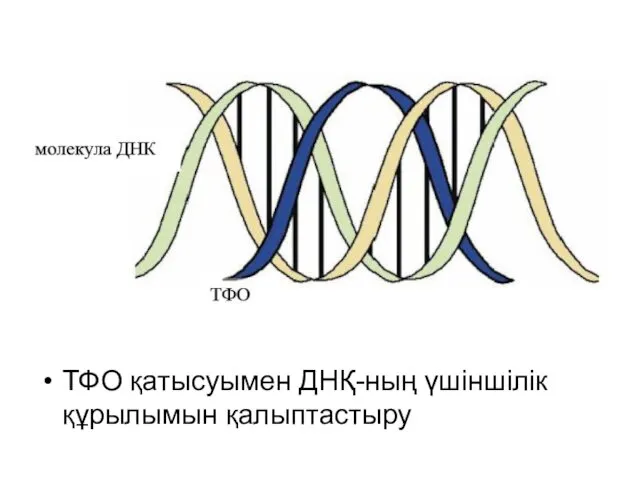
- 16. ТФО қатысуымен ДНҚ-ның үшіншілік құрылымын қалыптастыру
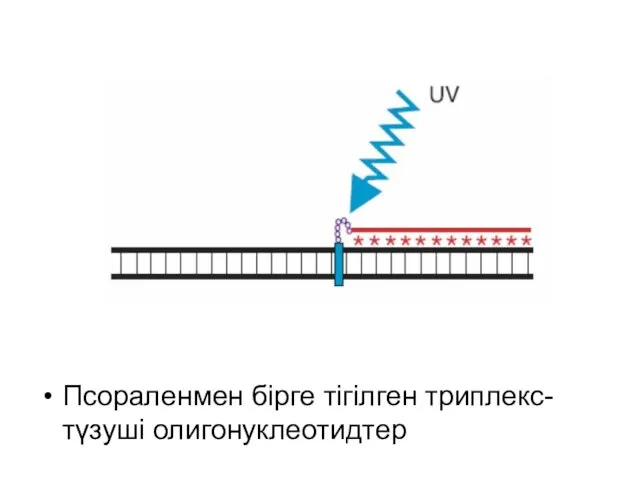
- 17. Псораленмен бірге тігілген триплекс-түзуші олигонуклеотидтер
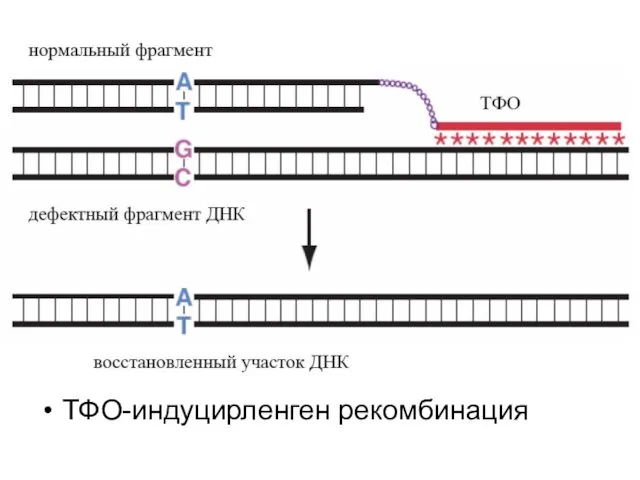
- 18. ТФО-индуцирленген рекомбинация
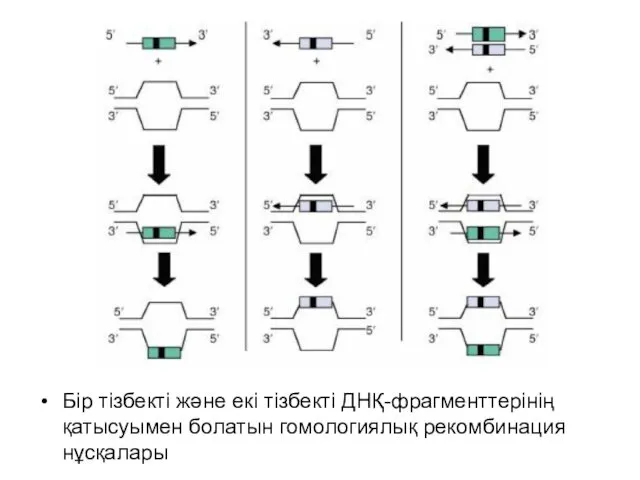
- 19. Бір тізбекті және екі тізбекті ДНҚ-фрагменттерінің қатысуымен болатын гомологиялық рекомбинация нұсқалары
- 20. Енгізілген геннің хромосомадан тыс экспрессиясы Ағза жасушасына хромосоманың арнайы орындарына орналасып, хромосомадан тыс экспрессиялана алатын қалыпты
- 21. Хромосомадан тыс гендік терапияның жасалуына мынандай білімдерді игеру әсерін тигізді: Тұқымқуалайтын, онкологиялық, басқа ауруларға жауапты геннің
- 22. Рекомбинанттық ДНҚ технологиясының кезеңдері: 1. Реттеуші тізбегінен терапиялық генді бөліп алу. Қазіргі таңда бұл кезең полимеразалық
- 23. Трансфекция мыналарды қолдану арқылы жүруі мүмкін: таза («жалаңаш» - ағылш. naked) ДНҚ-ны; Сәйкес плазмидаға салынған ДНҚ
- 24. Геннің векторлық тасымалы Соматикалық генотерапия тәжірибелері кезінде көбінесе вирустық векторлар қолданылады. Ретровирустық вектор. Ретровирустар (сем. Retroviridae)
- 25. Ретровирустың провирусының құрылымдық ұйымы 5’-LTR – транскрипцияның реттеуші сигналын алып жүретін ұзын соңғы қайталау; 3’-LTR –
- 26. Вектор құрастыруға арналған ДНҚ ретровирусының модификациясы y+ - қаптаушы сигнал; Neo - селективті маркер; Р –Neo
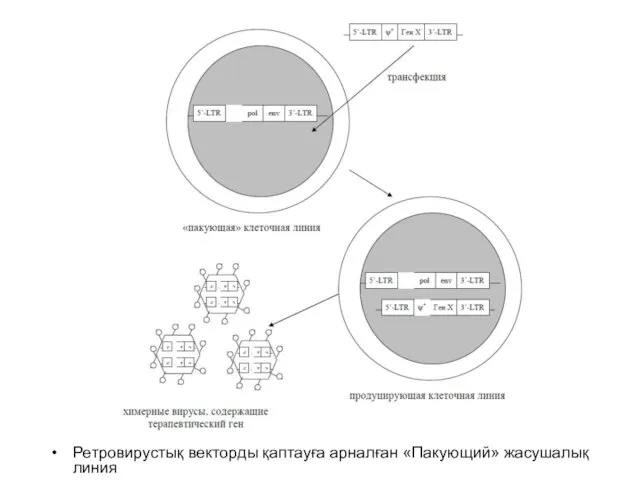
- 27. Ретровирустық векторды қаптауға арналған «Пакующий» жасушалық линия
- 28. Аденовирустық векторлар. Аденовирустар (сем. Adenoviridae, род Mastadenovirus) − кең тараған ДНҚ-сы бар вирустар, клиникалық көріністің полиморфизмімен
- 29. Аденовирус геномының құрылыдық ұйымы Е1 – трансформацияға арналған критикалық аймақ; Е1А – транскрипцияны реттеуші; Е1В –
- 30. Вирустық емес векторлар. Тасымалдаудың вирустық емес жүйесін құрастыру үшін мобильдік элементтердің тізбектері-транспозондар қолданылуы мүмкін. Бұл мақсат
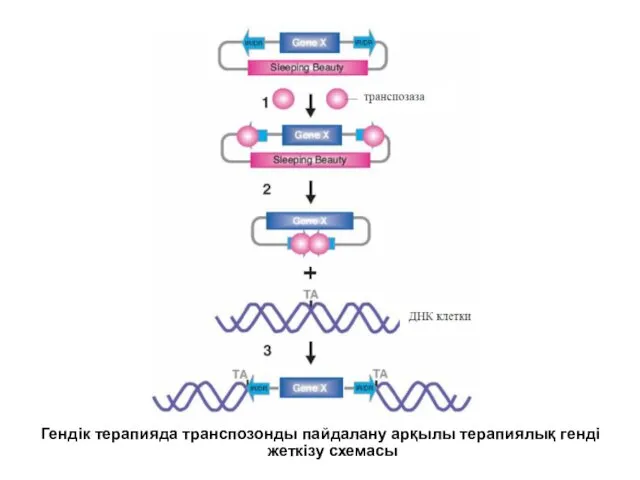
- 31. Гендік терапияда транспозонды пайдалану арқылы терапиялық генді жеткізу схемасы
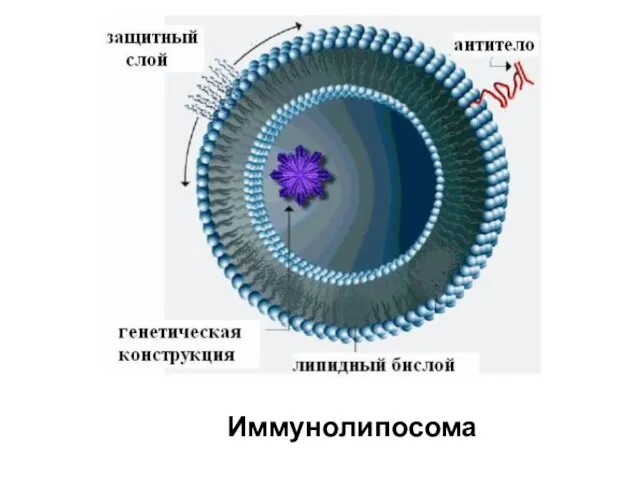
- 32. Липосомалардың көмегімен генді тасымалдау Липосомалар – бір немесе бірнеше биқабатты мембранадан түзілген микроскопиялық фосфолипидтік везикулалар, олар
- 33. Липосомаларға келесілей қасиеттер тән: Биосәйкестік; Қосылған заттарды қорғау; Гидрофобтық және гидрофильдік қосылыстарды тасымалдау мүмкіндігі; Нысана-жасушаның цитоплазмасына
- 34. Иммунолипосома
- 35. ДНҚ құрылымды нысана жасушаға трансфекцияның физикалық әдістерінің көмегімен, мысалы электротрансфекцияның көмегімен тура енгізу. Бұл әдіс электропорациямен
- 36. Ұлпаға генетикалық терапиялық құрылымдарды енгізудің басқа физикалық әдісі − «гендік пушканы» қолдану арқылы жүретін трансформацияның баллистикалық
- 37. НЕГАТИВТІ ГЕНОТЕРАПИЯ Инфекция немесе ісіктік трансформация кезінде ауру көбіне қалыпты жасушаға тән емес геннің артық қызметінің
- 38. мРНҚ деңгейінде ген қызметін басып тастау Антисенс РНҚ терапия. мРНҚ деңгейінде геннің жұмысын басып тастайтын құрылымды
- 39. Антимағыналы РНҚ арқылы терапия 1978 жылы 13 қалдықтан тұратын Раус саркомасы вирусының матрицалық РНҚ-сына комплементарлы олигонуклеотид
- 40. Рибозимді пайдалану арқылы жүретін гендік терапия мРНҚ деңгейінде ген экспрессиясын басып тастаудың тағы бір әдісі болып
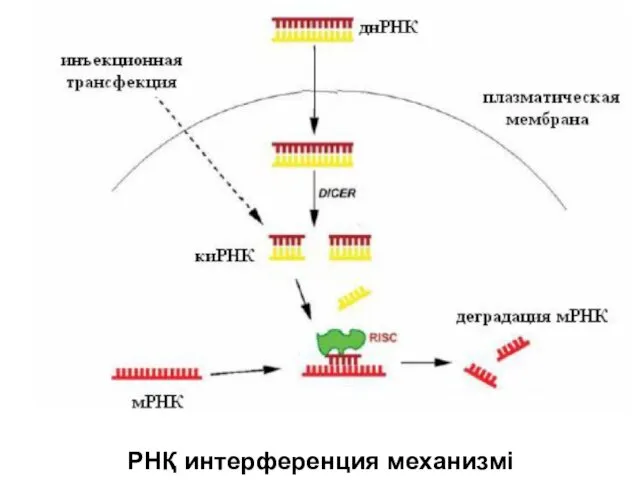
- 41. қтРНҚ-ның гендік терапиясы мРНҚ деңгейінде негативті генотерапияның басқа әдісі геномға келетін қауіптен және вирустардан қорғау механизмі
- 42. қтРНҚ-ныңИсточником днРНК могут быть: Геномы қтРНҚ түріндегі вирустар; Геномы бір тізбекті РНҚ түріндегі вирустар, бір тізбекті
- 43. РНҚ интерференция механизмі
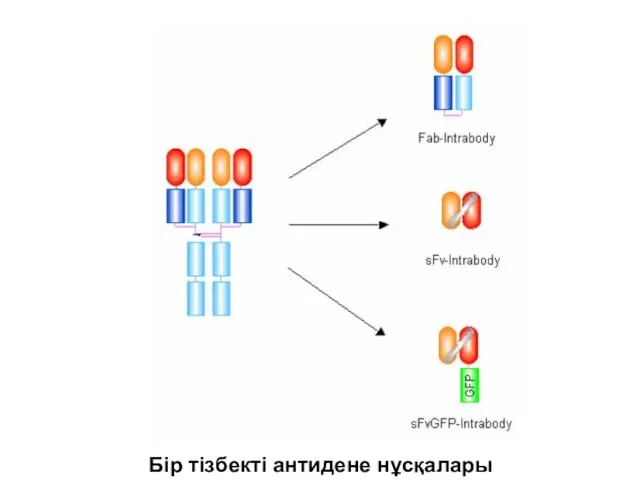
- 44. Белок деңгейінде ген функциясын басып тастау Жасушаішілік иммундау. Белок деңгейінде ген функциясын басып тастаудың бір әдісі.
- 45. Бір тізбекті антидене нұсқалары
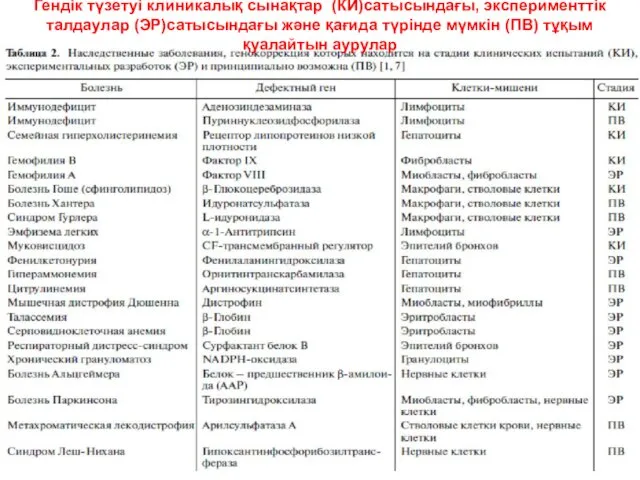
- 46. Гендік түзетуі клиникалық сынақтар (КИ)сатысындағы, эксперименттік талдаулар (ЭР)сатысындағы және қағида түрінде мүмкін (ПВ) тұқым қуалайтын аурулар
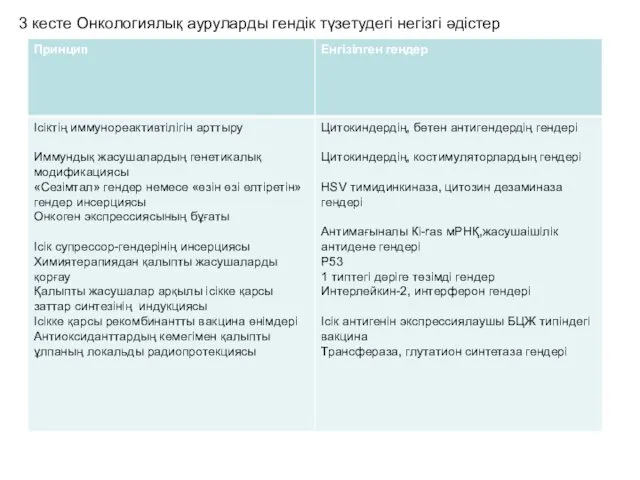
- 47. 3 кесте Онкологиялық ауруларды гендік түзетудегі негізгі әдістер
- 52. Скачать презентацию































 Синдром анемии в обще-врачебной практике
Синдром анемии в обще-врачебной практике ДЕГЕНЕРАТИВНАЯ БОЛЕЗНЬ ПОЗВОНОЧНИКА(ОСТЕОХОНДРОЗ)
ДЕГЕНЕРАТИВНАЯ БОЛЕЗНЬ ПОЗВОНОЧНИКА(ОСТЕОХОНДРОЗ)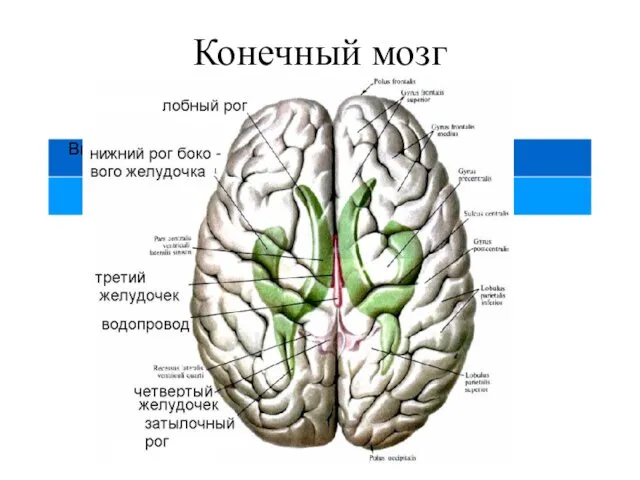 Конечный мозг
Конечный мозг Оценка и ведение тягостных симптомов у паллиативных пациентов
Оценка и ведение тягостных симптомов у паллиативных пациентов Клинико-иммунологические особенности пациентов с хроническим генерализованным пародонтитом
Клинико-иммунологические особенности пациентов с хроническим генерализованным пародонтитом Основные экзистенциалы: пространственность, темпоральность, телеснгсть, настроенность
Основные экзистенциалы: пространственность, темпоральность, телеснгсть, настроенность Инфекционный мононуклеоз у детей и его последствия
Инфекционный мононуклеоз у детей и его последствия Лечебное питание
Лечебное питание Личная гигиена пациента
Личная гигиена пациента Бульозні дерматози
Бульозні дерматози Современные направления комплексного ухода за пациентом с впервые выявленным сахарным диабетом
Современные направления комплексного ухода за пациентом с впервые выявленным сахарным диабетом Методы медицинской визуализации
Методы медицинской визуализации Механизмы восстановления функций
Механизмы восстановления функций Деменции. Болезнь Альцгеймера
Деменции. Болезнь Альцгеймера Основы оказания первой помощи
Основы оказания первой помощи Надлежащая аптечная практика лекарственных средств для медицинского применения
Надлежащая аптечная практика лекарственных средств для медицинского применения Повреждения таза и тазовых органов
Повреждения таза и тазовых органов Проблемы евгеники. Общие этические принципы в медицинской генетике
Проблемы евгеники. Общие этические принципы в медицинской генетике Отцы и дочери. Как найти взаимопонимание. Часть 2. После 10
Отцы и дочери. Как найти взаимопонимание. Часть 2. После 10 Лечебная физкультура при хронических воспалительных заболеваниях кишечника
Лечебная физкультура при хронических воспалительных заболеваниях кишечника Gonorrhoea. Nongonorrhoeal urethritis
Gonorrhoea. Nongonorrhoeal urethritis Основы сосудистой хирургии. Сосудистый шов
Основы сосудистой хирургии. Сосудистый шов Пороки развития мочеполовой системы
Пороки развития мочеполовой системы Острые нарушения мозгового кровообращения
Острые нарушения мозгового кровообращения Полиомиелит в постсертификационный период. Клиника, диагностика, профилактика
Полиомиелит в постсертификационный период. Клиника, диагностика, профилактика Технология изготовления керамических и металлокерамических коронок
Технология изготовления керамических и металлокерамических коронок Функціональна анатомія серця
Функціональна анатомія серця Туберкулез у детей и подростков. Эпидемиология, выявление, профилактика
Туберкулез у детей и подростков. Эпидемиология, выявление, профилактика