Содержание
- 2. ПЛАНЬ Биоэквивалентность Различают следующие виды эквивалентности лекарственных средств: Методология биоаналитической части исследования Какие параметры изучаются при
- 3. Биоэквивалентность -(фармакокинетическая эквивалентность) — степень подобия фармацевтически эквивалентного лекарственного средства по отношению к референтному препарату (обычно
- 4. Исследования биоэквивалентности В последнее время на фармацевтическом рынке России значительно возрос интерес к дженерикам, что обусловлено
- 5. Оценка биоэквивалентности Биоэквивалентность устанавливается сертифицированными фармакологическими центрами в исследованиях с участием здоровых добровольцев. Использование данных по
- 6. Дженерик должен быть эквивалентен оригиналу по своим фармацевтическим, фармакокинетическим и фармакодинамическим свойствам, что служит доказательной базой
- 7. Различают следующие виды эквивалентности лекарственных средств: фармацевтическая, фармакокинетическая, терапевтическая. Терапевтическая эквивалентность означает аналогичные оригинальному препарату эффективность
- 8. Методология биоаналитической части исследования Биоаналитическая часть исследований биоэквивалентности должна осуществляться в соответствии с принципамин адлежащей лабораторной
- 9. Основными характеристиками биоаналитической методики для обеспечения приемлемости и достоверности полученных аналитических данных являются селективность, нижний предел
- 10. Контроль за проведением исследований биоэквивалентности лекарств. При проведении исследований по биоэквивалентности допускается проведение инспектирования данных исследований.
- 12. Скачать презентацию









 Сальмонеллезный сепсис. Клинический случай
Сальмонеллезный сепсис. Клинический случай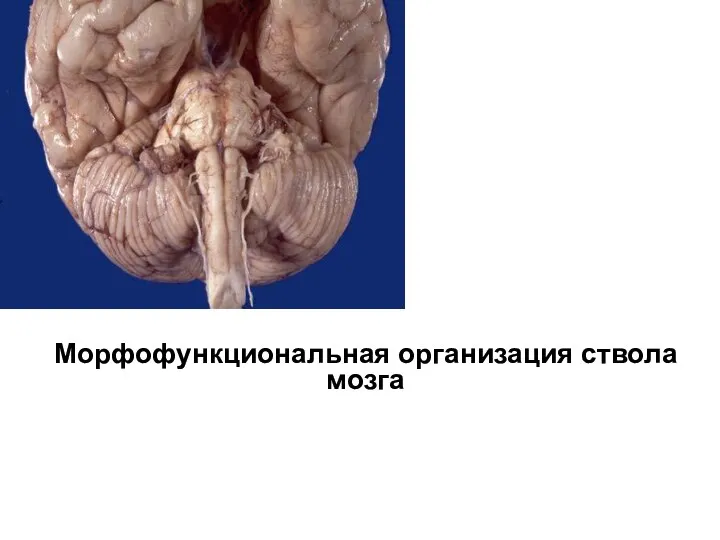 Морфофункциональная организация ствола мозга
Морфофункциональная организация ствола мозга ОРВИ
ОРВИ Действующие химические вещества в лекарственных растениях
Действующие химические вещества в лекарственных растениях Младенчество. Развитие от 0 до года
Младенчество. Развитие от 0 до года Многопрофильная клиника. Направления деятельности
Многопрофильная клиника. Направления деятельности Организация амбулаторно – поликлинической помощи населению в РК
Организация амбулаторно – поликлинической помощи населению в РК Патология эндокринной системы
Патология эндокринной системы Обеспечения безопасности пищевой продукции
Обеспечения безопасности пищевой продукции Агрессия детей: ее причины и предупреждение
Агрессия детей: ее причины и предупреждение Интерпретация гравидограмм
Интерпретация гравидограмм Массаж для подтяжки лица и активации лимфы
Массаж для подтяжки лица и активации лимфы Телемедицина
Телемедицина Контрацепция: защита женского здоровья и не только
Контрацепция: защита женского здоровья и не только Cахарный диабет и беременность
Cахарный диабет и беременность Питание детей дошкольного возраста
Питание детей дошкольного возраста Психобелсенді заттарды қабылдаумен байланысты экономикалық, әлеуметтік, ар-ождандық зардаптары
Психобелсенді заттарды қабылдаумен байланысты экономикалық, әлеуметтік, ар-ождандық зардаптары Оперативное лечение грыж
Оперативное лечение грыж Беременность и эпилепсия
Беременность и эпилепсия қызбааа.pptx
қызбааа.pptx Некроз. Смерть, признаки смерти. Посмертные изменения
Некроз. Смерть, признаки смерти. Посмертные изменения Лекция 2 диагностика, классификация
Лекция 2 диагностика, классификация Жедел гастрит
Жедел гастрит Профилактика синдрома эмоционального выгорания замещающих родителей
Профилактика синдрома эмоционального выгорания замещающих родителей Значение двигательной активности и физической культуры для здоровья человека
Значение двигательной активности и физической культуры для здоровья человека Причины возникновения заболеваний кожи
Причины возникновения заболеваний кожи Косыночные повязки
Косыночные повязки Семіотика уражень органів дихання у дітей. ГРЗ, бронхіти, пневмонії, плеврити. (Лекция 8)
Семіотика уражень органів дихання у дітей. ГРЗ, бронхіти, пневмонії, плеврити. (Лекция 8)