Содержание
- 2. Фармакодинамика — это изучение действия медицинского препарата на организм; ученые задают такие вопросы, как: Какое влияние
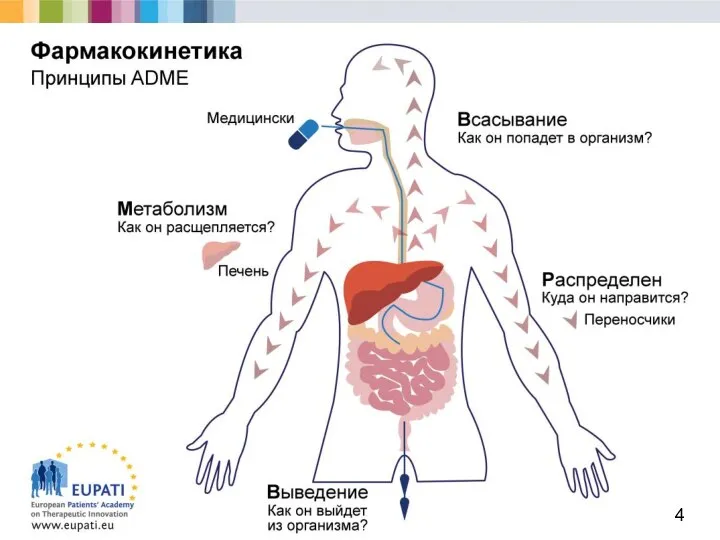
- 3. Фармакокинетика — это изучение действия организма на медицинский препарат; ученые задают такие вопросы, как: Как медицинский
- 5. Представляет собой сбор фармакокинетических данных для животных. Описывает систематическое воздействие на организм животных, а также влияние
- 6. Разработка активных веществ требует понимания процессов контроля всасывания. Всасыванием называют процесс поступления медицинских препаратов в кровоток.
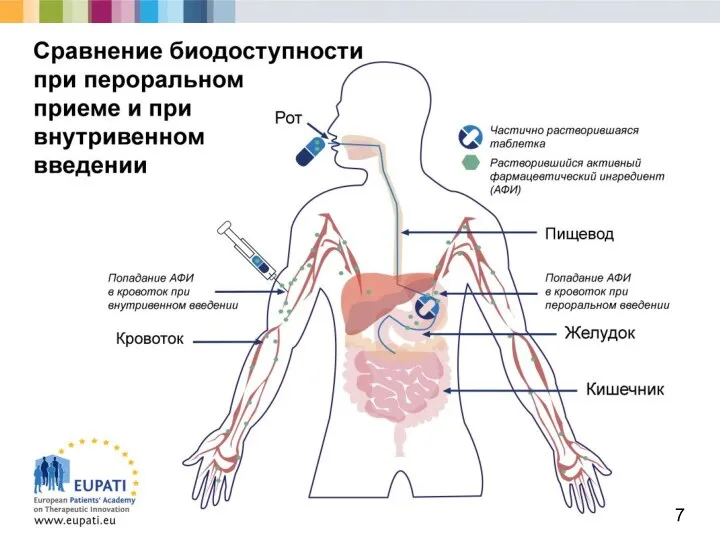
- 8. Препараты попадают в организм различными способами, после чего происходит их всасывание по мере продвижения препарата от
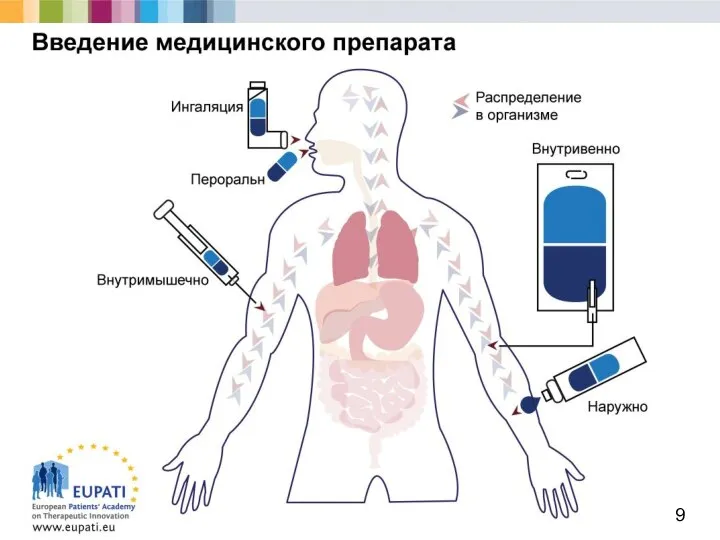
- 10. Наиболее распространенные способы введения медицинских препаратов: пероральный (проглатывание таблетки); внутримышечный (инъекция в мышцу, например руки); подкожно
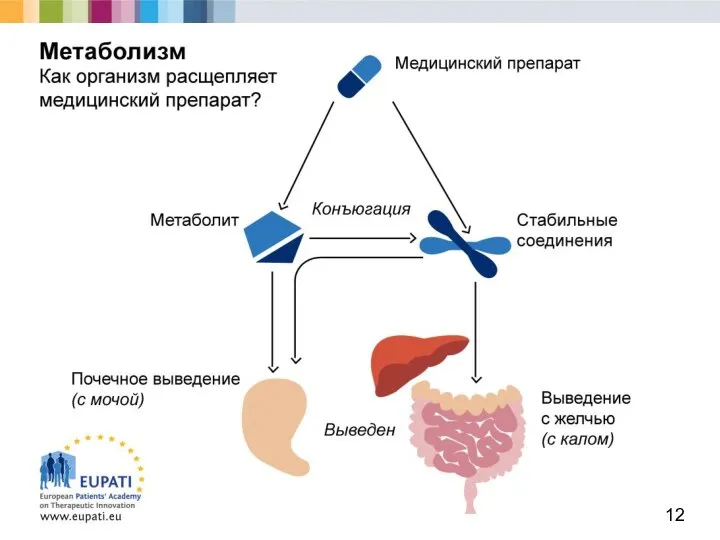
- 11. Большинство медицинских препаратов химически активны и в организме подвергаются метаболизму. Это имеет целый ряд последствий, таких
- 13. Медицинские препараты и метаболиты выводятся из организма различными путями. К ним относятся (по мере убывания важности):
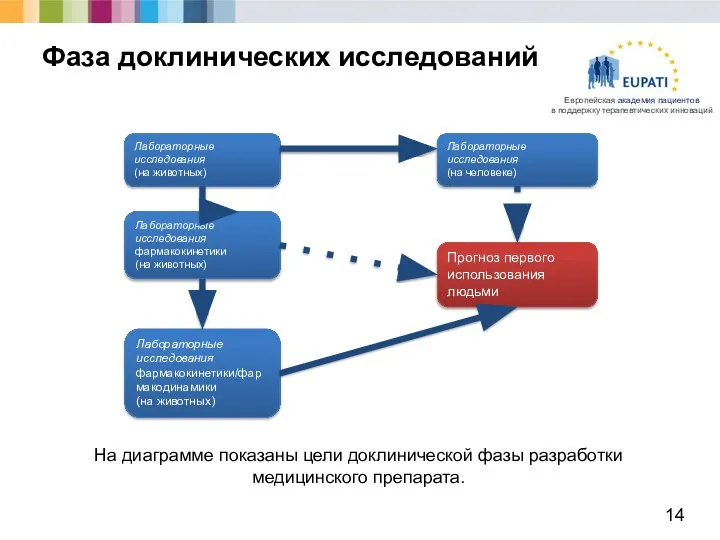
- 14. Фаза доклинических исследований На диаграмме показаны цели доклинической фазы разработки медицинского препарата.
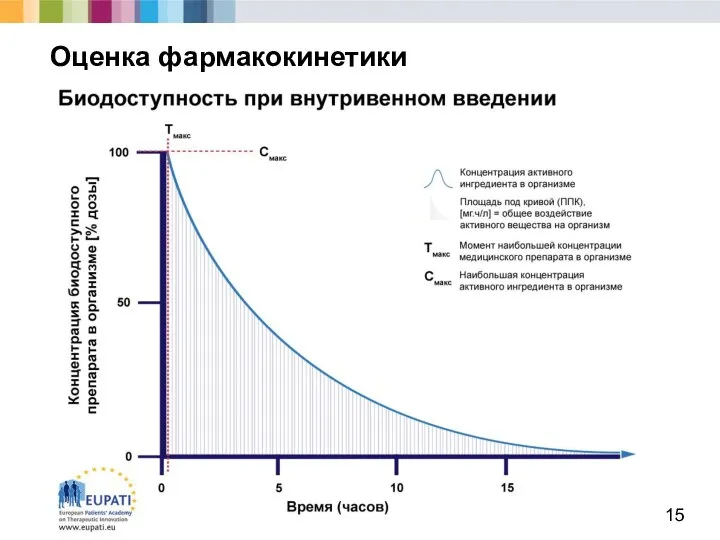
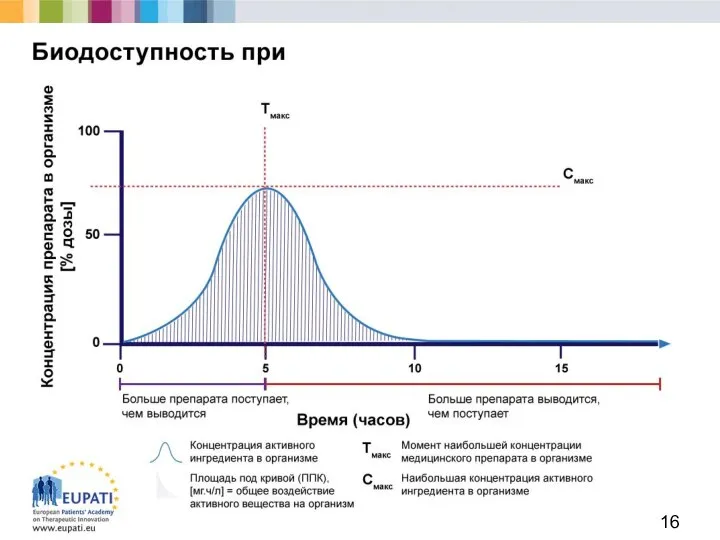
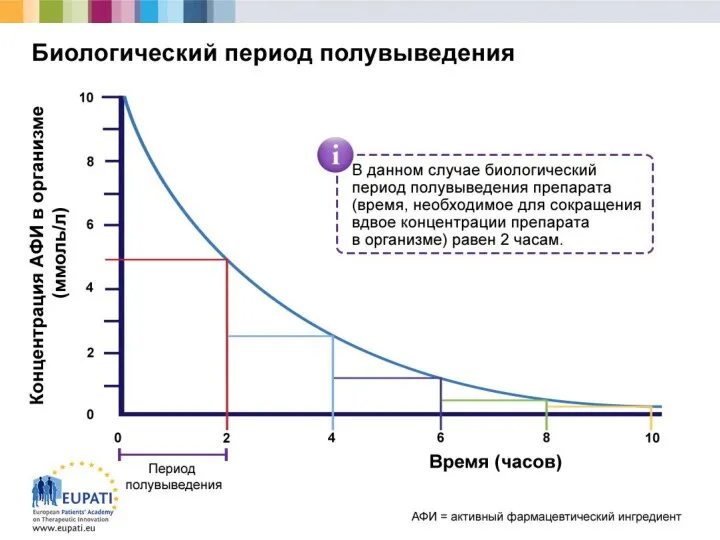
- 15. Оценка фармакокинетики
- 18. Рабочий вариант вещества — это еще не медицинский препарат. Как правило, он представляет собой наиболее сильнодействующий
- 19. Определение безопасной начальной дозы для «первых исследований на людях» должно основываться на данных, полученных в рамках
- 21. Guideline on Strategies to Identify and Mitigate Risks in First-in-Human Clinical Trials with investigational Medicinal Products
- 23. Скачать презентацию











 Селитебная территория
Селитебная территория 20131223_prez.urok23._oktyabr
20131223_prez.urok23._oktyabr Gorillas CCG ВТБ ВЕКТОР
Gorillas CCG ВТБ ВЕКТОР Шиверское, организация деятельности
Шиверское, организация деятельности Рахит
Рахит Игра викторина По страницам Великой Отечественной войны
Игра викторина По страницам Великой Отечественной войны Установление контакта
Установление контакта Портфолио Жумабаева Мукатжана
Портфолио Жумабаева Мукатжана Знаю всё о своём городе
Знаю всё о своём городе Проведение совещания перед началом бурения секции Pre-Section meeting
Проведение совещания перед началом бурения секции Pre-Section meeting Морфофизиологическая характеристика. Нервная система
Морфофизиологическая характеристика. Нервная система Мен топ жетекшісімін
Мен топ жетекшісімін Луковичная диаграмма
Луковичная диаграмма ° Game
° Game 20170512_ushinskiy
20170512_ushinskiy К.Г. Паустовский Растрёпанный воробей
К.Г. Паустовский Растрёпанный воробей Avgust_2022_Sobranie (1)
Avgust_2022_Sobranie (1) Основы проектирования и строительства железных дорог
Основы проектирования и строительства железных дорог blank-dice-template
blank-dice-template Технология обработки наружных фасонных поверхностей деталей из древесины
Технология обработки наружных фасонных поверхностей деталей из древесины Разработать конструкцию пульта управления тренажёра для единоборцев
Разработать конструкцию пульта управления тренажёра для единоборцев 10 заблуждений относительно цены (выбрать любые 5 и аргументированно согласиться или опровергнуть)
10 заблуждений относительно цены (выбрать любые 5 и аргументированно согласиться или опровергнуть) Разработка конструкции циклоидного редуктора с передаточным отношением 24
Разработка конструкции циклоидного редуктора с передаточным отношением 24 Фотоальбом. Мир не прост
Фотоальбом. Мир не прост Проект Радость приносим всем
Проект Радость приносим всем Фазовые проницаемости. Определение фазовых проницаемостей
Фазовые проницаемости. Определение фазовых проницаемостей Как разрушаются камни
Как разрушаются камни Уважаемые читатели
Уважаемые читатели