Содержание
- 2. ПЛАН: Физиологическое значение мышц. Физиологические свойства мышц. Понятие о моторной единице. Виды и режимы сокращения скелетных
- 3. В ОРГАНИЗМЕ ЧЕЛОВЕКА ИМЕЮТСЯ 3 ТИПА МЫШЦ: Скелетные – обеспечивают перемещение тела в пространстве, поддержание позы
- 4. Физиологическое значение мышц – обеспечивают перемещение тела в пространстве, взаимодействие организма с окружающей средой, работу внутренних
- 5. В зависимости от задействованной в сокращении мышечной массы выделяют: 1) локальные нагрузки – 1/3 массы; 2)
- 6. НЕЙРОМОТОРНАЯ ЕДИНИЦА – совокупность мышечных волокон, иннервируемых одним и тем же мотонейроном. По характеру возбуждения, возникающего
- 7. ФАЗНЫЕ НЕЙРОМОТОРНЫЕ ЕДИНИЦЫ ДЕЛЯТ НА: Быстрые – продолжительность потенциала действия в 2 раза меньше, волна сокращения
- 8. В состав скелетных мышц входят мышечные волокна, относящиеся к фазным и тоническим нейромоторным единицам. Попеременное их
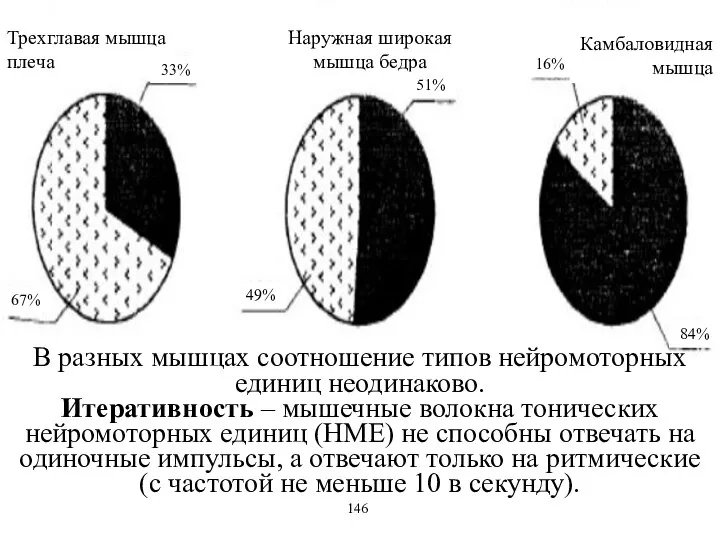
- 9. В разных мышцах соотношение типов нейромоторных единиц неодинаково. Итеративность – мышечные волокна тонических нейромоторных единиц (НМЕ)
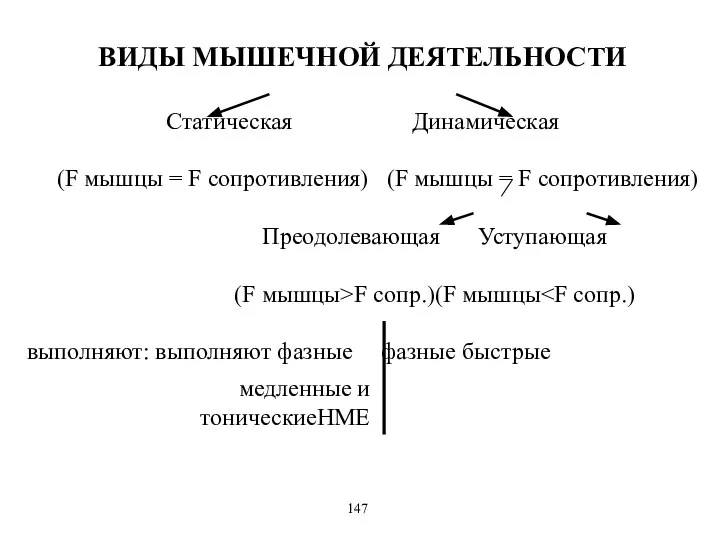
- 10. ВИДЫ МЫШЕЧНОЙ ДЕЯТЕЛЬНОСТИ Статическая Динамическая (F мышцы = F сопротивления) (F мышцы = F сопротивления) Преодолевающая
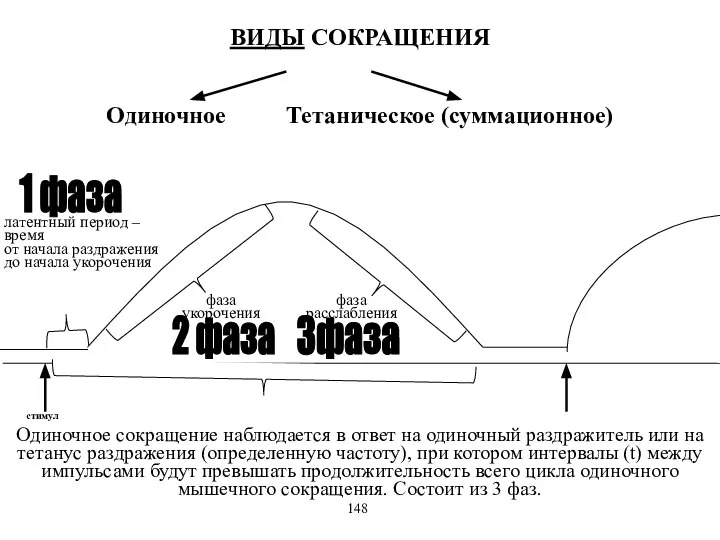
- 11. ВИДЫ СОКРАЩЕНИЯ Одиночное Тетаническое (суммационное) латентный период – время от начала раздражения до начала укорочения фаза
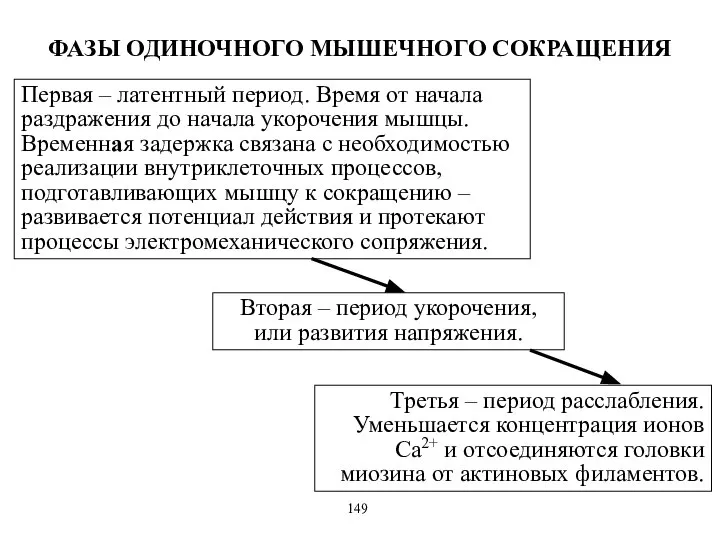
- 12. ФАЗЫ ОДИНОЧНОГО МЫШЕЧНОГО СОКРАЩЕНИЯ Первая – латентный период. Время от начала раздражения до начала укорочения мышцы.
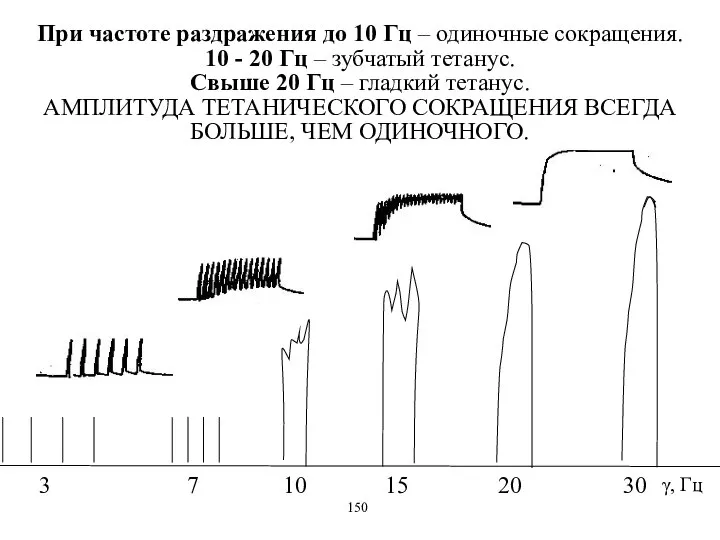
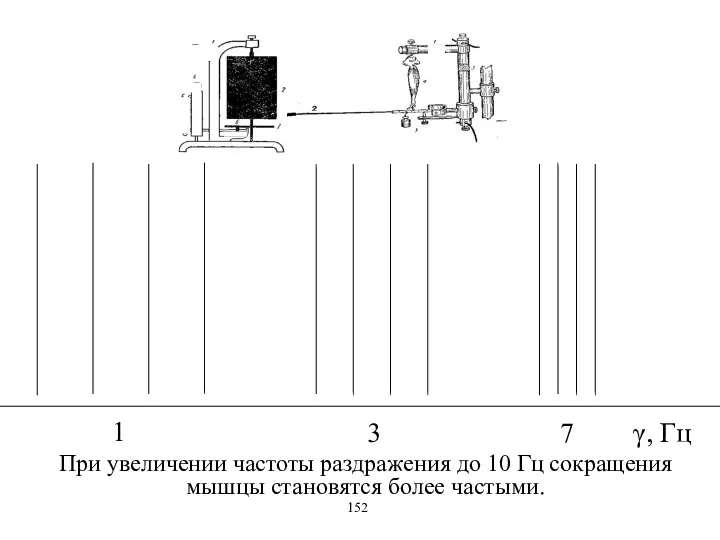
- 13. При частоте раздражения до 10 Гц – одиночные сокращения. 10 - 20 Гц – зубчатый тетанус.
- 14. Ответ: время между импульсами (t) должно быть > 0,1 сек, значит, частота должна быть Задача: продолжительность
- 15. γ, Гц 3 При увеличении частоты раздражения до 10 Гц сокращения мышцы становятся более частыми. 152
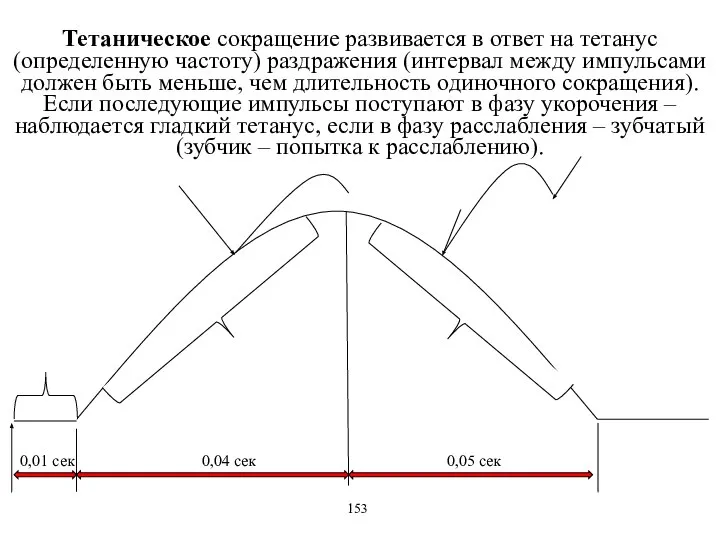
- 16. Тетаническое сокращение развивается в ответ на тетанус (определенную частоту) раздражения (интервал между импульсами должен быть меньше,
- 17. Ответ: для получения зубчатого тетануса t между импульсами должно быть > 0,05 (0,01+0,04) сек, но 10
- 18. РЕЖИМЫ СОКРАЩЕНИЯ СКЕЛЕТНЫХ МЫШЦ 1. Изометрический (эксцентрический) – наблюдается при закреплении мышцы с двух сторон. Размеры
- 19. В организме человека в изолированном виде изотонического или изометрического сокращения не происходит. 156
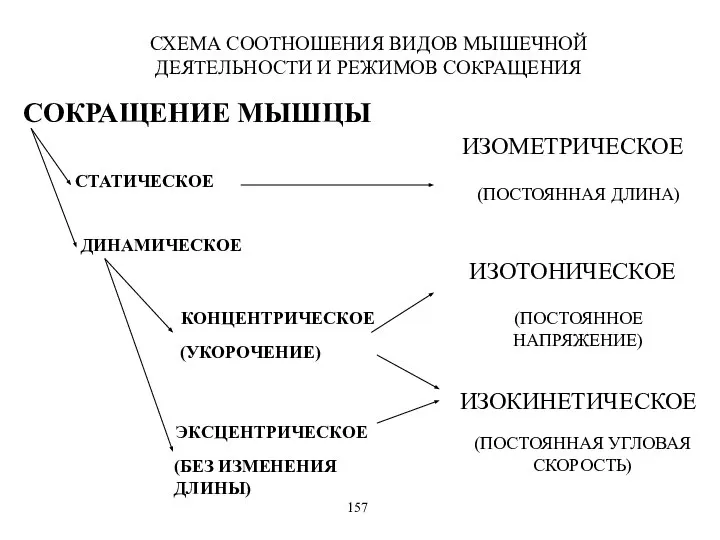
- 20. СХЕМА СООТНОШЕНИЯ ВИДОВ МЫШЕЧНОЙ ДЕЯТЕЛЬНОСТИ И РЕЖИМОВ СОКРАЩЕНИЯ СОКРАЩЕНИЕ МЫШЦЫ СТАТИЧЕСКОЕ ДИНАМИЧЕСКОЕ КОНЦЕНТРИЧЕСКОЕ ЭКСЦЕНТРИЧЕСКОЕ (УКОРОЧЕНИЕ) (БЕЗ
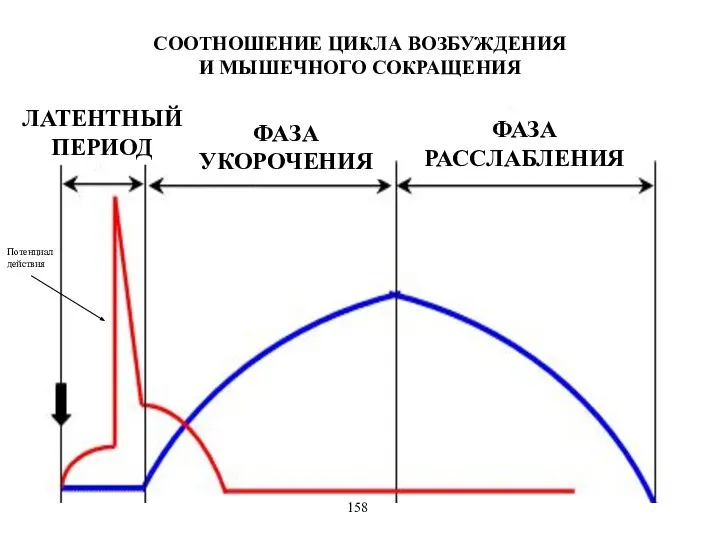
- 21. СООТНОШЕНИЕ ЦИКЛА ВОЗБУЖДЕНИЯ И МЫШЕЧНОГО СОКРАЩЕНИЯ ФАЗА УКОРОЧЕНИЯ ФАЗА РАССЛАБЛЕНИЯ ЛАТЕНТНЫЙ ПЕРИОД Потенциал действия 158
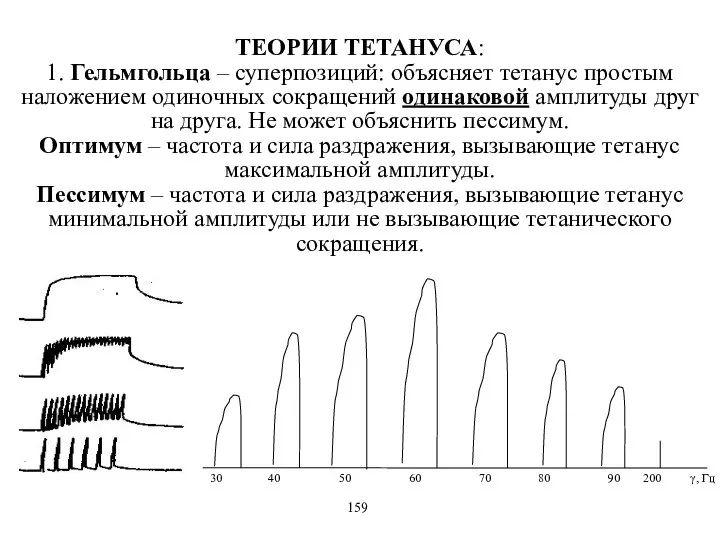
- 22. ТЕОРИИ ТЕТАНУСА: 1. Гельмгольца – суперпозиций: объясняет тетанус простым наложением одиночных сокращений одинаковой амплитуды друг на
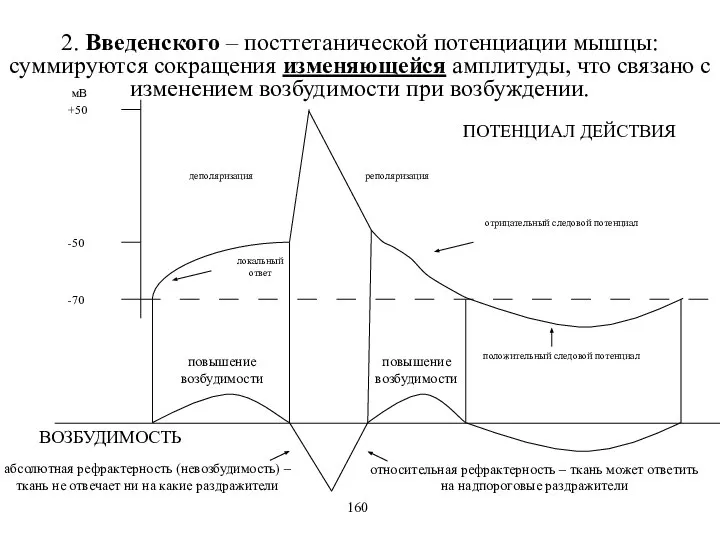
- 23. 2. Введенского – посттетанической потенциации мышцы: суммируются сокращения изменяющейся амплитуды, что связано с изменением возбудимости при
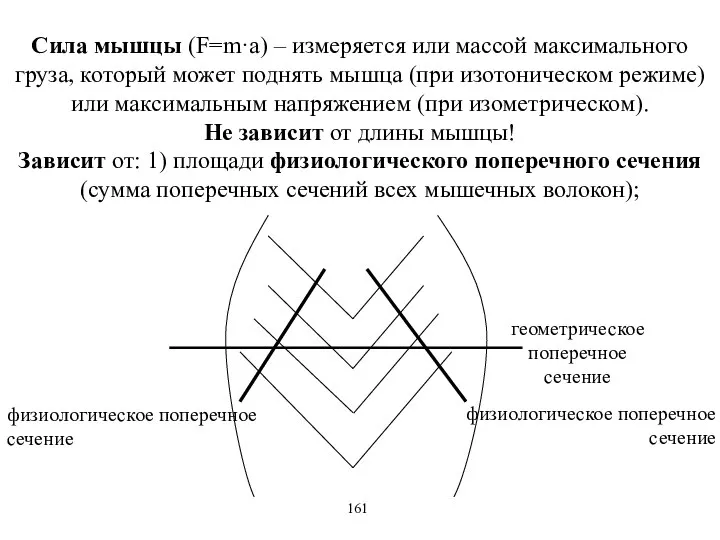
- 24. Сила мышцы (F=m·a) – измеряется или массой максимального груза, который может поднять мышца (при изотоническом режиме)
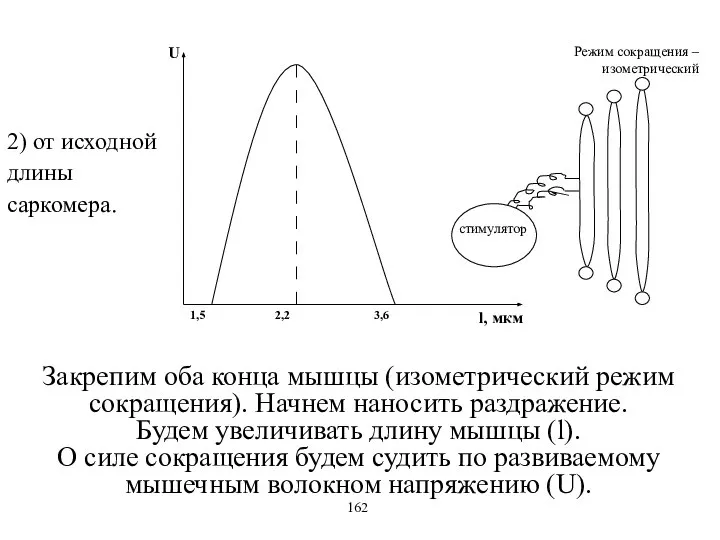
- 25. 2) от исходной длины саркомера. Закрепим оба конца мышцы (изометрический режим сокращения). Начнем наносить раздражение. Будем
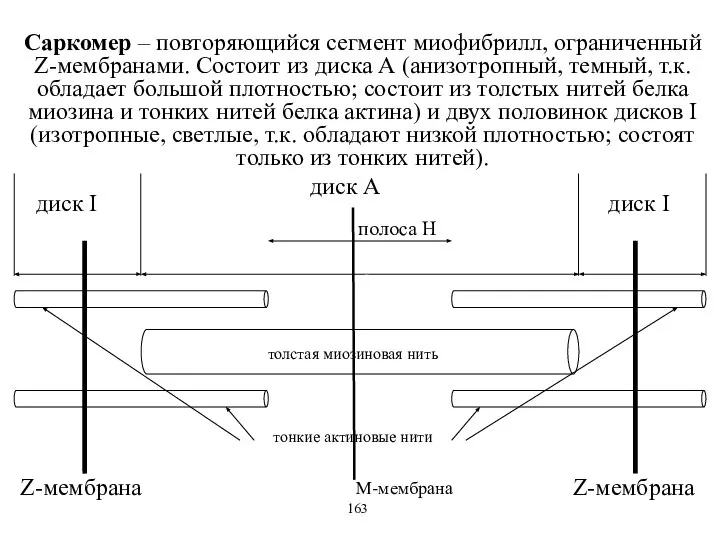
- 26. Саркомер – повторяющийся сегмент миофибрилл, ограниченный Z-мембранами. Состоит из диска А (анизотропный, темный, т.к. обладает большой
- 27. Fм = fэ х n Fм – сила мышцы fэ – сила элементарного рывка (усилие, развиваемое
- 28. Работа мышцы При поднятии груза A=P·h Р – вес груза h – высота поднятия груза При
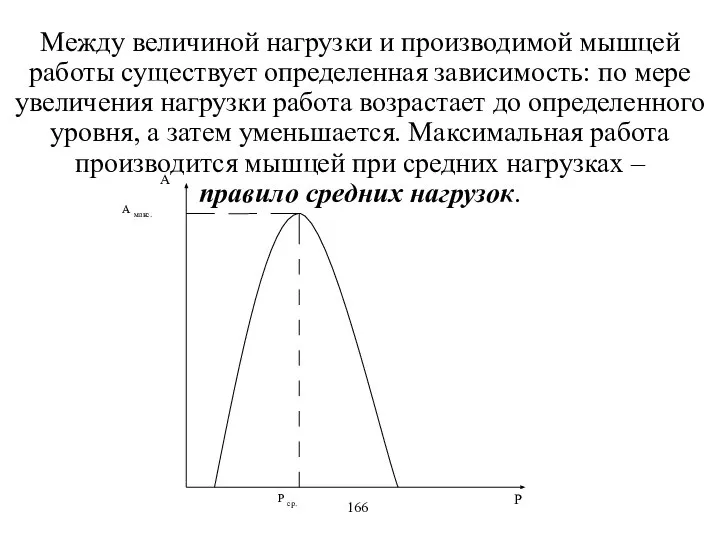
- 29. Между величиной нагрузки и производимой мышцей работы существует определенная зависимость: по мере увеличения нагрузки работа возрастает
- 30. Работа по поддержанию определенного положения тела в пространстве – статическая. Работа мышц по перемещению тела в
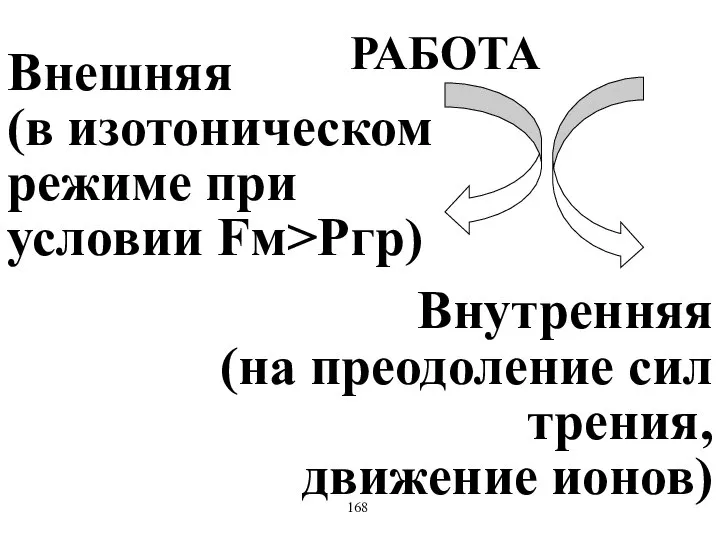
- 31. РАБОТА Внешняя (в изотоническом режиме при условии Fм>Pгр) Внутренняя (на преодоление сил трения, движение ионов) 168
- 32. Коэффициент полезного действия (КПД) мышечной работы представляет собой отношение величины внешней механической работы (W) к общему
- 33. 170 ЭЛЕКТРОМЕХАНИЧЕСКОЕ СОПРЯЖЕНИЕ (МЕМБРАННО-МИОФИБРИЛЛЯРНАЯ СВЯЗЬ) Осуществляет проводящая система мышечного волокна (триада): 1. Цитоплазматическая мембрана мышечного волокна.
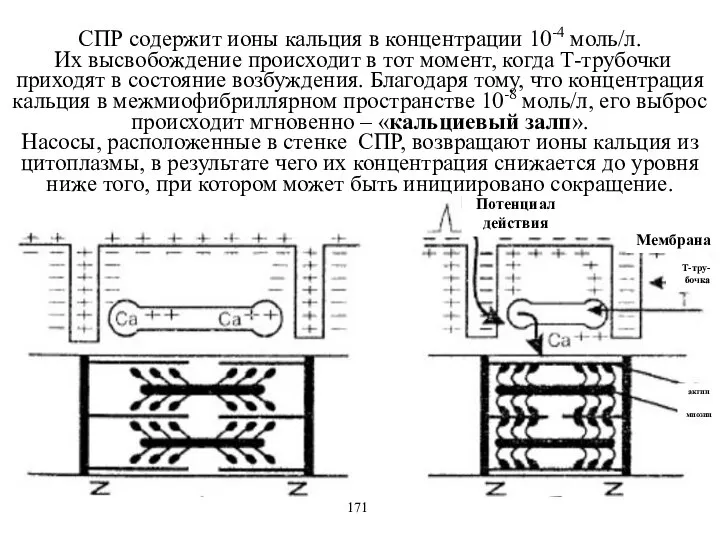
- 34. Потенциал действия Мембрана Т-тру-бочка актин миозин 171 СПР содержит ионы кальция в концентрации 10-4 моль/л. Их
- 35. Механизм сопряжения различен в скелетной, гладкой мышцах и мышце сердца. 172
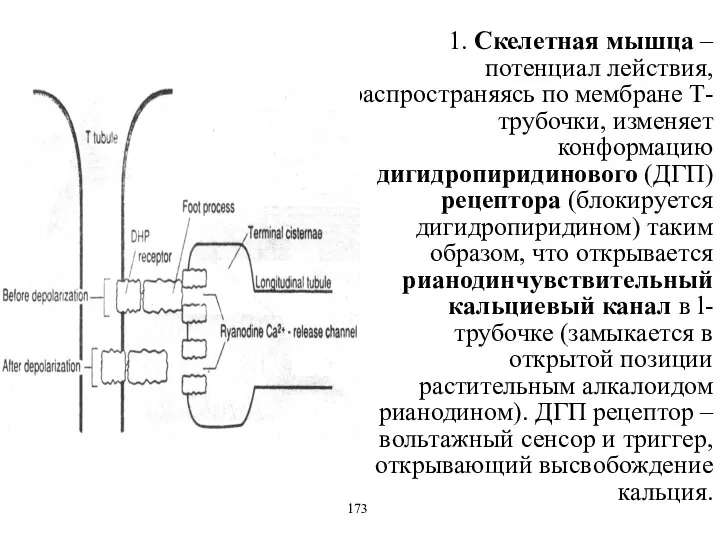
- 36. 1. Скелетная мышца – потенциал лействия, распространяясь по мембране Т-трубочки, изменяет конформацию дигидропиридинового (ДГП) рецептора (блокируется
- 37. 2. Сердечная мышца – потенциал действия изменяет конформацию ДГП-зависимого кальциевого канала Т-трубочки, через который происходит поступление
- 38. Сократительные белки мышц – актин и миозин. Были открыты в середине XIX века: Вильгельм Куне показал,
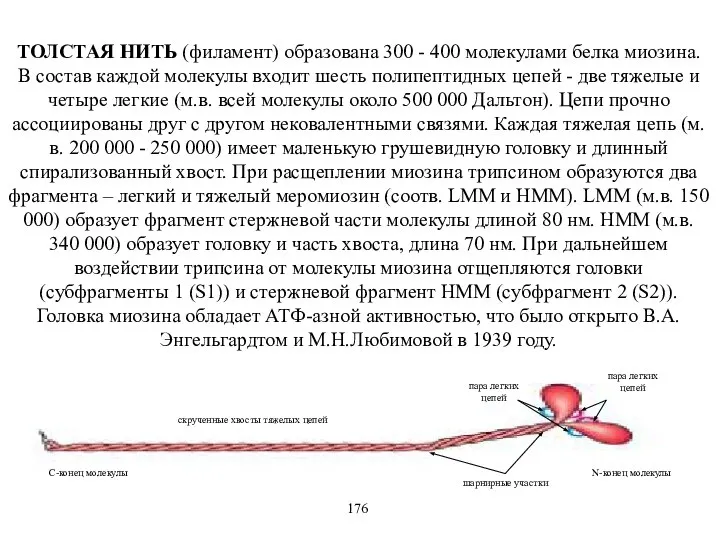
- 39. ТОЛСТАЯ НИТЬ (филамент) образована 300 - 400 молекулами белка миозина. В состав каждой молекулы входит шесть
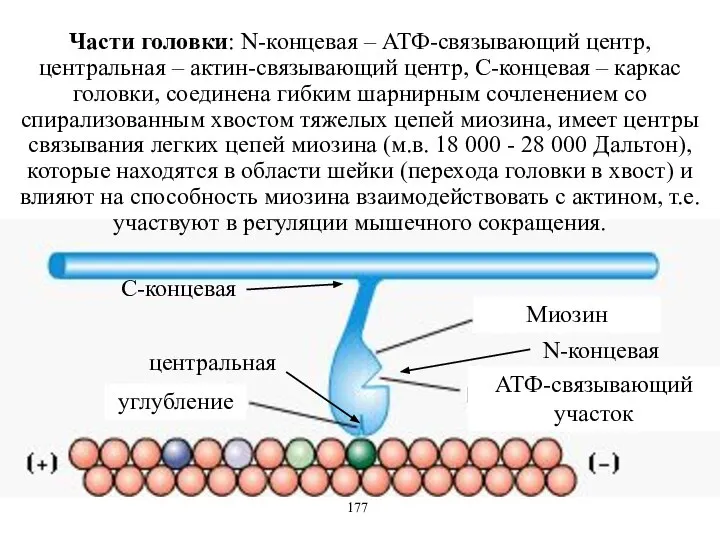
- 40. Части головки: N-концевая – АТФ-связывающий центр, центральная – актин-связывающий центр, С-концевая – каркас головки, соединена гибким
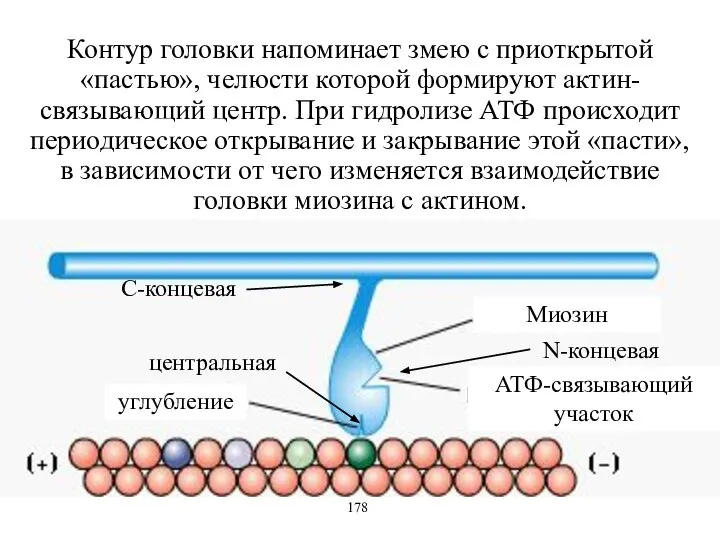
- 41. N-концевая центральная С-концевая Миозин АТФ-связывающий участок углубление 178 Контур головки напоминает змею с приоткрытой «пастью», челюсти
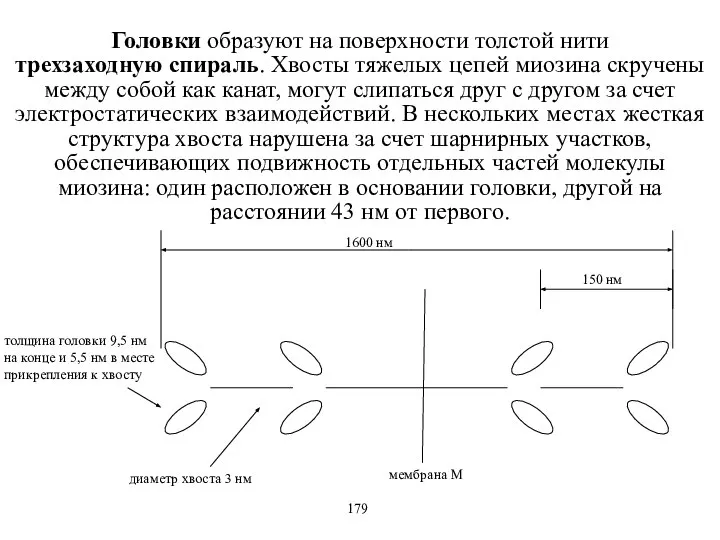
- 42. Головки образуют на поверхности толстой нити трехзаходную спираль. Хвосты тяжелых цепей миозина скручены между собой как
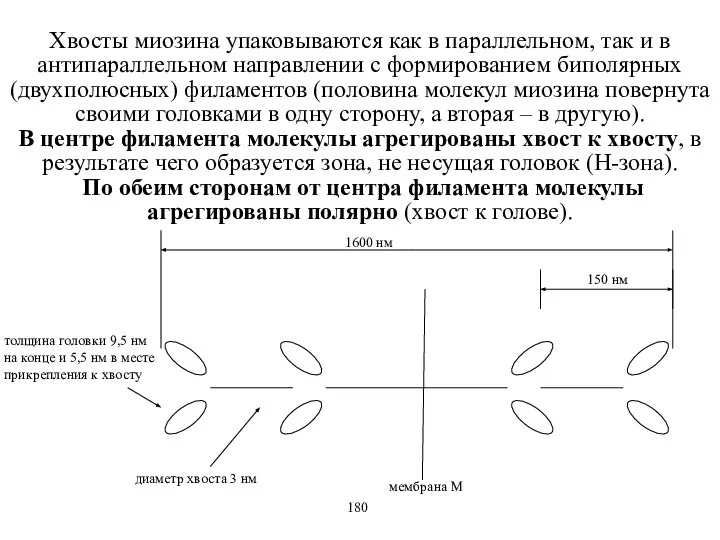
- 43. Хвосты миозина упаковываются как в параллельном, так и в антипараллельном направлении с формированием биполярных (двухполюсных) филаментов
- 44. В поперечном сечении толстая нить содержит 27 молекул миозина. При расположении их всех на поверхности нити,
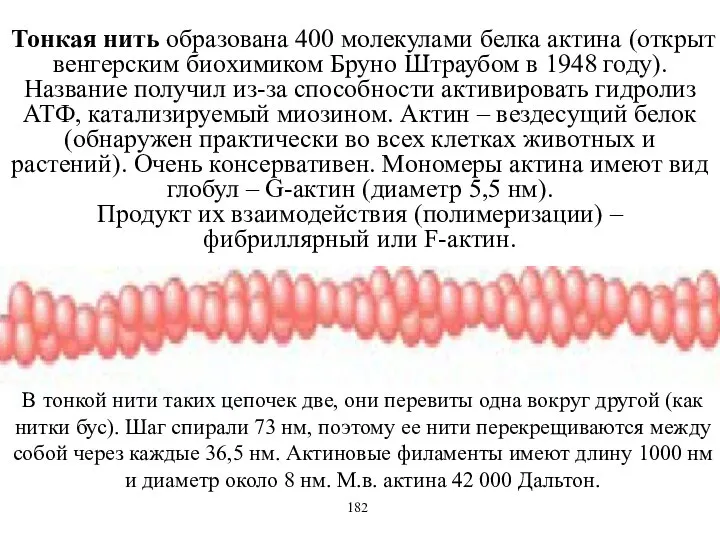
- 45. Тонкая нить образована 400 молекулами белка актина (открыт венгерским биохимиком Бруно Штраубом в 1948 году). Название
- 46. В состав тонкой нити также входят регуляторные белки – стержни тропомиозина и глобулы тропонина (через участки
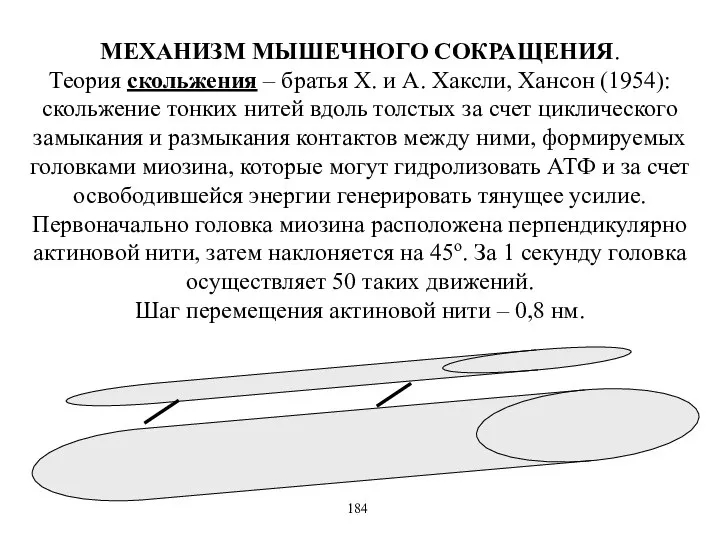
- 47. МЕХАНИЗМ МЫШЕЧНОГО СОКРАЩЕНИЯ. Теория скольжения – братья Х. и А. Хаксли, Хансон (1954): скольжение тонких нитей
- 48. Малый сократительный элемент (МСЭ) – толстая нить, окруженная 6 тонкими (гексагональная упаковка). Имеет внутреннюю «резьбу» –
- 49. В покое головка миозина уподоблена сжатой пружине, распрямиться которой мешает тропонин-тропомиозиновый комплекс, играющий роль защелки. В
- 50. Роль кальция и протонов. Кальций, как уже указывалось, инициирует мышечное сокращение. При гидролизе АТФ появляются протоны.
- 51. МЕХАНИЗМЫ РЕГУЛЯЦИИ МЫШЕЧНОГО СОКРАЩЕНИЯ В конце 19 века в классических опытах английского физиолога С. Рингера была
- 52. Миозиновый тип характерен для гладких мышц, с миозиновыми филаментами которых связан фермент «киназа легких цепей миозина»
- 53. При снижении концентрации кальция в клетке происходит диссоциация Са2+ из катионсвязывающих центров кальмодулина, отсоединение последнего от
- 54. Актиновый тип характерен для поперечнополосатых скелетных мышц и сердечной мышцы. В глубине продольных канавок, образующихся с
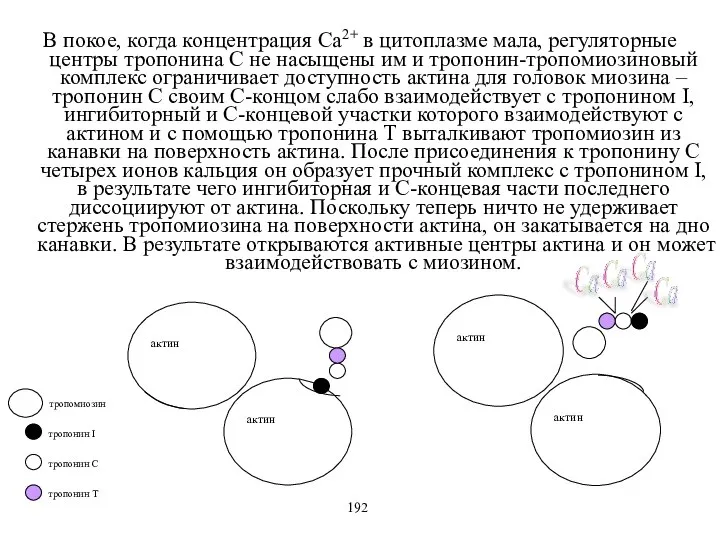
- 55. В покое, когда концентрация Са2+ в цитоплазме мала, регуляторные центры тропонина С не насыщены им и
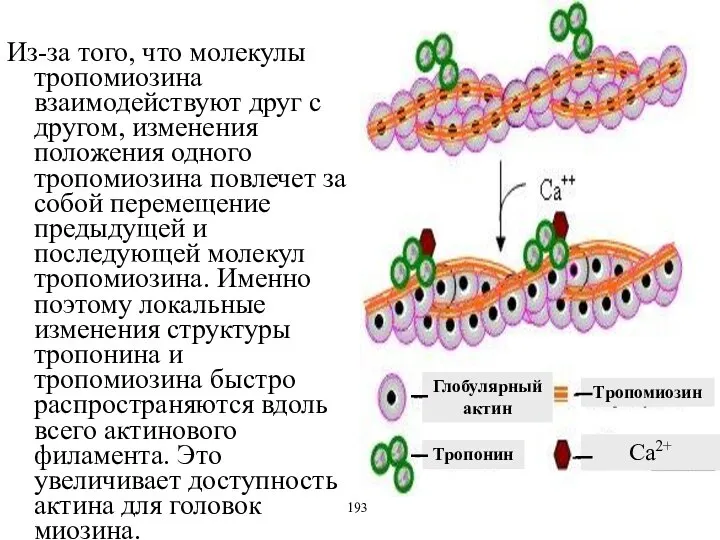
- 56. Из-за того, что молекулы тропомиозина взаимодействуют друг с другом, изменения положения одного тропомиозина повлечет за собой
- 57. ЭНЕРГЕТИКА МЫШЕЧНОГО СОКРАЩЕНИЯ АТФазная реакция креатинкиназная реакция (КФ+АДФ=К+АТФ) гликолиз окислительное фосфорилирование 194
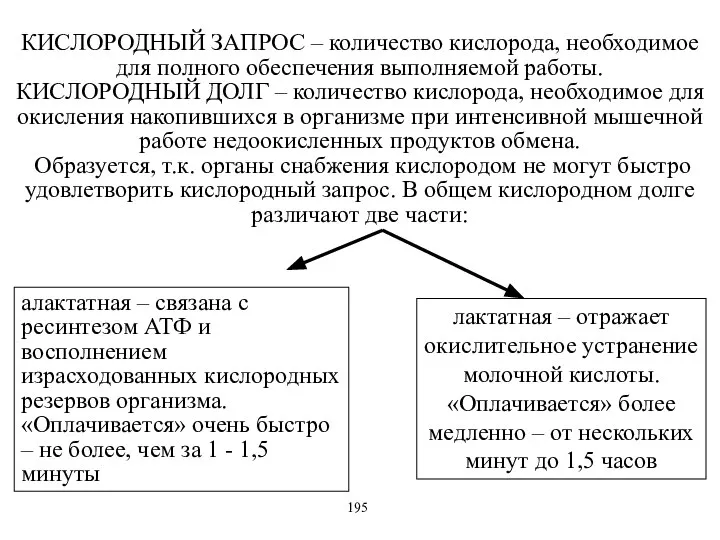
- 58. КИСЛОРОДНЫЙ ЗАПРОС – количество кислорода, необходимое для полного обеспечения выполняемой работы. КИСЛОРОДНЫЙ ДОЛГ – количество кислорода,
- 59. ФАЗЫ ТЕПЛООБРАЗОВАНИЯ В МЫШЦЕ Начальное теплообразование – вызывается биохимическими анаэробными процессами, ведущими к сокращению мышцы: тепло
- 60. В первую фазу выделяется около 40%, а во вторую – около 60% всей тепловой энергии, образовавшейся
- 61. В начале расслабление идёт пассивно – за счёт эластических компонентов мышцы (сухожилий, связок), а затем активно.
- 63. Скачать презентацию



























 Автоматизация послеуборочной обработки зерна
Автоматизация послеуборочной обработки зерна “Безработица равна 100%, если безработный – это Вы”. Адам Смит
“Безработица равна 100%, если безработный – это Вы”. Адам Смит SkyDNS-облачный контент-фильтр
SkyDNS-облачный контент-фильтр Виды работ при построении триангуляции
Виды работ при построении триангуляции  Этапы разработки технического задания
Этапы разработки технического задания Авторитет и лидерство. Формы власти и влияния, стили руководства
Авторитет и лидерство. Формы власти и влияния, стили руководства Генетика и медицина О разрешите мне загадку жизни, Мучительно старинную загадку… Скажите, что такое человек. Г.Гейне Наши врачи должны, как азбуку, знать законы наследственности. И.П. Павлов
Генетика и медицина О разрешите мне загадку жизни, Мучительно старинную загадку… Скажите, что такое человек. Г.Гейне Наши врачи должны, как азбуку, знать законы наследственности. И.П. Павлов Уроки рисования пастелью
Уроки рисования пастелью Место игры в применяемых педагогических образовательных технологиях и ее влияние на укрепление здоровья детей
Место игры в применяемых педагогических образовательных технологиях и ее влияние на укрепление здоровья детей Всички плодове и зеленчуци си имат цвят. Едни са жълти, други зелени, червени, лилави оранжеви. - презентация
Всички плодове и зеленчуци си имат цвят. Едни са жълти, други зелени, червени, лилави оранжеви. - презентация Презентация Роль таможенно-тарифного регулирования в обеспечении экономической безопасности страны
Презентация Роль таможенно-тарифного регулирования в обеспечении экономической безопасности страны  Методы физической культуры
Методы физической культуры Дифференциальные уравнения Однородные дифференциальные уравнения Линейные дифференциальные уравнения Уравнения Бернулли
Дифференциальные уравнения Однородные дифференциальные уравнения Линейные дифференциальные уравнения Уравнения Бернулли Обменное взаимодействие. Симметрия координатных и спиновых функций
Обменное взаимодействие. Симметрия координатных и спиновых функций  Организация и проведение криминологического исследования
Организация и проведение криминологического исследования РЕШЕНИЕ НЕРАВЕНСТВ С ОДНИМ НЕИЗВЕСТНЫМ
РЕШЕНИЕ НЕРАВЕНСТВ С ОДНИМ НЕИЗВЕСТНЫМ  Выйдя на улицу, юный пешеход должен вежливо передвигаться только по тротуару или обочине! - презентация
Выйдя на улицу, юный пешеход должен вежливо передвигаться только по тротуару или обочине! - презентация Отраслевые информационные центры
Отраслевые информационные центры Публикация материалов на сервисе Calaméo © Збицкая Наталья Юрьевна, учитель математики МОУ «Средняя школа №13» г. Балаково Саратовской области
Публикация материалов на сервисе Calaméo © Збицкая Наталья Юрьевна, учитель математики МОУ «Средняя школа №13» г. Балаково Саратовской области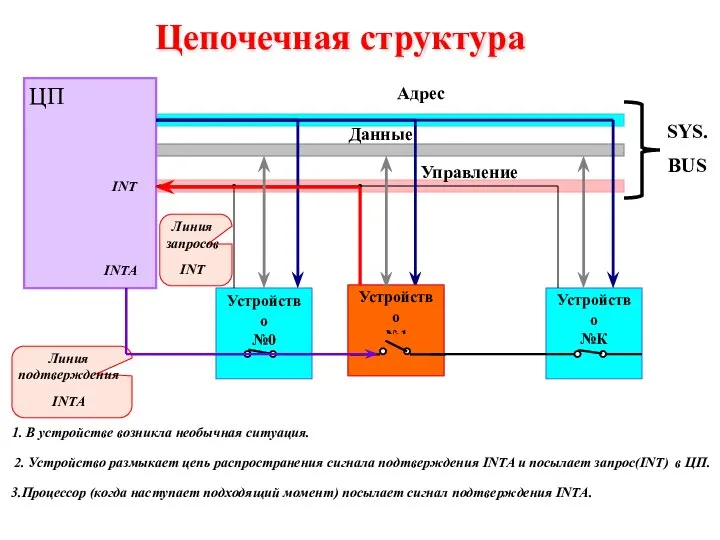 Цепочечная структура
Цепочечная структура Рейтинговая система оценивания достижений учащихся (материалы к выступлению на методическом семинаре) Выполнила зам.директора
Рейтинговая система оценивания достижений учащихся (материалы к выступлению на методическом семинаре) Выполнила зам.директора  Монтаж конструкций
Монтаж конструкций Права и свободы человека и гражданина РФ
Права и свободы человека и гражданина РФ Средства и методы физического воспитания
Средства и методы физического воспитания American versus British English
American versus British English Пример воздействия агрессивной среды на неметаллические конструкции
Пример воздействия агрессивной среды на неметаллические конструкции Презентация Актуальные вопросы административной ответственности за нарушение таможенных правил
Презентация Актуальные вопросы административной ответственности за нарушение таможенных правил  Презентация "Кредитный брокер - для физических лиц" - скачать презентации по Экономике
Презентация "Кредитный брокер - для физических лиц" - скачать презентации по Экономике