Содержание
- 2. Окислительно-восстановительные процессы Под окислением понимаем процесс отдачи (восстановитель окисляется), под восстановлением – приема (окислитель восстанавливается) электронов.
- 3. Примеры реакций Фотосинтез: 106CO2 + 16NO3- + HPO42- + 122H2O +18H+ + 686 кал/моль ––> С106
- 4. Примеры реакций сульфатредукция: SO4 2- + 2H2O + 2Cорг –––> H2S + 2HCO3-; SO4 2- +
- 5. окислительно-восстановительный потенциал Eh Каждая природная вода характеризуется определенной величиной окислительно-восстановительного потенциала Eh, который, как и рН,
- 6. Ео – нормальный (стандартный) потенциал реакции В земной коре окисление и восстановление, как правило, протекают при
- 7. Примеры использования стандартных потенциалов Е0 для геохимических построений Щелочные и щелочноземельные металлы (Na, K, Ca) обладают
- 8. На величину Еh природных вод влияют свободный O2, Н2S, Fe2+, Fe3+, Mn2+, Mn4+, V3+‚ V5+‚ Н+,
- 9. Oкислительная и восстановительная среды Для каждого элемента окислительная и восстановительная среда характеризуется различным Еh (имеют значение
- 10. Смешение вод разного химического состава Большинство природных вод представляет собой сложные смеси по минерализации, составу, температуре,
- 11. Процесс смешения природных вод представляет собой более сложное физико-химическое явление. Прямолинейная зависимость А. Н. Огильви, по-видимому,
- 12. Если с – концентрация г/л, то масса растворенного вещества cV = c1V1 + c2V2 если V2
- 13. Сравнивая фактические (сfact ) и полученные по уравнениям смешения (сteor) концентрации, судим о протекающих процессах, увеличивающих
- 14. При этом наиболее вероятными процессами являются либо переход растворенных компонентов в твердую фазу, либо переход компонентов
- 16. Скачать презентацию













 Правила и методы построения принципиальных электрических схем САУ
Правила и методы построения принципиальных электрических схем САУ Общая схема работы компилятора
Общая схема работы компилятора Презентация Коррупция и методы борьбы с ней
Презентация Коррупция и методы борьбы с ней Древнерусское искусство. Иконопись
Древнерусское искусство. Иконопись Гибкие (Agile) методы управления в условиях цифровой трансформации экономики
Гибкие (Agile) методы управления в условиях цифровой трансформации экономики pravlenie_knyazya_vladimira._kreshchenie_rusi
pravlenie_knyazya_vladimira._kreshchenie_rusi Теория и методика физической культуры. Лекция «Введение в теорию физической культуры»
Теория и методика физической культуры. Лекция «Введение в теорию физической культуры» Басқару қызметі слайд
Басқару қызметі слайд  Образование Белгородской области Презентация для модуля краеведения на уроках природоведения 5 класса Выполнил: учитель природ
Образование Белгородской области Презентация для модуля краеведения на уроках природоведения 5 класса Выполнил: учитель природ Web-сервис для отдела по приему автомобилей предприятия «Автотрейд»
Web-сервис для отдела по приему автомобилей предприятия «Автотрейд» Физические основы Астрофизики
Физические основы Астрофизики  Африка континент в эпоху перемен
Африка континент в эпоху перемен  Базовые модели стратегического планирования
Базовые модели стратегического планирования  Схема взаимодействия таможенных органов России с государствами- членами Таможенного союза при осуществлении проверки экспорт
Схема взаимодействия таможенных органов России с государствами- членами Таможенного союза при осуществлении проверки экспорт Интервью у Бога
Интервью у Бога Презентация "Торгово-промышленная палата Республики Карелия" - скачать презентации по Экономике
Презентация "Торгово-промышленная палата Республики Карелия" - скачать презентации по Экономике Международное публичное право. ООН: история, структура, цели и задачи
Международное публичное право. ООН: история, структура, цели и задачи Развитие педагогической мысли в России
Развитие педагогической мысли в России  Программирование с "защитой от ошибок". Сквозной структурный контроль
Программирование с "защитой от ошибок". Сквозной структурный контроль Презентация КОММЕРЧЕСКАЯ ОРГАНИЗАЦИЯ С ИНОСТРАННЫМИ ИНВЕСТИЦИЯМИ
Презентация КОММЕРЧЕСКАЯ ОРГАНИЗАЦИЯ С ИНОСТРАННЫМИ ИНВЕСТИЦИЯМИ  Департамент образования Ярославской области Государственное образовательное учреждение среднего профессионального образовани
Департамент образования Ярославской области Государственное образовательное учреждение среднего профессионального образовани Монолитные ребристые перекрытия с балочными плитами
Монолитные ребристые перекрытия с балочными плитами Интегрированная среда разработки программного обеспечения Microsoft Visual Studio. Платформа.NET. Среда Visual Studio.NET
Интегрированная среда разработки программного обеспечения Microsoft Visual Studio. Платформа.NET. Среда Visual Studio.NET Социальное партнерство в сфере труда
Социальное партнерство в сфере труда Принцип Дирихле
Принцип Дирихле Математический бой
Математический бой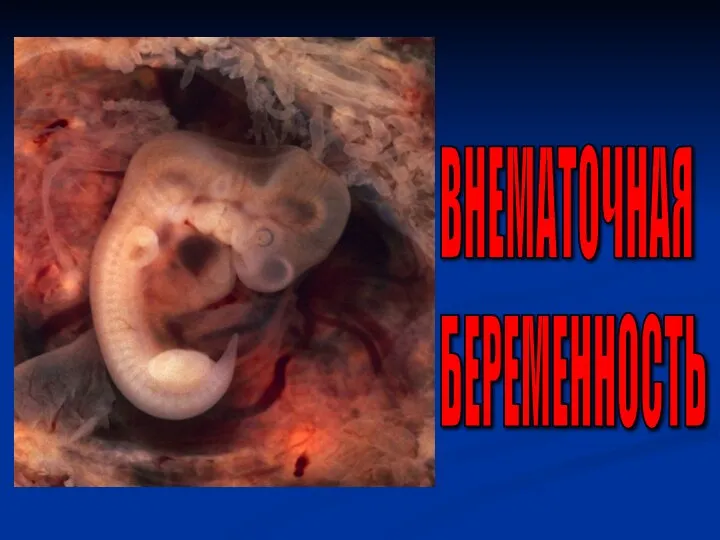 Презентация на тему "Внематочная беременность" - скачать презентации по Медицине
Презентация на тему "Внематочная беременность" - скачать презентации по Медицине Эндоскопия
Эндоскопия