Содержание
- 2. Мета дисципліни – оволодіння комплексом знань з основних розділів прикладної економіки, знайомство з методами організації ефективного
- 3. Програма дисципліни Підприємство і підприємництво 1.1 Галузева структура виробництва 1.2 Виробниче підприємство-основа економіки 1.3 Основи підприємницької
- 4. Фармацевтична галузь та суспільство “Фармгалузь суттєво домінує над науковим суспільством за впливом на масову свідомість посередством
- 5. ФАРМАЦЕВТИЧНА ГАЛУЗЬ – сукупність підприємств, організацій і установ, зайнятих у процесі створення, виробництва, реалізації лікарських субстанцій,
- 6. Організаційна побудова і взаємозв’язки фармацевтичної галузі України Міністерство охорони здоров'я
- 8. Державна служба України з лікарських засобів (Держлікслужб України) є центральним органом виконавчої влади, діяльність якого спрямовується
- 9. ТЕХНІКО –ЕКОНОМІЧНІ ОСОБЛИВОСТІ ФАРМАЦЕВТИЧНОГО ВИРОБНИЦТВА: Фармацевтична галузь випускає продукцію особливої значущості, що обумовлює особливі вимоги до
- 10. Аналіз рис інноваційної і традиційної моделі розвитку фармацевтичного виробництва
- 11. ВІТЧИЗНЯНА ФАРМАЦЕВТИЧНА ПРОМИСЛОВІСТЬ На 1.01.2012 в Україні мають ліцензію на виробництво лікарських засобів – 108 підприємств.
- 12. ТОР – 20 фармацевтичних компаній на українському фармацевтичному ринку
- 13. Причини зниження ефективності лікарського забезпечення в Україні і доступності якісних лікарських засобів вітчизняного виробництва: 1. В
- 14. Шляхи розвитку фармацевтичної галузі України в умовах переходу до інноваційно-інвестиційної моделі: Передбачити дієві законодавчі механізми підтримки
- 15. 4. Розробити систему моніторингу та аналізу потреби населення України у життєво необхідних лікарських засобах, а також
- 16. 16. Розробити державні цільові програми із визначенням джерел їх фінансування, термінів виконання і відповідальних осіб (структур)
- 17. Виробництво лікарських засобів розвивається за такими напрямками: Створення нових лікарських засобів Створення копій та їх модифікація
- 18. ІННОВАЦІЙНИЙ ЛІКАРСЬКИЙ ПРЕПАРАТ ГЕНЕРИЧНИЙ ЛІКАРСЬКИЙ ПРЕПАРАТ Докліничне вивчення за GLP Клінічні випробування за GCP Виробництво за
- 19. З постанови Кабинету Міністрів України від 28.10.2004р. № 1419: “Міністерству охорони здоров'я забезпечити починаючи з 1
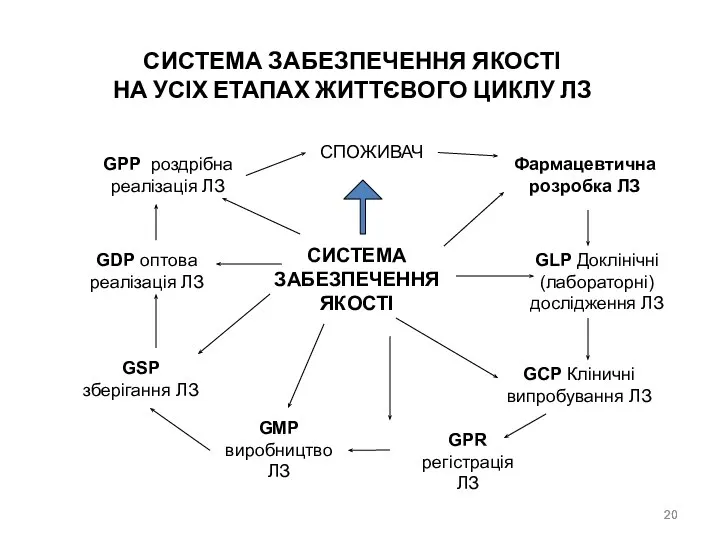
- 20. СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ НА УСІХ ЕТАПАХ ЖИТТЄВОГО ЦИКЛУ ЛЗ СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ СПОЖИВАЧ Фармацевтична розробка ЛЗ
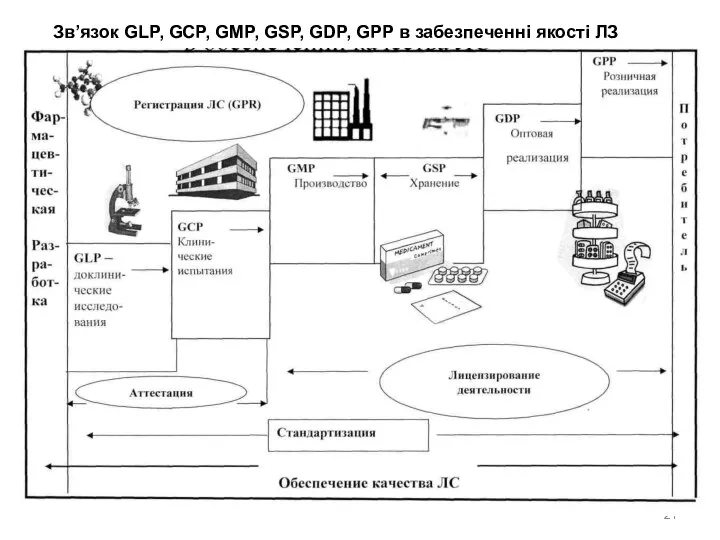
- 21. Зв’язок GLP, GCP, GMP, GSP, GDP, GPP в забезпеченні якості ЛЗ
- 23. Скачать презентацию
Мета дисципліни – оволодіння комплексом знань з основних розділів прикладної економіки,
Мета дисципліни – оволодіння комплексом знань з основних розділів прикладної економіки,
Завдання дисципліни вивчення стану та перспектив розвитку фармацевтичної галузі та фармацевтичної промисловості України, шляхів підвищення ефективності використання матеріальних, трудових, фінансових ресурсів підприємств в ринковій економіці, питань організації праці та заробітної плати, механізму формування собівартості продукції та цін, особливостей управління підприємством в умовах ринку, проблем інвестиційної, інноваційної, зовнішньоекономічної діяльності підприємств та ін.
Програма дисципліни
Підприємство і підприємництво
1.1 Галузева структура виробництва
1.2 Виробниче підприємство-основа економіки
1.3 Основи
Програма дисципліни
Підприємство і підприємництво
1.1 Галузева структура виробництва
1.2 Виробниче підприємство-основа економіки
1.3 Основи
2. Ресурсне забезпечення підприємства
2.1 . Основні фонди підприємства
2.2. Оборотні кошти підприємства
2.3. Матеріально-технічне забезпечення підприємства
2.4 Фінансово-кредитні та нематеріальні ресурси підприємства
2.5 Праця та заробітна плата
2.6 Інвестиційні ресурси підприємства.
3. Результати та ефективність виробництва
3.1 Витрати і собівартість продукції
3.2 Ціни та ціноутворення в ринкових умовах
3.3 Фінансово-економічні результати діяльності підприємства.
3.4 Економічна і соціальна ефективність виробництва
3.5 Якість продукції
4. Умови і фактори економічного розвитку підприємства
4.1 Інноваційна діяльність підприємства
4.2 Планування діяльності підприємства
4.3 Зовнішньоекономічна діяльність підприємства
4.4. Реструктуризація й санація підприємств та організацій
4.5 Банкрутство й ліквідація підприємства (організації)
Фармацевтична галузь та суспільство
“Фармгалузь суттєво домінує над науковим суспільством за впливом
Фармацевтична галузь та суспільство
“Фармгалузь суттєво домінує над науковим суспільством за впливом
ФАРМАЦЕВТИЧНА ГАЛУЗЬ – сукупність підприємств, організацій і установ, зайнятих у
ФАРМАЦЕВТИЧНА ГАЛУЗЬ – сукупність підприємств, організацій і установ, зайнятих у
До складу фармацевтичної галузі входять:
1)фармацевтичні підприємства – виробники ЛП, субстанцій, харчових добавок, ветеринарних препаратів, лікувальних косметичних засобів та ін.;
2) підприємства, які здійснюють оптову та роздрібну реалізацію цієї продукції;
3) наукові заклади, які виконують науково-дослідні та дослідно-конструкторські роботи зі створення нових ЛП, технологічних процесів, обладнання та методів контролю якості;
4) навчальні заклади та факультети, які здійснюють підготовку та перепідготовку фахівців для потреб галузі (фармацевтів, провізорів, клінічних провізорів, спеціалістів з лабораторної діагностики, інженерів-технологів з виробництва фармацевтичних препаратів, біотехнологів, провізорів-косметологів, економістів, маркетологів, менеджерів та ін.);
5) організації та установи, які формують і реалізують інформаційно-аналітичне забезпечення фармацевтичної галузі. В Україні фармацевтична підпорядкована МОЗ;
6) входять установи які здійснюють контроль за якістю ЛЗ.
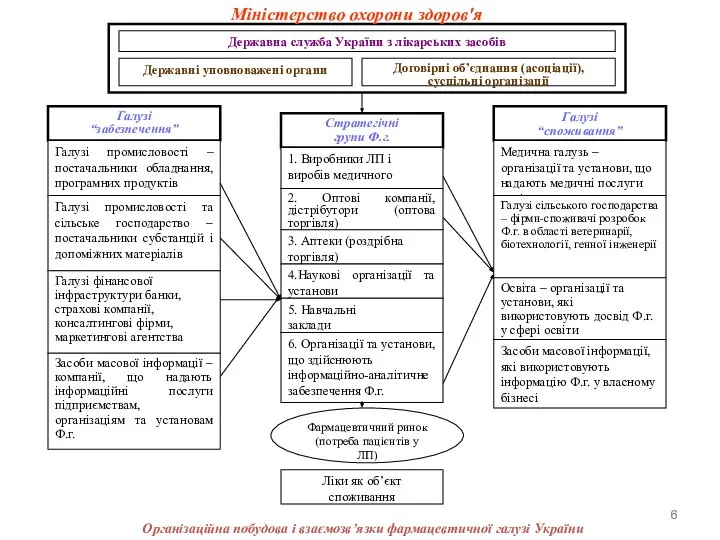
Організаційна побудова і взаємозв’язки фармацевтичної галузі України
Міністерство охорони здоров'я
Організаційна побудова і взаємозв’язки фармацевтичної галузі України
Міністерство охорони здоров'я
Державна служба України з лікарських засобів (Держлікслужб України) є центральним
Державна служба України з лікарських засобів (Держлікслужб України) є центральним
Держлікслужба України входить до системи органів виконавчої влади у галузі охорони здоров'я та утворюється для забезпечення реалізації державної політику сферах контролю якості та безпеки лікарських засобів, у тому числі медичних імунобіологічних препаратів медичної техніки і виробів медичного призначення, що перебувають в обігу та / або застосовуються у сфер охорони здоров'я, дозволені до реалізації в аптечних закладах і їх структурних підрозділах, а також ліцензування господарської діяльності з виробництва лікарських засобів, оптової та роздрібної торгівлі лікарськими засобами.
Основними завданнями Держлікслужби України є:
внесення пропозицій щодо формування державної політики у сферах контролю якості та безпеки лікарських засобів, медичних виробів, а також ліцензування господарської діяльності з виробництва лікарських засобів, оптової та роздрібної лікарськими засобами;
реалізація державної політики у сфері державного контролю якості та безпеки лікарських засобів і медичних виробів;
ліцензування господарської діяльності з виробництва лікарських засобів, оптової та роздрібної торгівлі лікарськими засобами.
ПОЛОЖЕННЯ ПРО ДЕРЖАВНУ СЛУЖБУ УКРАЇНИ
З ЛІКАРСЬКИХ ЗАСОБІВ
ТЕХНІКО –ЕКОНОМІЧНІ ОСОБЛИВОСТІ ФАРМАЦЕВТИЧНОГО ВИРОБНИЦТВА:
Фармацевтична галузь випускає продукцію особливої значущості,
ТЕХНІКО –ЕКОНОМІЧНІ ОСОБЛИВОСТІ ФАРМАЦЕВТИЧНОГО ВИРОБНИЦТВА:
Фармацевтична галузь випускає продукцію особливої значущості,
Економічна стійкість галузі до змін політичної та економічної ситуації в країні;
Висока матеріаломісткість продукції;
Висока наукомісткість виробництва та особливості інноваційних процесів;
Малотонажність виробництва;
Великий асортимент продукції, що випускається;
Велика кількість технологічних процесів, багато стадійність виробництва;
Велика кількість технологічного обладнання, які підвернені прискореному зносу;
Додаткові витрати пов’язані з охороною праці та навколишнього середовища;
Особливі вимоги до підготовки персоналу;
Відносно короткий життєвий цикл ЛЗ;
Особливості ціноутворення на ЛЗ;
Високий рівень конкуренції, який притаманний фармацевтичній галузі;
Низький рівень еластичності попиту на ЛЗ.
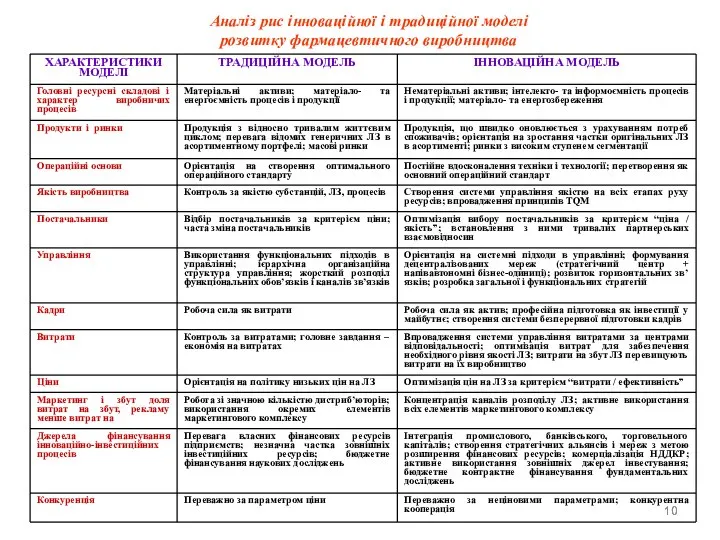
Аналіз рис інноваційної і традиційної моделі
розвитку фармацевтичного виробництва
Аналіз рис інноваційної і традиційної моделі
розвитку фармацевтичного виробництва
ВІТЧИЗНЯНА ФАРМАЦЕВТИЧНА ПРОМИСЛОВІСТЬ
На 1.01.2012 в Україні мають ліцензію на виробництво лікарських
ВІТЧИЗНЯНА ФАРМАЦЕВТИЧНА ПРОМИСЛОВІСТЬ
На 1.01.2012 в Україні мають ліцензію на виробництво лікарських
з них виробники субстанцій - 13
фармацевтичних фабрик - 27
На відповідність вимогам Належної виробничої практики сертифіковано 38 виробничі дільниці, подано заявок на проходження сертифікації ще на 99 дільниці.
На 1.03.2011 року в Україні зареєстровано 14308 ліків, з них 11527 – торгових марок готових лікарських засобів (ТМ), інші – субстанції та упаковки in bulk. Із ТМ вітчизняного виробництва – 3057, що складає 26,5%. Частка імпортних ТМ приходиться 73,5% всіх ліків, зареєстрованих в Україні.
Частка оригінальних лікарських засобів складає приблизно 5% від загального обсягу реалізації.
Номенклатура вітчизняних ліків складає до 4000 найменувань практично всіх фармакотерапевтичних груп.
За останні 5 років українськими підприємствами щорічно впроваджується у виробництво більше 100 найменувань лікарських засобів, у 2007 - 126, з них:
оригінальних – біля 5 % від запровадженої номенклатури
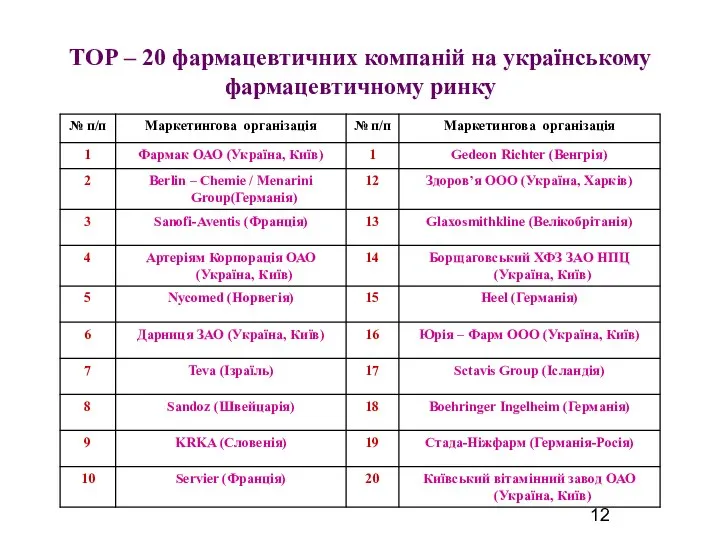
ТОР – 20 фармацевтичних компаній на українському фармацевтичному ринку
ТОР – 20 фармацевтичних компаній на українському фармацевтичному ринку
Причини зниження ефективності лікарського забезпечення в Україні і доступності якісних лікарських
Причини зниження ефективності лікарського забезпечення в Україні і доступності якісних лікарських
1. В Україні не виробляється необхідний асортимент основних лікарських засобів.
2. До державних цільових програм не були включені розробки необхідних вітчизняних лікарських препаратів-генериків та оригінальних препаратів, які б могли замінити імпортні аналоги і мали б нижчу ціну;
3. В Україні втрачені існуючі та припинено розробки й впровадження нових технологій виробництва біотехнологічних препаратів та вакцин;
4. Практично всі підприємства-виробники фармацевтичної галузі України є акціонерними підприємствами, а тому самостійно визначають асортимент продукції, що виробляється;
5. Відсутня ефективна система преференцій для вітчизняних фармвиробників при державних закупівлях лікарських препаратів.
МОЗ України не планувало розробку за державні кошти вітчизняних препаратів на заміну імпорту з таких причин:
Відсутності фармацевтичних виробників з державною формою власності, де можна було б розмістити виробництво створених за державні кошти лікарських засобів;
Обмеженості дієвих механізмів партнерської взаємодії держави та фармацевтичного бізнесу;
Недостатньої уваги державних органів влади до стимулювання фармацевтичних виробничих підприємств стосовно розробки та виробництва інноваційних лікарських препаратів шляхом надання інноваційного податкового кредиту, державних гарантій щодо страхування інноваційних ризиків та ін.;
Повільних темпів переходу фармацевтичних виробників України до вимог Належної виробничої практики (GMP).
Шляхи розвитку фармацевтичної галузі України в умовах переходу до інноваційно-інвестиційної моделі:
Передбачити
Шляхи розвитку фармацевтичної галузі України в умовах переходу до інноваційно-інвестиційної моделі:
Передбачити
Сформувати сучасну систему економічного й аналітичного забезпечення у галузі наукових розробок, активізувати створення інтегрованих науково-освітніх структур у системі МОЗ України, сприяти розвитку науково-дослідної інфраструктури, залученню і формуванню венчурного капіталу. Як свідчить міжнародна практика, особливе значення сьогодні слід приділяти організації внутрішнього фірмових венчурних підрозділів у науково-дослідних інститутах (центрах) і віщих навчальних закладах, які безпосередньо будуть займатися питаннями комерціалізації наукових розробок. Передбачити створення у системі МОЗ України, провідних науково-дослідних інститутах і навчальних закладах сучасної патентно-інформаційної бази та довідково-пошукового апарату до неї з використанням світових досягнень інформатики і патентних технологій. Всі ці заходи дозволяють усунути розрив між фундаментальними дослідженнями та їх безпосереднім впровадженням у виробництво.
Визначити перелік пріоритетних (стратегічних) фармвиробників в Україні, які мають відповідну науково-дослідну, матеріальну базу і висококваліфікований персонал для розміщення на них на конкурентній основі виробництва імпортозаміщуючих лікарських засобів, створених за бюджетні кошти; стимулювати зацікавленість фармвтиробників щодо розвитку інноваційних процесів шляхом надання інноваційних податкових кредитів, відкриття безвідсоткових кредитних ліній та інші. Сформувати перелік критеріїв (вимог) щодо належних фармацевтичних підприємств, які дозволяють підприємствам використовувати преференції та мати режим найбільшого сприяння.
4. Розробити систему моніторингу та аналізу потреби населення України у життєво
4. Розробити систему моніторингу та аналізу потреби населення України у життєво
5. Фінансування за кошти держбюджету закупівлю ліцензій на виробництво інноваційних лікарських засобів, призначених для лікування соціально-небезпечних захворювань (туберкульоз, СНІД та ін.), з подальшим розміщенням їх виробництва на конкурсній основі на пріоритетних (незалежних) фармацевтичних підприємствах.
6. Усунути надлишкові адміністративні бар'єри при реєстрації нових лікарських засобів вітчизняного виробництва.
7. Впровадити нову систему преференцій щодо Державної закупівлі вітчизняних лікарських засобів. Забезпечити пріоритет державних закупівель лікарських препаратів вітчизняного виробництва, які розроблені за державні кошти і мають необхідний рівень якості та доказовості їх ефективності та безпечності.
8. Здійснити Державну підтримку виробничих аптек з приготування екстемпоральних, дитячих, орфанних лікарських засобів з переліку життєво необхідних. Визначити відповідний орган, що буде координувати діяльність аптечних закладів щодо централізованого забезпечення обладнанням, лікарськими субстанціями, щодо.
9. Провести необхідне удосконалення існуючої системи просування лікарських засобів, оскільки на даний час вона в більшій мірі стимулює фармвиробників вкладати значні кошти не в інноваційні розробки, а в проведення маркетингових заходів і рекламу.
10. Опрацювати можливість створення регіональних фармацевтичних кластерів із залученням наявного наукового, освітнього, виробничого, кадрового потенціалу окремих регіонів (м. Харків, м. Київ, м. Львів).
11. Здійснити реконструкцію, розширення, а також при необхідності будівництво нових підприємств з виробництва інноваційних лікарських засобів.
12. Розробити та затвердити гармонізовані настанови з біологічних та біотехнологічних препаратів.
13. Здійснити за бюджетні кошти технічне переобладнання Державного підприємства “Державний науковий центр лікарських засобів і медичної продукції” та провести його реорганізацію шляхом приєднання до Національного фармацевтичного університету.
14. Передбачити будівництво нових та реконструкцію існуючих спеціалізованих лабораторій та віваріїв, придбання сучасного лабораторного обладнання для розробки інноваційних лікарських засобів, що потребують індивідуальних технічних засобів.
15. Затвердити перелік наукового та технологічного обладнання для фармації (в тому числі комплектуючих та запасних частин до нього), аналогів якого не виробляють в Україні, ввіз якого на митну територію України не підлягає оподаткуванню ПДВ.
16. Розробити державні цільові програми із визначенням джерел їх фінансування, термінів
16. Розробити державні цільові програми із визначенням джерел їх фінансування, термінів
16.1. Протитуберкульозні препарати.
16.2. Препарати для профілактики та лікування СНІДу.
16.3. Препарати для лікування онкологічних хворих.
16.4. Препарати для лікування розсіяного склерозу.
16.5. Препарати у формі аерозолів для лікування бронхіальної астми та хронічного обструктивного бронхіту.
16.6. Препарати для дітей (дитячі лікарські форми).
16.7. Лікарські засоби замісної підтримувальної терапії при лікуванні наркотичної залежності.
16.8. Вакцини, генні діагностикуми, антибіотики, моноклональні антитіла, тощо.
16.9. Препарати інших фармакотерапевтичних груп.
16.10. Розробка та організація виробництва лікарських субстанцій.
16.11. Інші препарати за замовленням МОЗ України.
Розробка таких лікарських препаратів та їх виробництво потребує залучення до однієї державної цільової програми різних центральних органів виконавчої влади, підприємств та організацій різних галузей національної економіки і вимагає централізованого фінансування з державного бюджету.
Такий підхід надасть можливість швидко здійснити впровадження у виробництво багатьох життєво важливих вітчизняних імпортозаміщуючих лікарських засобів, відтворити виробництво більшості фармацевтичних субстанцій в Україні та вивести на сучасний рівень вітчизняні фундаментальні дослідження по створенню оригінальних фармацевтичних субстанцій.
Виробництво лікарських засобів розвивається
за такими напрямками:
Створення нових
лікарських засобів
Створення
Виробництво лікарських засобів розвивається
за такими напрямками:
Створення нових
лікарських засобів
Створення
модифікація
(зниження ціни на
лікарські засоби)
Модифіковані
генерики:
препарати
2 – 4-го покоління
Оригінальні
лікарські
засоби
Інноваційні
лікарські
засоби
Раціональна фармакокінетика за умови оптимальної терапевтичної концентрації ЛЗ
Різні вимоги
до регістраційних
документів
та процедури
регістрації !!!
2. Для копій: ціль -
підвищення
безпеки
та клінічної
ефективності
діючих
речовин
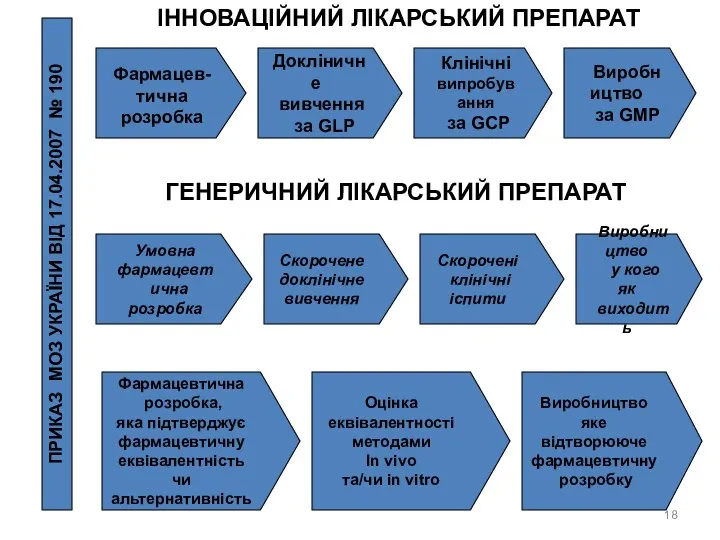
ІННОВАЦІЙНИЙ ЛІКАРСЬКИЙ ПРЕПАРАТ
ГЕНЕРИЧНИЙ ЛІКАРСЬКИЙ ПРЕПАРАТ
Докліничне
вивчення
за GLP
Клінічні
випробування
за
ІННОВАЦІЙНИЙ ЛІКАРСЬКИЙ ПРЕПАРАТ
ГЕНЕРИЧНИЙ ЛІКАРСЬКИЙ ПРЕПАРАТ
Докліничне
вивчення
за GLP
Клінічні
випробування
за
Виробництво
за GMP
Умовна
фармацевтична
розробка
Скорочене
доклінічне
вивчення
Скорочені
клінічні
іспити
Виробництво
у кого як
виходить
Фармацевтична
розробка,
яка підтверджує
фармацевтичну
еквівалентність чи
альтернативність
Оцінка
еквівалентності
методами
In vivo
та/чи in vitro
Виробництво
яке відтворююче
фармацевтичну
розробку
ПРИКАЗ МОЗ УКРАЇНИ ВІД 17.04.2007 № 190
Фармацев-тична
розробка
З постанови Кабинету Міністрів України від 28.10.2004р. № 1419:
“Міністерству охорони здоров'я
З постанови Кабинету Міністрів України від 28.10.2004р. № 1419: “Міністерству охорони здоров'я
СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ
НА УСІХ ЕТАПАХ ЖИТТЄВОГО ЦИКЛУ ЛЗ
СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ
СПОЖИВАЧ
Фармацевтична
СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ
НА УСІХ ЕТАПАХ ЖИТТЄВОГО ЦИКЛУ ЛЗ
СИСТЕМА ЗАБЕЗПЕЧЕННЯ ЯКОСТІ
СПОЖИВАЧ
Фармацевтична
GLP Доклінічні (лабораторні) дослідження ЛЗ
GCP Кліничні випробування ЛЗ
GPR регістрація ЛЗ
GMP виробництво ЛЗ
GPP роздрібна реалізація ЛЗ
GDP оптова реалізація ЛЗ
GSP зберігання ЛЗ
Зв’язок GLP, GCP, GMP, GSP, GDP, GPP в забезпеченні якості ЛЗ
Зв’язок GLP, GCP, GMP, GSP, GDP, GPP в забезпеченні якості ЛЗ














 Классификация продовольственных товаров на группы однородной продукции
Классификация продовольственных товаров на группы однородной продукции  Журнал «Современник» – боевой орган революционной демократии
Журнал «Современник» – боевой орган революционной демократии Презентация "Анри де Тулуз-Лотрек. Жизнь и творчество Маленького гения" - скачать презентации по МХК
Презентация "Анри де Тулуз-Лотрек. Жизнь и творчество Маленького гения" - скачать презентации по МХК Хохломская роспись
Хохломская роспись Реконструкция газпромовской универсальной спортивной площадки
Реконструкция газпромовской универсальной спортивной площадки Traditions of the USA
Traditions of the USA Здоровьесберегающие технологии на уроках физической культуры
Здоровьесберегающие технологии на уроках физической культуры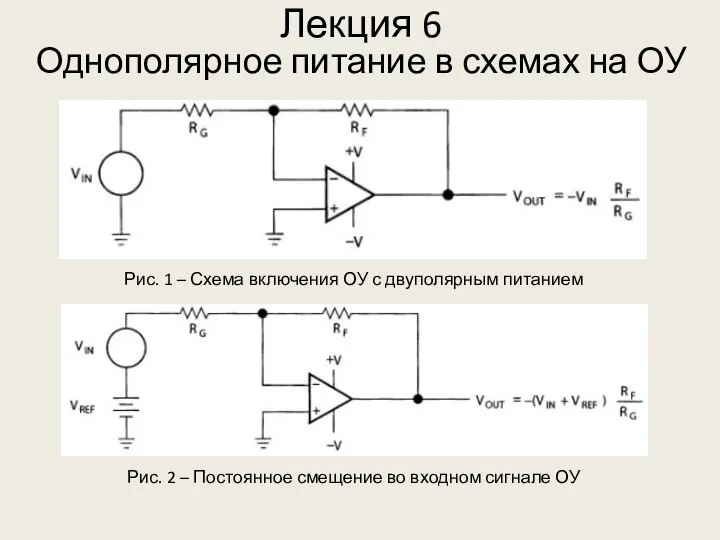 Однополярное питание в схемах на ОУ. (Лекция 6)
Однополярное питание в схемах на ОУ. (Лекция 6) Филология в системе современного гуманитарного знания
Филология в системе современного гуманитарного знания Контрабанда леса
Контрабанда леса Kleidung
Kleidung Презентация Совместное равновесие на рынках благ и денег: модель IS-LM (модель Хикса)
Презентация Совместное равновесие на рынках благ и денег: модель IS-LM (модель Хикса) Дослідження хімічного складу їжі
Дослідження хімічного складу їжі  Основная образовательная программа начального общего образования МОУ «Соколовская СОШ» Заместитель директора по учебно-вос
Основная образовательная программа начального общего образования МОУ «Соколовская СОШ» Заместитель директора по учебно-вос Эксплуатация, техническое обслуживание и ремонт автомобильных кондиционеров
Эксплуатация, техническое обслуживание и ремонт автомобильных кондиционеров Презентация "Налогообложение при совершении операций на рынке производных инструментов" - скачать презентации по Экономике
Презентация "Налогообложение при совершении операций на рынке производных инструментов" - скачать презентации по Экономике Сценарное планирование в современном стратегическом менеджменте
Сценарное планирование в современном стратегическом менеджменте Доение коров
Доение коров Политическая система
Политическая система Сотовая связь
Сотовая связь Данкович Марина Іванівна
Данкович Марина Іванівна Обратная польская запись (ОПЗ)
Обратная польская запись (ОПЗ) Введен в соответствии с Федеральным законом от 04.10.2014 № 284-ФЗ – глава 32 НК РФ Введен в соответствии с Федеральным законом от 04.1
Введен в соответствии с Федеральным законом от 04.10.2014 № 284-ФЗ – глава 32 НК РФ Введен в соответствии с Федеральным законом от 04.1 Миссионерская деятельность
Миссионерская деятельность Предложение на абонентское юридическое обслуживание
Предложение на абонентское юридическое обслуживание Национальная безопасность Польши
Национальная безопасность Польши Организация ивент-мероприятий и бизнес событий
Организация ивент-мероприятий и бизнес событий Баженовское месторождение
Баженовское месторождение