Содержание
- 2. Биохимия – наука о молекулярных основах жизни. Биохимия изучает различные молекулы, химические реакции и процессы, протекающие
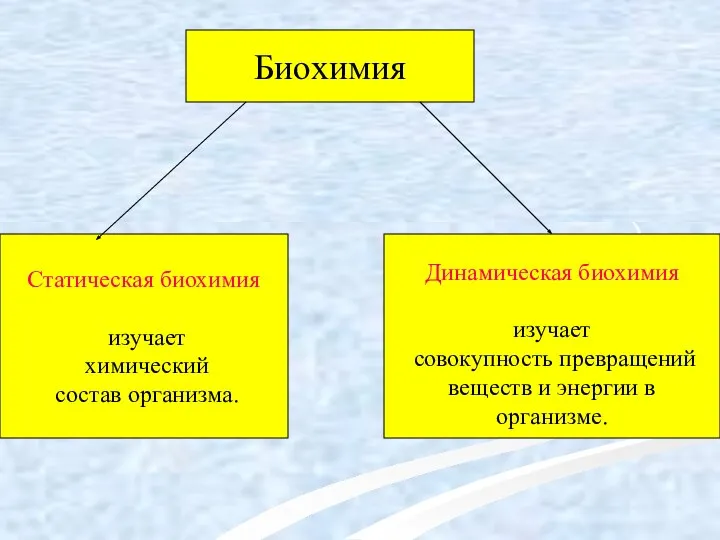
- 3. Биохимия Статическая биохимия изучает химический состав организма. Динамическая биохимия изучает совокупность превращений веществ и энергии в
- 4. В зависимости от объекта исследования выделяют биохимию человека и животных, биохимию растений, биохимию микроорганизмов.
- 5. Разделы биохимии эволюционная биохимия, энзимология, биохимия витаминов, квантовая биохимия, молекулярная биология, клиническая биохимия.
- 6. Клиническая биохимия раздел биохимии, изучающий изменения биохимических процессов в организме человека при патологических состояниях, а также
- 7. Значение клинической биохимии На современном этапе развития медицины возросло значение биохимических исследований. Применение новых лекарств, методов
- 8. Разделы клинической биохимии клиническая энзимология, клиническая нейрохимия, клиническая витаминология.
- 9. Биохимические исследования позволяют выявить причину заболевания, предложить рациональный и эффективный путь лечения, разработать методику ранней диагностики,
- 10. Основные достижения биохимии определён химический состав клеток, тканей, организма, открыта двойная спираль ДНК, многие ферменты изучены
- 11. Генная терапия Дефицит аденозиндезаминазы ведёт к развитию иммунодефицита. Ген АDА вносится в клетки больного. Вирусы как
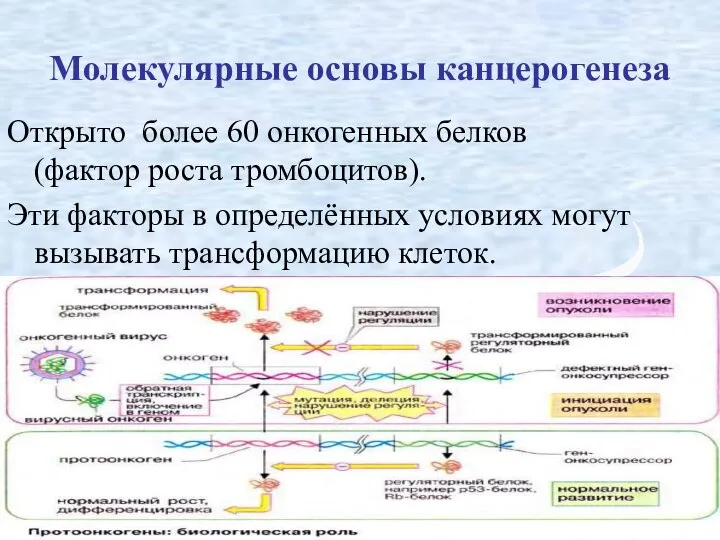
- 12. Молекулярные основы канцерогенеза Открыто более 60 онкогенных белков (фактор роста тромбоцитов). Эти факторы в определённых условиях
- 13. Молекулярные механизмы иммунитета Применяется молекулярные регуляторы иммунитета: ИЛ-2 применяется в лечении злокачественных опухолей. ИЛ-2 стимулирует созревание
- 14. Главные направления развития в области биохимии биологические мембраны и биоэнергетика, биосинтез белка, молекулярные основы памяти, рациональное
- 15. Белки высокомолекулярные азотсодержащие органические вещества, молекулы которых построены из остатков АМК, составляют основу и структуры, и
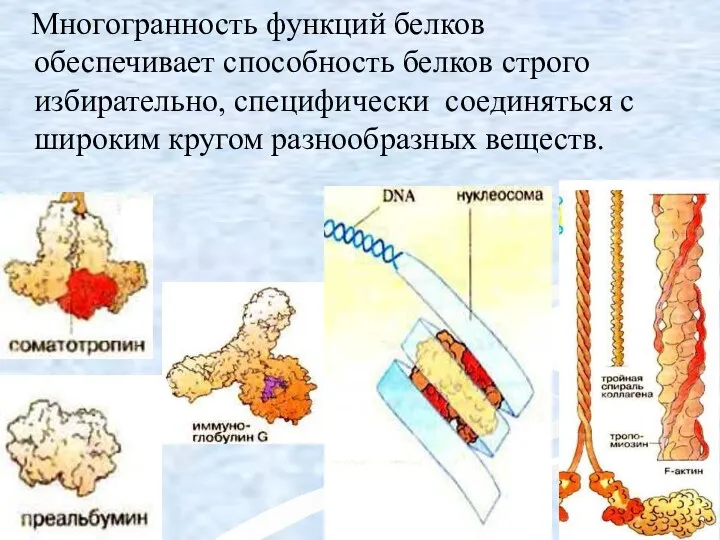
- 16. Многогранность функций белков обеспечивает способность белков строго избирательно, специфически соединяться с широким кругом разнообразных веществ.
- 17. На долю белков приходится - 70-80 % в: мышцах, печени, селезёнке, почках. - 45 % во
- 18. Состав белков Помимо углерода, кислорода, водорода, входящих в состав почти всех органических полимерных молекул, обязательным компонентом
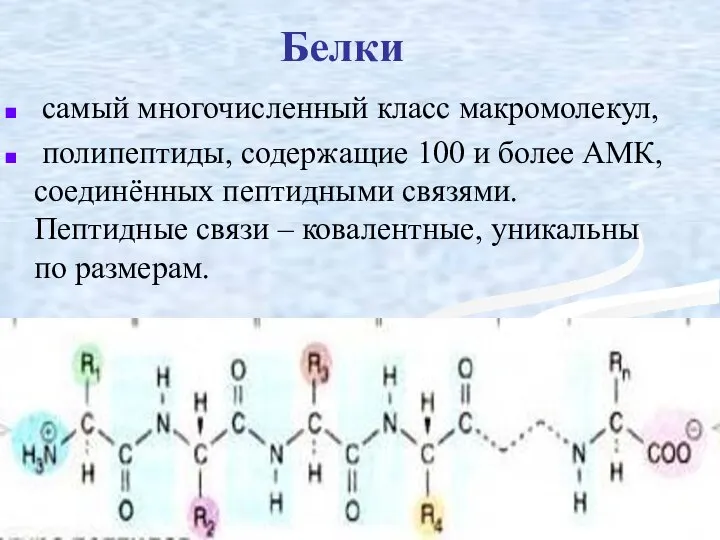
- 19. Белки самый многочисленный класс макромолекул, полипептиды, содержащие 100 и более АМК, соединённых пептидными связями. Пептидные связи
- 20. Специфические особенности белков определяются длиной пептидной цепи, различиями АМК состава, порядком чередования АМК.
- 21. Аминокислотный состав белков Помимо 20 АМК в некоторых белках обнаружены и другие АМК, а также их
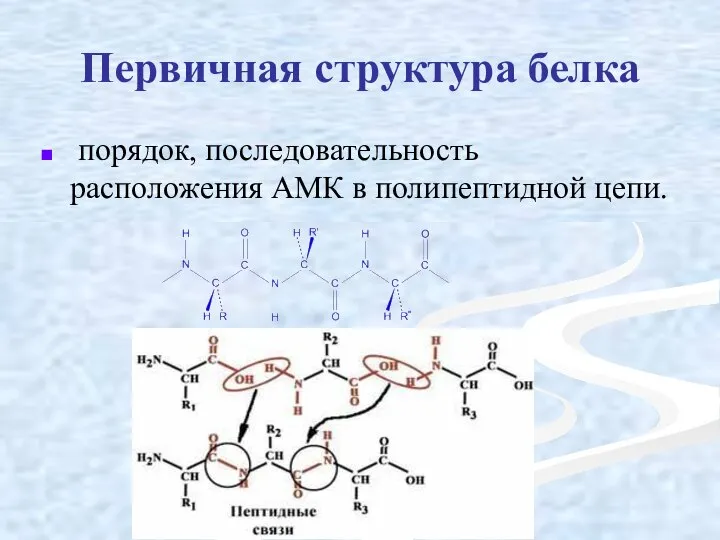
- 22. Первичная структура белка порядок, последовательность расположения АМК в полипептидной цепи.
- 23. Свойства первичной структуры белка уникальна, детерминирована генетически, её стабильность обеспечивается в основном пептидными связями, возможно участие
- 24. По частоте обнаружения АМК делят на постоянно встречающиеся, изредка встречающиеся.
- 25. Для определения АМК состава белки гидролизуют. Гидролизат: в АМК анализатов, с помощью автоматической ионообменной хроматографии, секвенатор
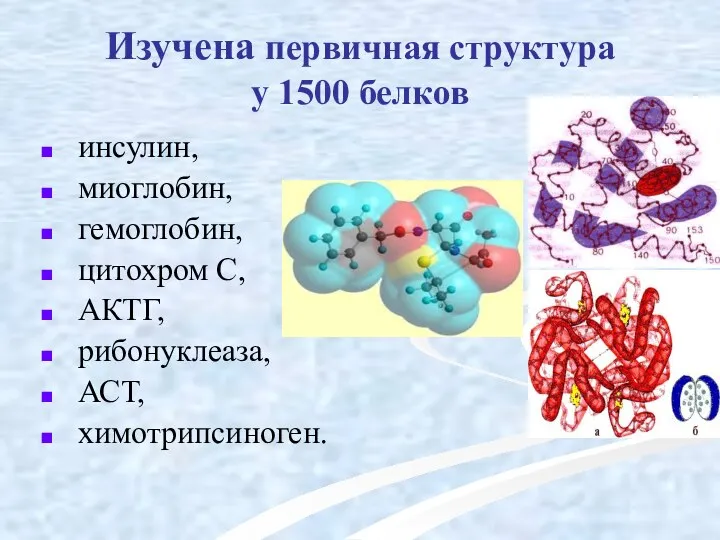
- 26. Изучена первичная структура у 1500 белков инсулин, миоглобин, гемоглобин, цитохром С, АКТГ, рибонуклеаза, АСТ, химотрипсиноген.
- 27. Даже небольшие изменения первичной структуры изменяют свойства белков. HbA1 - у здоровых людей, HbS - у
- 28. Вторичная структура пространственное расположение полипептидной цепи, поддерживаемое водородными связями С=О … Н-N между фрагментами цепи. Связи
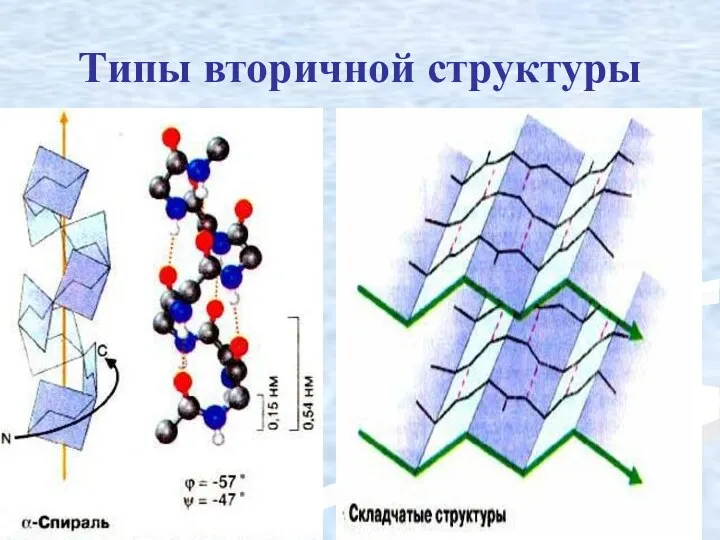
- 29. Типы вторичной структуры
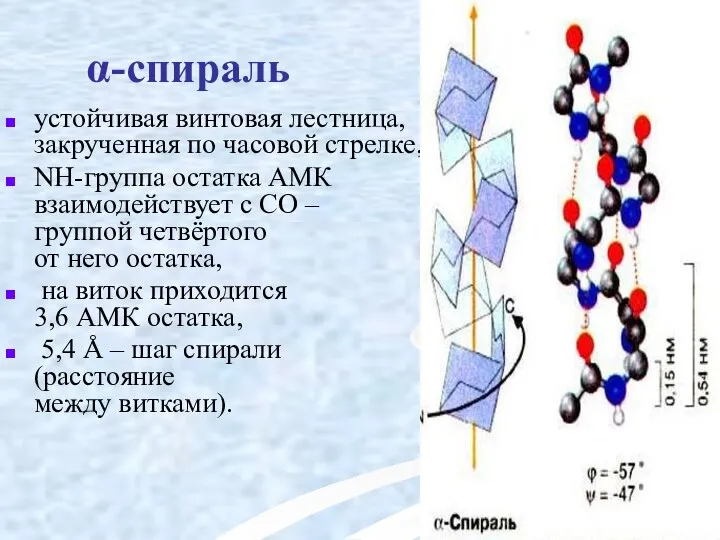
- 30. α-спираль устойчивая винтовая лестница, закрученная по часовой стрелке, NН-группа остатка АМК взаимодействует с СО – группой
- 31. АМК формирующие α-спираль: ала, лей, глн, цис, фен, тир, три, мет, вал, дестабилизирующие α-спираль: сер, иле,
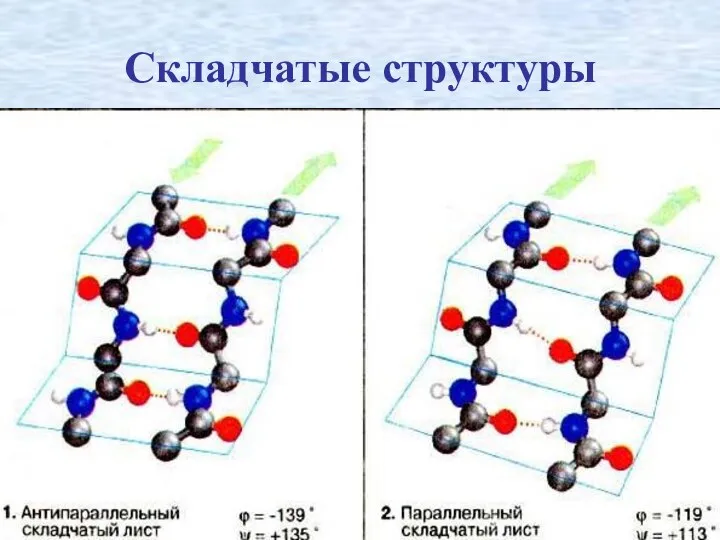
- 32. β-складчатость пептидные цепи располагаются параллельно друг другу в один слой, подобно листу, сложенному гармошкой. На каждой
- 33. Складчатые структуры
- 34. В белках встречаются области с нерегулярной вторичной структурой, которые называются беспорядочными клубками. Во многих белках присутствует
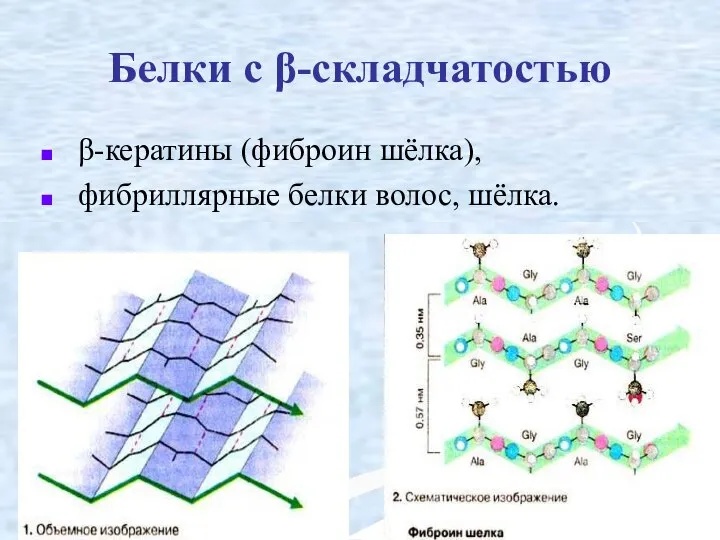
- 35. Белки с β-складчатостью β-кератины (фиброин шёлка), фибриллярные белки волос, шёлка.
- 36. Метод для расшифровки вторичной структуры рентгеноструктурный анализ. Этим методом доказано существование ещё двух уровней структурной организации
- 37. Надвторичные структуры агрегаты полипептидных цепей, обладающих собственной вторичной структурой и образующихся в белках в результате их
- 38. Домен компактная глобулярная структурная единица внутри полипептидных цепей. Домены создаются объединением и чередованием α-цепей и β-слоёв,
- 39. Третичная структура пространственное расположение пептидной цепи, поддерживаемое межрадикальными связями. Все биологические свойства белков связаны с сохранностью
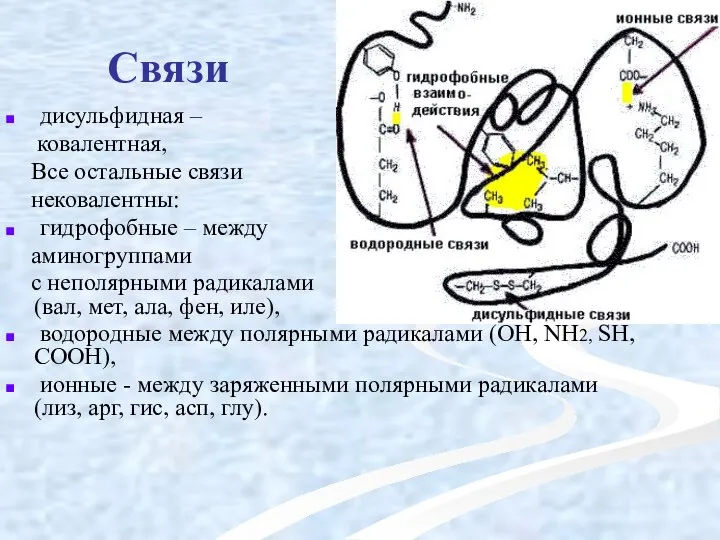
- 40. Связи дисульфидная – ковалентная, Все остальные связи нековалентны: гидрофобные – между аминогруппами с неполярными радикалами (вал,
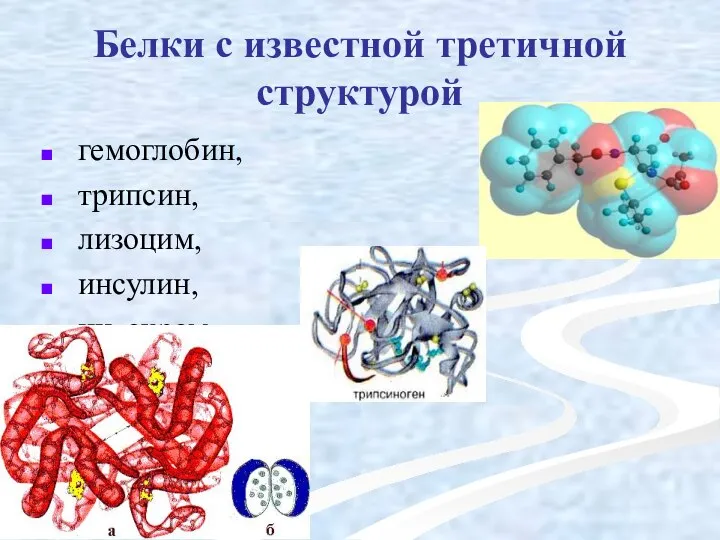
- 41. Белки с известной третичной структурой гемоглобин, трипсин, лизоцим, инсулин, цитохром.
- 42. Методы изучения третичной структуры рентгеноструктурный анализ, электронное микроскопирование.
- 44. Формы конформаций Т-форма, R-форма. Фолдинг – процесс укладки синтезированной полипептидной цепи. Описан ряд наследственных заболеваний человека,
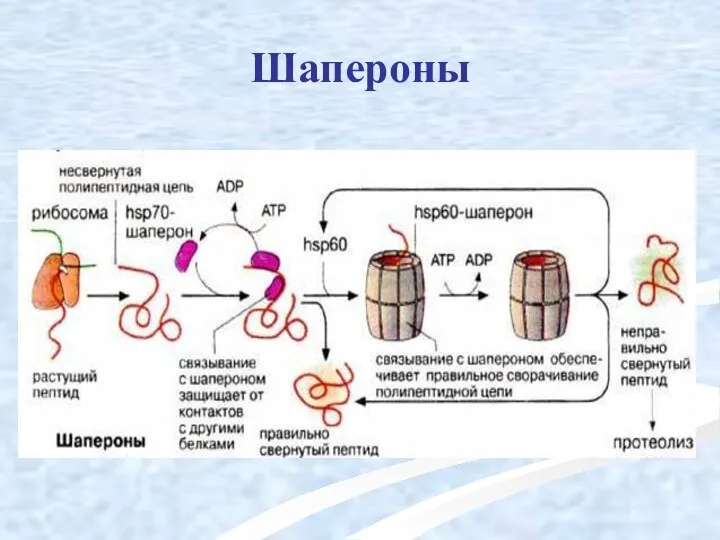
- 45. Белки теплового шока (шапероны) располагаются между N-концевым сигнальным пептидом и матричным белком, стресслимитирующая система, играют роль
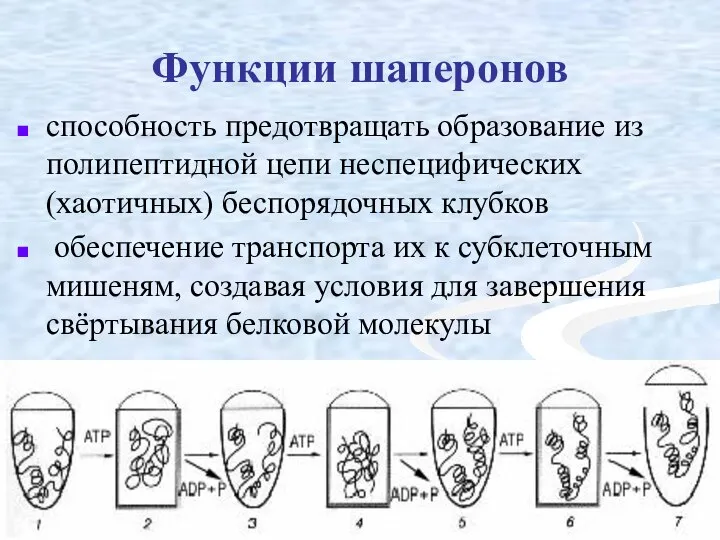
- 46. Функции шаперонов способность предотвращать образование из полипептидной цепи неспецифических (хаотичных) беспорядочных клубков обеспечение транспорта их к
- 47. Шапероны
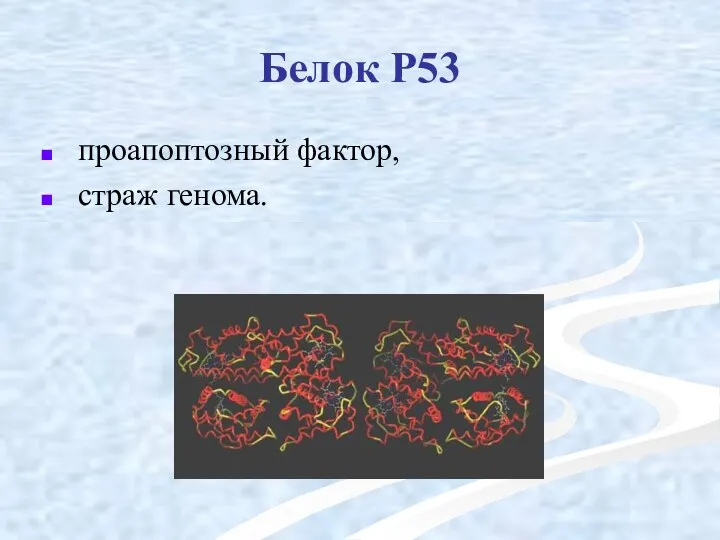
- 48. Белок Р53 проапоптозный фактор, страж генома.
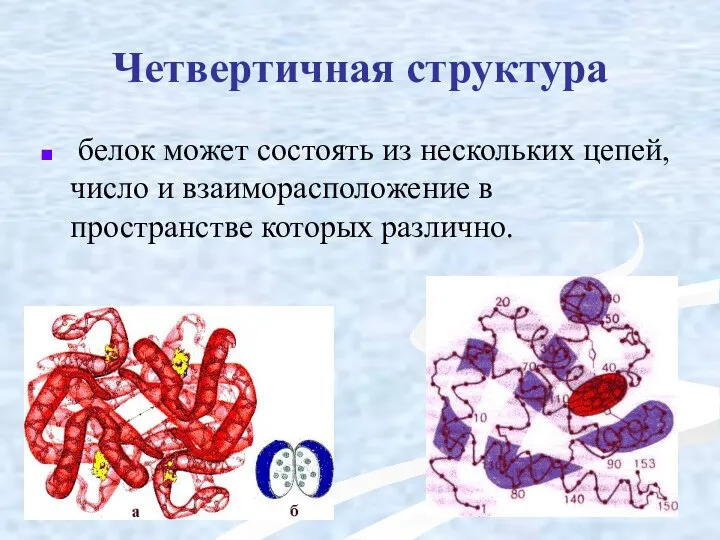
- 49. Четвертичная структура белок может состоять из нескольких цепей, число и взаиморасположение в пространстве которых различно.
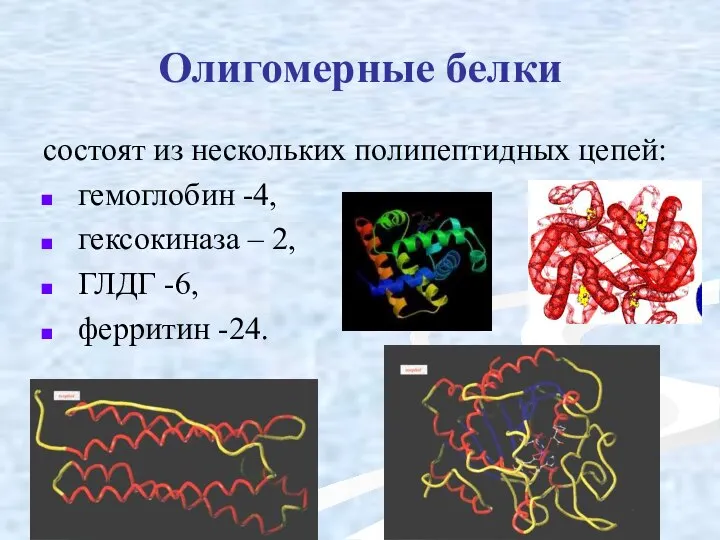
- 50. Олигомерные белки состоят из нескольких полипептидных цепей: гемоглобин -4, гексокиназа – 2, ГЛДГ -6, ферритин -24.
- 51. Связи, поддерживающие четвертичную структуру гидрофобные, ионные, водородные.
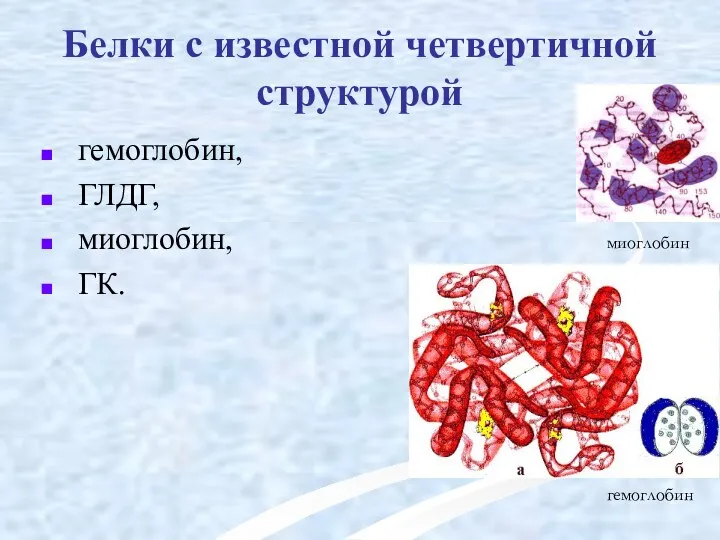
- 52. Белки с известной четвертичной структурой гемоглобин, ГЛДГ, миоглобин, ГК. миоглобин гемоглобин
- 53. Каждый белок характеризуется уникальной структурой, обеспечивающей уникальность его функций.
- 54. Пептиды органические молекулы, в состав которых входит несколько (до 30) остатков АМК, связанных пептидной связью, низкомолекулярные
- 55. Различают пептиды – гормоны: вазопрессин, окситоцин, глюкагон, пептиды, участвующие в регуляции пищеварения: гастрин, секретин, пептиды крови:
- 56. Функции белков структурная, каталитическая, регуляторная, рецепторная, иммунологическая, защитная, транспортная, сократительная, опорная, обезвреживающая, энергетическая, геннорегуляторная, создание биопотенциалов
- 58. Скачать презентацию



































 Товароведческая экспертиза лекарственных средств
Товароведческая экспертиза лекарственных средств Квадратное уравнение Ладанова И.В. МКОУ «Верх-Жилинская ООШ»
Квадратное уравнение Ладанова И.В. МКОУ «Верх-Жилинская ООШ» Образование в США
Образование в США GIA 13
GIA 13 Школьная форма
Школьная форма Психологические проблемы педагогического оценивания (Морозова Д.М., 4 курс ППО)
Психологические проблемы педагогического оценивания (Морозова Д.М., 4 курс ППО) Презентация "Дали, Сальвадор" - скачать презентации по МХК
Презентация "Дали, Сальвадор" - скачать презентации по МХК Углы
Углы Гигиеническая оценка типовых проектов лечебно-профилактических учреждений
Гигиеническая оценка типовых проектов лечебно-профилактических учреждений  Тема 1. Финансы предприятий и финансовый менеджмент
Тема 1. Финансы предприятий и финансовый менеджмент  Молодежный сленг и жаргон
Молодежный сленг и жаргон Ведение воинского учета
Ведение воинского учета Бушманова Наталья Васильевна, учитель начальных классов МБОУ «Средняя общеобразовательная школа№1 имени Героя России М.Г. Ефремо
Бушманова Наталья Васильевна, учитель начальных классов МБОУ «Средняя общеобразовательная школа№1 имени Героя России М.Г. Ефремо Кафедра физико – математических дисциплин.
Кафедра физико – математических дисциплин. Документальное оформление хозяйственных операций и его влияние на способы совершения преступлений
Документальное оформление хозяйственных операций и его влияние на способы совершения преступлений Агентский договор и договор комиссии Выполнила: студентка 4-го курса ФТД ДС.1 Восколович Юля
Агентский договор и договор комиссии Выполнила: студентка 4-го курса ФТД ДС.1 Восколович Юля  Генетика иммунитета
Генетика иммунитета  Презентация Речь, воображение
Презентация Речь, воображение  Презентация "Влияние древних культур на современность" - скачать презентации по МХК
Презентация "Влияние древних культур на современность" - скачать презентации по МХК Уголовная ответственность лиц с психическими расстройствами, не исключающими вменяемости
Уголовная ответственность лиц с психическими расстройствами, не исключающими вменяемости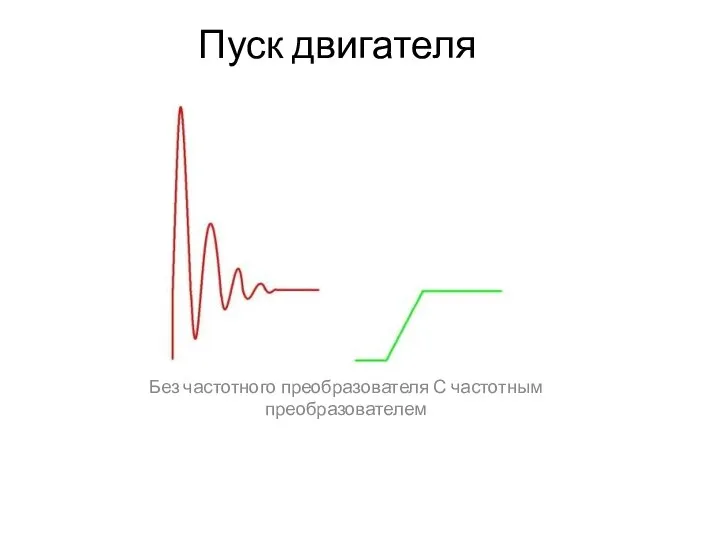 Пуск двигателя без частотного преобразователя с частотным преобразователем
Пуск двигателя без частотного преобразователя с частотным преобразователем 23456789101112131415161718192021. - презентация
23456789101112131415161718192021. - презентация Товарная номенклатура внешнеэкономической деятельности: классификация товаров, предварительное решение. Лекция 4
Товарная номенклатура внешнеэкономической деятельности: классификация товаров, предварительное решение. Лекция 4 «Различные действия с дробями»
«Различные действия с дробями» Занимательное черчение (7 класс)
Занимательное черчение (7 класс) Древняя Индия
Древняя Индия Применение ОРС технологий
Применение ОРС технологий Свойства степени (7 класс) - презентация по Алгебре_
Свойства степени (7 класс) - презентация по Алгебре_