Содержание
- 2. « Просто знать - ещё не всё, знания нужно уметь использовать». Гёте
- 3. видео
- 4. Получение соляной кислоты: 1.В промышленности получают сжиганием водорода в хлоре и растворением продукта реакции в воде.
- 5. Химические свойства: 1. Изменение окраски индикатора (лакмус- красный) 2. Взаимодействует с металлами Mg + 2HCl →
- 6. Вывод: Если металл находится в ряду, составленном Н.Н.Бекетовым, до водорода, то выделяется водород и образуется соль.
- 7. 3. Взаимодействует с основными и амфотерными оксидами: MgO + 2HCl → MgCl2 + H2O ZnO +
- 8. 4. Взаимодействует с основаниями: HCl + KOH → KCl + H2O 3HCl + Al(OH)3 → AlCl3
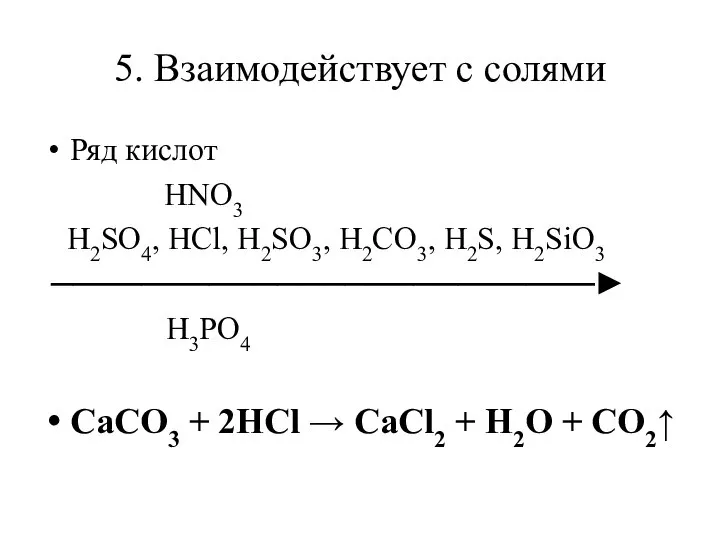
- 9. 5. Взаимодействует с солями Ряд кислот HNO3 H2SO4, HCl, H2SO3, H2CO3, H2S, H2SiO3 ────────────────────────► H3PO4 CaCO3
- 10. Вывод: В соответствии с рядом кислот, каждая предыдущая кислота может вытеснить из соли последующую, образуется другая
- 11. 6. Взаимодействует с нитратом серебра HCl + AgNO3 → AgCl↓ + HNO3 выпадает осадок белого цвета,
- 12. Вывод: Нитрат серебра является реактивом на соляную кислоту и её соли т.е. используется в качестве качественной
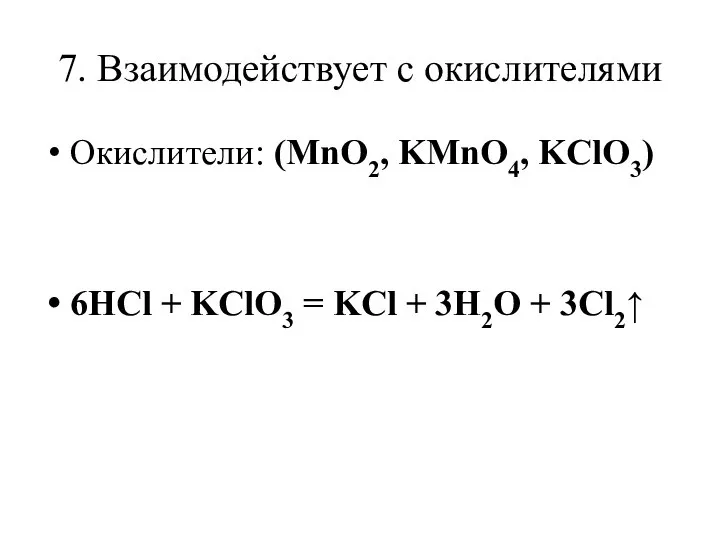
- 13. 7. Взаимодействует с окислителями Окислители: (MnO2, KMnO4, KClO3) 6HCl + KClO3 = KCl + 3H2O +
- 14. Вывод: Во всех нами изученных реакциях получились хлориды- соли соляной кислоты.
- 15. Применение соляной кислоты Входит в состав желудочного сока и способствует перевариванию белковой пищи Для производства лекарств,
- 16. Применение солей - хлоридов KCl - удобрение, используется также в стекольной и химической промышленности. HgCl2 -
- 17. Задания для закрепления №1. Осуществите превращения по схеме: HCl → Cl2 → AlCl3 →Al(OH)3 → Al2O3
- 18. №3. Решите задачу: Какое количество алюминия прореагирует с избытком соляной кислоты для получения 5,6 л водорода
- 20. Скачать презентацию















 Тұздар гидролизі
Тұздар гидролизі Компоненты нефти, газов и нефтепродуктов. Состав, строение, свойства. Насыщенные углеводороды
Компоненты нефти, газов и нефтепродуктов. Состав, строение, свойства. Насыщенные углеводороды Катаболизм жирных кислот
Катаболизм жирных кислот Карбон Колообіг в природі
Карбон Колообіг в природі  Основы общей химии
Основы общей химии Chemical Formulas and Nomenclature of compounds
Chemical Formulas and Nomenclature of compounds Химия и стирка
Химия и стирка  Кислородные соединения азота
Кислородные соединения азота Аміак
Аміак  Антисептические и дезинфицирующие средства
Антисептические и дезинфицирующие средства Формальная кинетика. Предмет химической кинетики
Формальная кинетика. Предмет химической кинетики Алкины. Ацетилен
Алкины. Ацетилен Общая фармакопейная статья
Общая фармакопейная статья Презентация по Химии "Алюминий как химический элемент и как простое вещество" - скачать смотреть
Презентация по Химии "Алюминий как химический элемент и как простое вещество" - скачать смотреть  Присоединение аммиака и аминов
Присоединение аммиака и аминов Гексан С6Н14
Гексан С6Н14 Carbohydrate metabolism
Carbohydrate metabolism Переработка углеводородных газов. Поточные схемы завода
Переработка углеводородных газов. Поточные схемы завода Углерод
Углерод Полиэтилен - термопластичный полимер этилена
Полиэтилен - термопластичный полимер этилена Золото. Свойство золота
Золото. Свойство золота Природный газ
Природный газ Использование энергии солнца на земле
Использование энергии солнца на земле Введение в биохимию
Введение в биохимию Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Д. И. Менделеев
Д. И. Менделеев Методы выделения и анализа биологически активных веществ
Методы выделения и анализа биологически активных веществ Оксиды. Подготовка к ОГЭ
Оксиды. Подготовка к ОГЭ